引用本文: 余游, 鄒昌, 譚鵬, GuyRomeo Kenmegne, 尹一杰, 黃申博, 何帥, 方躍. 復合型髖臼骨折圍手術期多次靜脈使用氨甲環酸的有效性及安全性評價. 華西醫學, 2024, 39(3): 461-467. doi: 10.7507/1002-0179.202311281 復制
版權信息: ?四川大學華西醫院華西期刊社《華西醫學》版權所有,未經授權不得轉載、改編
髖臼骨折通常由高能量的創傷引起,由于其解剖結構復雜并常伴有并發癥,因此致殘率及死亡率較高[1]。根據 Judet-Letournel 分型,髖臼骨折分為簡單骨折和復合型骨折[2-3];恢復髖臼與股骨頭匹配關系,切開復位內固定已經成為髖臼骨折的標準治療方法[4-5],但髖臼骨折圍手術期總失血量約 1 000 mL,通常需要輸血以糾正貧血[6-9],而且復合型骨折比簡單骨折創傷更大,機體纖溶亢進易導致患者更多的失血。因此,骨科創傷醫生需要采用各種干預措施來降低圍手術期失血量、減少輸血。氨甲環酸(tranexamic acid, TXA)是一種人工合成的賴氨酸衍生物,作為圍手術期常用的抗纖溶藥物,通過降低纖溶酶對止血纖維蛋白的溶解作用,從而減少圍手術期的失血,同時不會引起下肢深靜脈血栓形成。TXA 在骨科加速康復中使用極其廣泛,尤其在關節置換術中和術后的應用更發揮了突出作用;但在骨盆髖臼骨折中應用經驗尚顯不足[10]。關于 TXA 在髖臼骨折圍手術期使用的相關文獻報道少,對減少失血的有效性存在爭議,多次靜脈使用 TXA 的臨床研究尚無報道,面對復合型髖臼骨折創傷后血管內膜損傷和血液高凝狀態,靜脈滴注 TXA 形成靜脈血栓風險的安全性尚需進一步證實。本研究以在四川大學華西醫院骨科/創傷中心擬行復合型髖臼骨折切開復位內固定術患者為研究對象,對比圍手術期靜脈使用 TXA 不同方案,分析患者隱性失血量、總失血量、輸血率、靜脈血栓發生率結果,以評估多次靜脈滴注 TXA 是否可減少復合型髖臼骨折圍手術期失血,促進術后快速康復,以及其安全性和可能增加血栓事件的風險。
1 對象與方法
1.1 研究對象
選取 2021 年 9 月-2022 年 12 月四川大學華西醫院骨科/創傷中心骨盆髖臼組收治的擬行復合型髖臼骨折切開復位內固定術患者。納入標準:① 年齡 18~65 歲,受傷至入院時間≤14 d;② 術前血紅蛋白(hemoglobin, Hb)>90 g/L 或紅細胞壓積(hematocrit, Hct)>30%、血小板計數>50×109/L、凝血酶原時間<16 s、部分凝血酶原時間<47 s;③ 術前影像學檢查(X 線片及 CT 片)按照 Judet-Letournel 分型符合髖臼復合型骨折[2-3]。排除標準:① 血栓形成高危者,包括心房顫動、心臟起搏器和支架植入術后;② 既往有血栓病史或者雙下肢靜脈彩色多普勒超聲(彩超)提示有深靜脈血栓者;③ 既往曾對 TXA 過敏或使用禁忌者;④ 嚴重的肝腎功能不全者;⑤ 同時行髖臼骨折及其他部位手術者;⑥ 患有嚴重的血液類疾病,有出血性疾病或既往有出血性疾病病史,長期口服抗血小板、抗凝藥物者;⑦ 既往有患側髖部骨折、髖臼骨骼畸形、髖部手術者;⑧ 病理性骨折或有活動性感染(體表、肺部或泌尿系統)者。經四川大學華西醫院生物醫學倫理委員會審查[2019年審(1156)號],所有患者均簽署知情同意書。
本研究參考了 Spitler 等[11]關于髖臼骨折圍手術期失血量的研究結果估計所需的樣本量,采用了 GPower 3.1 軟件進行重復測量方差分析。在分析中,設定α=0.05 和檢驗效能為 0.8。根據這些參數計算得出研究至少需要 29 例。因此,本研究共需招募患者 60 例,每組各 30 例,以確保統計分析的有效性和結果的可靠性。
1.2 研究方法
1.2.1 分組
按照前瞻性雙盲隨機原則,將納入患者分為對照組和試驗組。具體方法:將患者從 1 ~ 60 編號,從隨機數字表 1~1 000 中任意一個數開始獲取 60 個隨機數字,每個患者沿同一方向順序獲取一個隨機數字;然后根據隨機數字大小排序,每 30 個數字一組,患者對應到相應的組別。在本研究中,一組研究人員和研究參與者只知道編號,不能預測研究參與者的具體入組情況,執行者為手術室及病房護理人員,病歷及臨床試驗數據管理系統由另一組研究人員進行記錄、資料收集及匯總工作。對照組:術前 10~15 min 靜脈滴注 TXA 2 g;試驗組:術前 10~15 min 靜脈滴注 TXA 2 g,在第 1 劑 TXA 靜脈滴注結束后第 3、6 小時各再次靜脈滴注 TXA 1 g。
1.2.2 手術方法
本研究所有手術均由同一組主任醫師獨立完成,患者使用全身麻醉,麻醉師控制性降壓,血壓保持在 90 / 60 mm Hg(1 mm Hg=0.133 kPa)的水平,手術中的肌松度滿意。
根據患者骨折情況選擇采用了改良的 stoppa+髂窩前方入路、Kocher-Langenbeck 后方入路(K-L 入路)和前后聯合入路的方法之一。① 改良的 stoppa+髂窩前方入路適用于除后壁、后柱骨折類型的其他髖臼復合型骨折。這種入路方式采用仰臥位,皮膚切口由臍部至恥骨聯合縱向連接中遠段約 8~10 cm,依序切開皮膚和皮下組織,顯露腹白線縱向切開,將腹直肌兩側拉開并保留止點,外推患側腹壁肌。在切開腹橫筋膜后,進入腹膜前間隙,向外側解剖,進入 Retzius 間隙,顯露結扎閉孔動靜脈與髂外或腹壁下動靜脈之間的交通支(即死亡冠血管),剝離暴露恥骨聯合至骶髂關節真性骨盆緣,顯露內側窗骨盆前環;髂窩前方入路從髂前上嵴沿髂嵴向后切開皮膚、皮下組織,緊貼髂骨內板骨膜下剝離至髂窩,顯露外側窗骨盆后環;骨折予以頂棒、骨盆復位螺釘、骨盆復位鉗等器械配合患肢牽引等方法復位,結合克氏針、螺釘等,鋼板塑形固定。C 臂透視骨折復位情況及內固定位置、長度,確定內固定物未進入髖臼。② K-L 入路適用于橫行伴后壁、后柱伴后壁等骨折,這種入路方式采用俯臥位,切開皮膚、皮下組織以及闊筋膜,鈍性分離臀大肌和臀中肌,部分切斷梨狀肌和短外旋肌群,顯露并保護坐骨神經。顯露髖臼后方,通過使用頂棒、骨盆復位螺釘、骨盆復位鉗等器械,直視下復位骨折端,然后鋼板塑形進行固定。通過 C 臂透視觀察骨折復位情況以及內固定的位置和長度,確保內固定物未進入髖臼。③ 單一入路骨折無法復位或固定滿意的類型采用前后聯合入路。
1.2.3 圍手術期處理方法
在本研究中,手術前后的抗凝措施遵循中國骨科大手術靜脈血栓栓塞癥預防指南[12],采用藥物聯合物理措施進行指導。術中輸血的決策是由麻醉醫師和手術醫師共同根據術中失血量及 Hb 檢查結果(術中血氣分析)來確定。術后輸血的指標是 Hb<70 g/L 或 Hct<25%[13-14]。所有患者術后均留置創腔負壓引流管,并在術后 48 h 內拔除。在創腔引流量增多、Hb 或 Hct 進行性下降的情況下,暫停抗凝治療,直至患者的 Hb 或 Hct 穩定[12]。出院前,對所有患者進行雙下肢血管超聲檢查,以確認是否有血栓形成。如果住院期間患者出現下肢腫脹并伴有疼痛,立即進行下肢血管超聲檢查,以了解下肢循環情況。肺栓塞的診斷則基于患者的臨床表現和胸部 CT 造影等檢查結果[15]。在術后康復過程中,根據內固定的穩定性決定患者是否可以坐起,并鼓勵其進行早期的股四頭肌功能鍛煉及踝泵鍛煉。此外,一旦雙下肢血管超聲檢查排除了血栓形成,采用氣壓泵對患者進行治療,以進一步預防血栓形成,促進其術后康復。
1.3 觀察指標
1.3.1 一般資料
患者性別、年齡、體質量指數、手術入路和手術時長。
1.3.2 有效性評價指標
患者的血容量、失血量、隱形失血量、輸血率。血容量根據 Nadler 方程[16]計算;記錄術前、術后第 1 天及第 3 天 Hb、Hct;總失血量根據 Gross 方程[17]計算;隱性失血量=(總失血量+輸血量)-(術中失血量+術后 48 h 內引流量);每組患者輸血率=(術中輸血患者例數+術后輸血患者例數)/每組總例數。
1.3.3 纖溶指標
術前、術后第 1 天及第 3 天的纖維蛋白原(fibrinogen, Fib)以及 D-二聚體。
1.3.4 安全性評價指標
靜脈血栓事件發生率:下肢靜脈彩超報告的靜脈血栓分深靜脈血栓(deep vein thrombosis, DVT)和肌間靜脈血栓(intramuscular vein thrombosis, IVT)兩類統計。
1.4 統計學方法
采用 SPSS 25.0軟件分析數據。正態分布的計量資料采用均數±標準差表示,組間比較采用獨立樣本 t 檢驗;非正態分布的計量資料采用中位數(下四分位數,上四分位數)表示,組間比較采用 Mann-Whitney 秩和檢驗;計數資料采用例數和/或百分比表示,組間比較采用χ2 檢驗。對于重復測量資料,如果滿足正態分布和方差齊性則采用重復測量方差分析(不符合 Mauchly 球形檢驗假設時采用 Greenhouse-Geisser 校正分析),否則采用 Kruskal-Wallis 非參數檢驗。雙側檢驗水準α=0.05。
2 結果
2.1 一般資料
共納入患者 60 例,每組各 30 例。所有患者均按計劃進行手術并完成相關指標檢查。兩組一般資料比較見表1。可見,兩組患者的性別、年齡、體質量指數、手術入路及手術時長比較,差異均無統計學意義(P>0.05)。
2.2 有效性評價
2.2.1 Hb 與 Hct
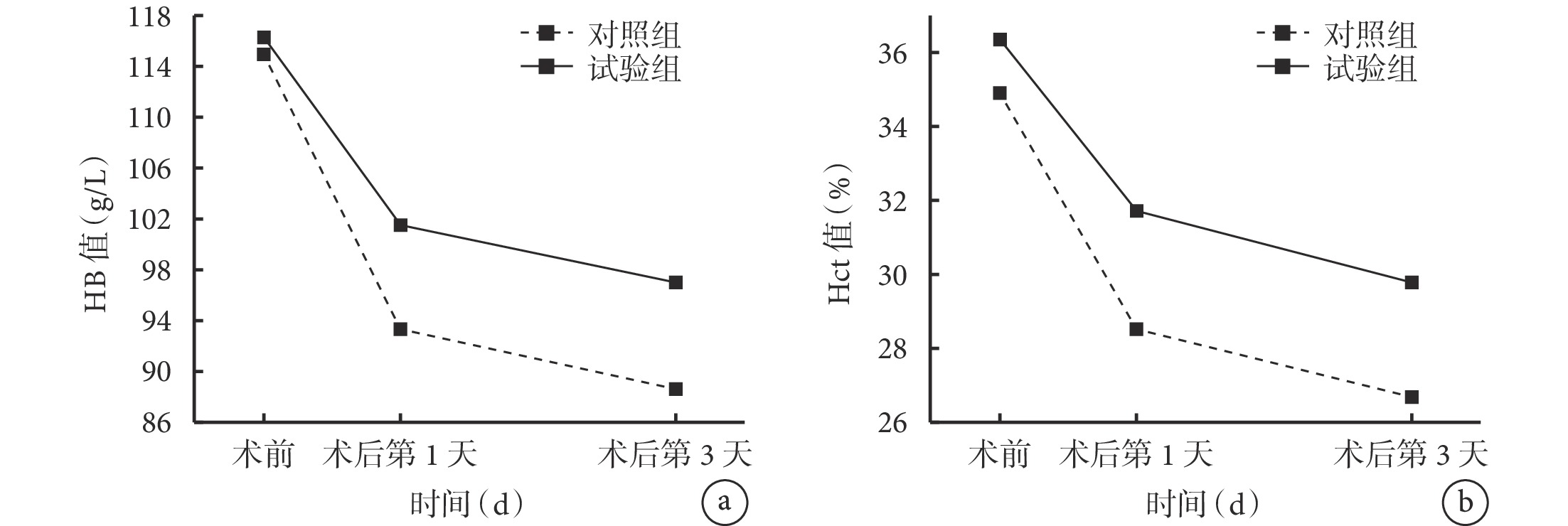
兩組患者的 Hb 和 Hct 變化趨勢見圖1。可見,術前,對照組和試驗組的 Hb[(114.93±16.35) vs.(116.20±17.92) g/L]、Hct[(34.90±4.98)% vs.(36.33±5.52)%]比較,差異均無統計學意義(P>0.05);術后第 1 天,對照組的 Hb[(93.33±16.29)g/L vs.(101.43±14.88)g/L]、Hct[(28.57±5.16)% vs.(31.70±4.40)%]均低于試驗組(P<0.05);術后第 3 天,對照組的 Hb[(88.60±17.04)g/L vs.(97.03±14.73)g/L]、Hct[(26.70±4.95)% vs.(29.73±4.02)%]均低于試驗組(P<0.05)。組內比較顯示,兩組患者術后第 1 天及術后第 3 天的 Hb 及 Hct 均較術前下降(P<0.05); 術后第 1 天與術后 第 3 天的 Hb 及 Hct 比較,差異均無統計學意義 (P>0.05)。兩組患者 Hb 及 Hct 值的重復測量方差分析不符合球形檢驗球對稱性(P<0.05),校正分析結果顯示,Hb 及 Hct 時間效應有統計學意義(F=88.485、106.426,P<0.001),組別效應無統計學意義(F=2.388、4.964,P=0.128、0.229),組別與時間不存在交互作用(F=2.547、2.531,P=0.087、0.117)。
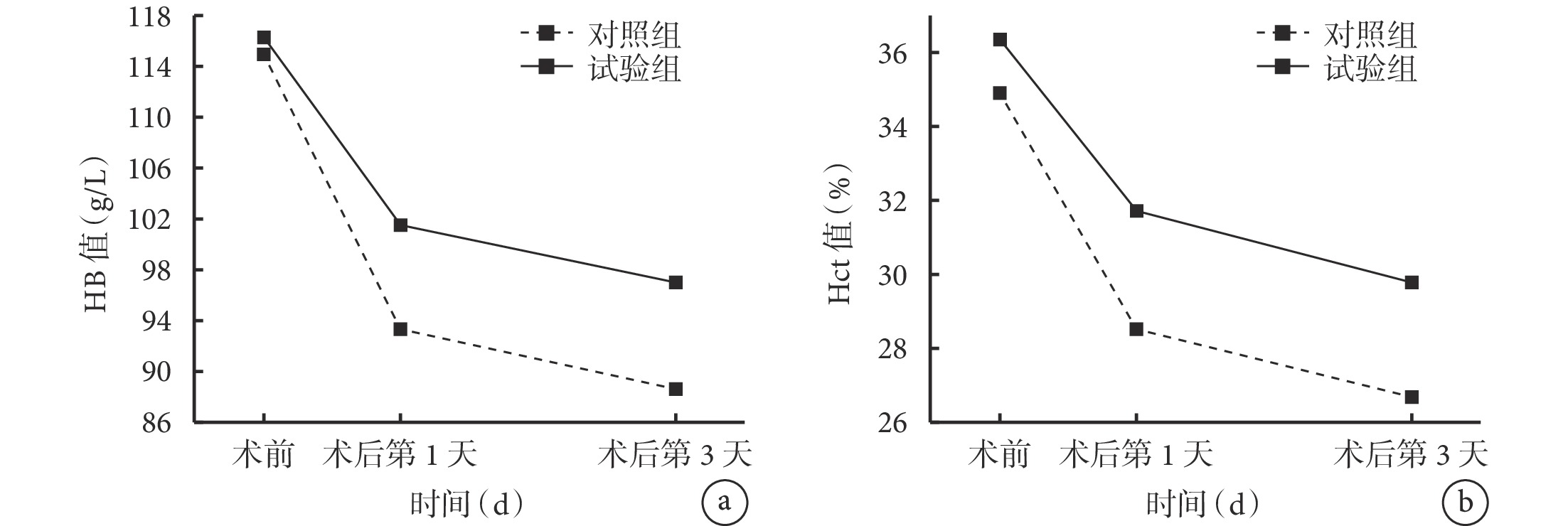 圖1
兩組患者的 Hb 和 Hct 變化趨勢(n=30)
圖1
兩組患者的 Hb 和 Hct 變化趨勢(n=30)
a. Hb;b. Hct
2.2.2 失血相關指標
兩組患者失血相關指標比較見表2。可見,除血容量、術中失血量外(P>0.05),兩組的術后 48 h 引流量、總失血量、隱形失血量和輸血率比較,差異均有統計學意義(P<0.05)。
2.3 纖溶指標
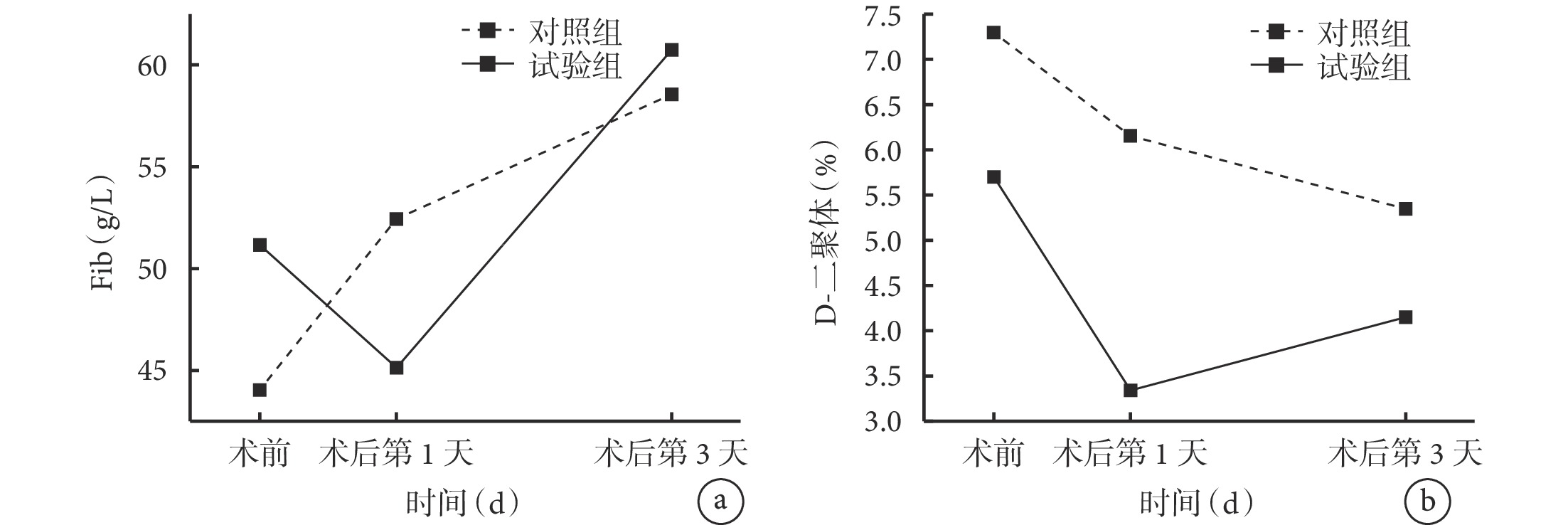
兩組患者的 Fib 和 D-二聚體變化趨勢見圖2。可見,術前,對照組和試驗組的 Fib[(4.40±1.81) vs.(5.11±1.61) g/L]、D-二聚體[(7.28±3.89)% vs.(5.69±2.81)%]比較,差異均無統計學意義(P>0.05);術后第 1 天,對照組的 Fib[(5.23±1.45) vs.(4.51±1.21) g/L]、D-二聚體[(6.16±3.42)% vs.(3.32±1.57)%]均高于試驗組(P<0.05);術后第 3 天,對照組和試驗組的 Fib[(5.85±1.85) vs.(6.07±1.20) g/L]、D-二聚體[(5.36±2.83)% vs.(4.15±2.06)%]比較,差異均無統計學意義(P>0.05)。組內比較顯示,對照組術后第 1 天的 Fib 較術前上升、D-二聚體較術前下降,試驗組術后第 1 天的 Fib 較術前下降,但差異均無統計學意義(P>0.05);與術前比較,試驗組術后第 1 天的 D-二聚體下降(P<0.05),兩組術后第 3 天的 Fib 均升高、D-二聚體均下降(P<0.05);試驗組術后第 3 天的 Fib 高于術后第 1 天(P<0.05);對照組術后第 1 天與術后第 3 天的 Fib 和 D-二聚體比較,試驗組術后第 1 天與術后第 3 天的 D-二聚體比較,差異均無統計學意義(P>0.05)。兩組患者 Fib 重復測量方差分析不符合球形檢驗球對稱性(P<0.05),進行校正分析結果顯示,時間效應有統計學意義(F=29.716,P<0.001),組別效應無統計學意義(F=0.041,P=0.841),組別與時間存在交互作用(F=12.227,P<0.001)。兩組患者 D-二聚體的重復測量方差分析符合球形檢驗球對稱性(P=0.244),分析結果顯示,時間效應有統計學意義(F=17.375,P<0.001),組別效應無統計學意義(F=3.154,P=0.081),組別與時間存在交互作用(F=8.933,P<0.001)。
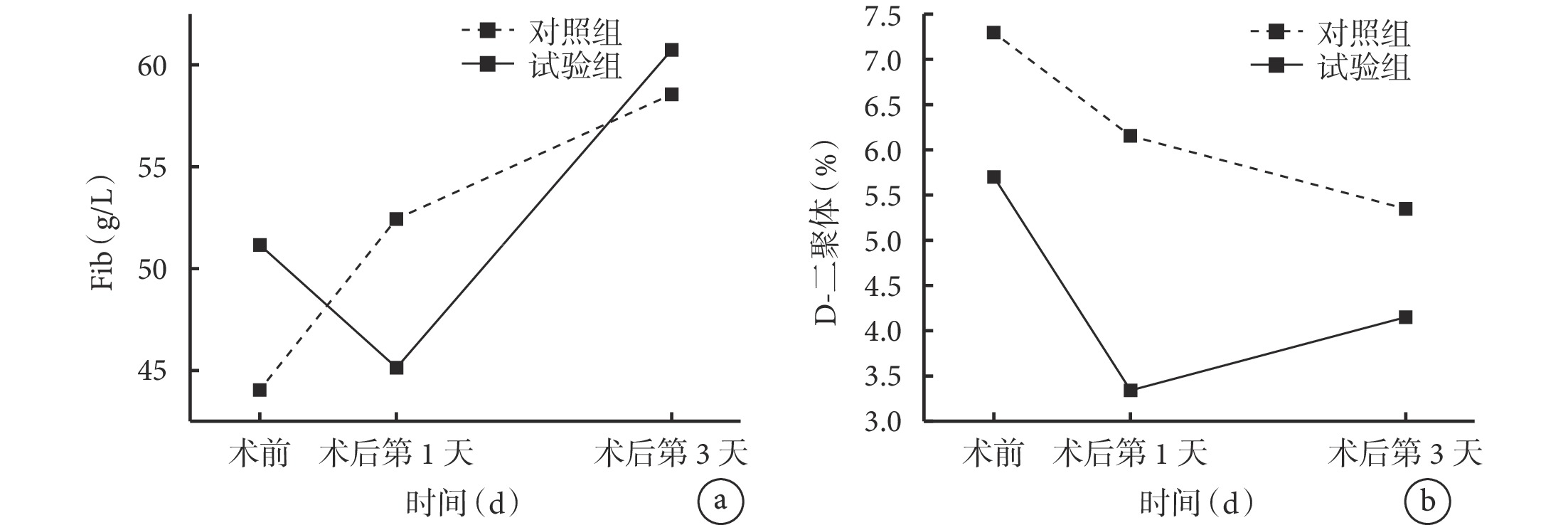 圖2
兩組患者的 Fib 和 D-二聚體變化趨勢(n=30)
圖2
兩組患者的 Fib 和 D-二聚體變化趨勢(n=30)
a. Fib;b. D-二聚體
2.4 安全性評價
兩組患者術后血栓發生率比較見表3。可見,患者術前下肢血管彩超中均未發現 DVT,兩組 IVT 發生率差異無統計學意義(P>0.05)。術后兩組的 DVT 及 IVT 發生率比較,差異均無統計學意義(P>0.05),且患者均未出現肺栓塞情況。
3 討論
復合型髖臼骨折的切開復位內固定術因髖部解剖結構的復雜性以及周圍豐富的血管網,導致圍手術期失血量多,輸血率高[6-9]。為了解決這一問題,通過采取血液稀釋、自體血回輸、圍手術期注射重組人促紅細胞生成素以及蔗糖鐵等方法被用于減少髖臼骨折圍手術期失血。盡管 Bigsby 等[18]表明自體血回輸相對輸注同種異體血具有一定成本效益,但實際治療費用仍較高;而重組人促紅細胞生成素、蔗糖鐵等方法的使用周期相對長、監測指標多等[19]。對于復合型髖臼骨折患者,找到一種更為經濟、方便、有效、安全的治療方法是骨科創傷醫生所面臨的挑戰。TXA 是一種傳統的抗纖溶藥物,在骨科加速康復專家共識中明確指出其是安全有效的[10,20],因此本研究將單次靜脈滴注 TXA 作為對照組,但并沒有設置未使用 TXA 作為空白對照組。Andersson 等 [21]對 TXA 藥代動力學研究發現,靜脈滴注 5~15 min 血藥濃度達到峰值,半衰期約為 3 h。Xie 等[22]研究發現機體纖溶亢進狀態于術后 6 h 達到峰值,并持續 18~24 h。因此,本研究根據 TXA 的半衰期及纖溶峰值時間,采用成熟的關節置換多次靜脈使用 TXA 方案設置試驗組用藥,于術前第 1 劑靜脈使用 2 g TXA 后 3 h 及 6 h 各追加 1 d TXA。目前尚無復合型髖臼骨折圍手術期多次靜脈使用 TXA 的有效性和安全性的研究報告,值得進一步深入研究。
3.1 有效性評價
TXA 通過競爭性阻斷纖溶酶原的賴氨酸位點,有效阻止纖溶酶的活化,從而抑制纖維蛋白凝塊的分解,發揮抗纖溶作用并產生止血效果。因此,TXA 主要適用于各類手術或創傷后因纖維蛋白過度溶解導致的出血問題,尤其在需要精確操作的復雜骨科手術中。TXA 的使用能有效減少圍手術期的失血,節約血液制品,減少異體輸血的潛在風險,同時降低了患者的住院費用。姚歡等[23]報道多次靜脈使用 TXA 可有效且安全地減少全髖關節置換圍手術期的隱性失血和 Hb 的丟失,特別是在術后 3、6 h 多次給藥的效果更為顯著。Maniar 等[24]研究表明,在全膝關節置換圍手術期至少使用 2 次 TXA 才能減少總失血量,多次使用的止血效果優于單次使用。本研究發現,兩組的 Hb 和 Hct 在術后呈現出下降趨勢,但兩組比較差異無統計學意義(P>0.05)。然而,相比于對照組,試驗組的 Hb 和 Hct 下降幅度相對較小。這一發現說明術后多次靜脈使用 TXA 可能在一定程度上減輕了 Hb 和 Hct 的下降。此外,兩組患者在術后 48 h 引流量、總失血量及隱性失血量方面的差異進一步支持了 TXA 在減少復合型髖臼骨折圍手術期失血方面的潛在效益。
隱性失血是評估術后失血的重要指標之一,因術后血液滲透至組織間隙、溶血作用以及氧化損傷紅細胞膜等因素導致,側面說明了術后機體的纖溶反應水平。有研究報道也支持 TXA 在減少全髖關節置換術圍手術期隱性失血方面的效用[25-26]。本研究通過 Nadler 公式計算患者血容量及 Gross 方程計算患者的總失血量,結合顯性失血量及輸血量計算出隱性失血量。最終結果顯示,試驗組中多次靜脈使用 TXA 可以有效地減少復合髖臼骨折圍手術期隱形失血量。在本研究中,患者的 Fib 和 D-二聚體水平在術后隨時間發生了明顯變化。值得注意的是,盡管兩組患者在 Fib 和 D-二聚體的整體水平上沒有表現出顯著差異,但它們隨時間的變化模式卻呈現不同趨勢。術后,Fib 在對照組中呈上升趨勢,而在試驗組中則呈先下降后上升趨勢;D-二聚體在對照組中呈下降趨勢,而在試驗組中則呈先下降后上升趨勢。這些趨勢在術后第 1 天表現得尤為顯著,但到了術后第 3 天,差異性不再具有統計學意義。這一趨勢表明,多次靜脈使用 TXA 在術后初期對 Fib 和 D-二聚體的纖溶指標產生了影響,但這種影響在術后第 3 天逐漸減弱。這一發現意味著,多次靜脈使用 TXA 在術后初期對于纖溶指標具有顯著影響,更能夠有效地降低機體的纖溶水平,同上述文獻報道一致,解釋了多次靜脈使用 TXA 減少復合型髖臼骨折圍手術期總失血量方面的作用。
3.2 安全性評價
使用TXA實現止血效果的同時,是否會增加下肢深靜脈血栓形成的風險,其安全性一直備受關注。然而,多中心研究已經報道了在心臟外科、婦產科、骨科等不同領域的圍手術期中,通過靜脈滴注TXA的應用是安全有效的[27-28]。甚至在 VTE 高危患者中,TXA 的應用也被證明是安全有效的[29]。目前 TXA 在骨科各亞專業如關節外科、脊柱外科和創傷醫學中得到了廣泛應用,其應用方式包括口服、局部、靜脈及聯合應用等。一般而言,TXA 的應用時間主要集中在術后 24 h 以內,應用次數主要為術前單次,或者根據藥代動力學、藥物半衰期進行多次重復應用。TXA 的應用劑量多為 1~6 g。TXA 的相關臨床研究都涉及了其使用安全性的問題,且結果顯示 TXA 的應用并沒有明顯增加患者發生靜脈血栓栓塞等并發癥的風險[30-35]。本研究發現術后兩組患者的 DVT、IVT 發生率比較,差異均無統計學意義(P>0.05),這明確了多次靜脈使用 TXA 在復合型髖臼骨折圍手術期是安全的。
3.3 優點和不足
本研究發現復合型髖臼骨折圍手術期多次靜脈使用 TXA 可以有效地減少失血量,并且具有安全性。其原因為:① 采用前瞻性隨機對照研究設計,具備較高級別的證據水平;② 設計的納入標準和排除標準有助于減少選擇性偏倚的影響;③ 通過方程計算得出的血容量和失血量結果具有較高準確性和可靠性;④ 所有手術都由同一組醫師來完成,因此偏倚得以最小化。但本研究也存在一些不足:① 每個研究組只有 30 個樣本,樣本量較小,還需要后續更大樣本量的研究;② 不同的圍手術期輸液量可能會對總失血量產生一定的影響。
綜上所述,本研究發現對于復合型髖臼骨折圍手術期多次靜脈使用 TXA 有效減少患者總失血量、隱性失血量,減少圍手術期輸血率,且不增加靜脈血栓性疾病及手術并發癥的發生。因此,推薦復合型髖臼骨折術前 5~15 min 靜脈使用 2 g TXA,第 1 劑后 3、6 h 再次靜脈使用 1 g TXA。
利益沖突:所有作者聲明不存在利益沖突。
髖臼骨折通常由高能量的創傷引起,由于其解剖結構復雜并常伴有并發癥,因此致殘率及死亡率較高[1]。根據 Judet-Letournel 分型,髖臼骨折分為簡單骨折和復合型骨折[2-3];恢復髖臼與股骨頭匹配關系,切開復位內固定已經成為髖臼骨折的標準治療方法[4-5],但髖臼骨折圍手術期總失血量約 1 000 mL,通常需要輸血以糾正貧血[6-9],而且復合型骨折比簡單骨折創傷更大,機體纖溶亢進易導致患者更多的失血。因此,骨科創傷醫生需要采用各種干預措施來降低圍手術期失血量、減少輸血。氨甲環酸(tranexamic acid, TXA)是一種人工合成的賴氨酸衍生物,作為圍手術期常用的抗纖溶藥物,通過降低纖溶酶對止血纖維蛋白的溶解作用,從而減少圍手術期的失血,同時不會引起下肢深靜脈血栓形成。TXA 在骨科加速康復中使用極其廣泛,尤其在關節置換術中和術后的應用更發揮了突出作用;但在骨盆髖臼骨折中應用經驗尚顯不足[10]。關于 TXA 在髖臼骨折圍手術期使用的相關文獻報道少,對減少失血的有效性存在爭議,多次靜脈使用 TXA 的臨床研究尚無報道,面對復合型髖臼骨折創傷后血管內膜損傷和血液高凝狀態,靜脈滴注 TXA 形成靜脈血栓風險的安全性尚需進一步證實。本研究以在四川大學華西醫院骨科/創傷中心擬行復合型髖臼骨折切開復位內固定術患者為研究對象,對比圍手術期靜脈使用 TXA 不同方案,分析患者隱性失血量、總失血量、輸血率、靜脈血栓發生率結果,以評估多次靜脈滴注 TXA 是否可減少復合型髖臼骨折圍手術期失血,促進術后快速康復,以及其安全性和可能增加血栓事件的風險。
1 對象與方法
1.1 研究對象
選取 2021 年 9 月-2022 年 12 月四川大學華西醫院骨科/創傷中心骨盆髖臼組收治的擬行復合型髖臼骨折切開復位內固定術患者。納入標準:① 年齡 18~65 歲,受傷至入院時間≤14 d;② 術前血紅蛋白(hemoglobin, Hb)>90 g/L 或紅細胞壓積(hematocrit, Hct)>30%、血小板計數>50×109/L、凝血酶原時間<16 s、部分凝血酶原時間<47 s;③ 術前影像學檢查(X 線片及 CT 片)按照 Judet-Letournel 分型符合髖臼復合型骨折[2-3]。排除標準:① 血栓形成高危者,包括心房顫動、心臟起搏器和支架植入術后;② 既往有血栓病史或者雙下肢靜脈彩色多普勒超聲(彩超)提示有深靜脈血栓者;③ 既往曾對 TXA 過敏或使用禁忌者;④ 嚴重的肝腎功能不全者;⑤ 同時行髖臼骨折及其他部位手術者;⑥ 患有嚴重的血液類疾病,有出血性疾病或既往有出血性疾病病史,長期口服抗血小板、抗凝藥物者;⑦ 既往有患側髖部骨折、髖臼骨骼畸形、髖部手術者;⑧ 病理性骨折或有活動性感染(體表、肺部或泌尿系統)者。經四川大學華西醫院生物醫學倫理委員會審查[2019年審(1156)號],所有患者均簽署知情同意書。
本研究參考了 Spitler 等[11]關于髖臼骨折圍手術期失血量的研究結果估計所需的樣本量,采用了 GPower 3.1 軟件進行重復測量方差分析。在分析中,設定α=0.05 和檢驗效能為 0.8。根據這些參數計算得出研究至少需要 29 例。因此,本研究共需招募患者 60 例,每組各 30 例,以確保統計分析的有效性和結果的可靠性。
1.2 研究方法
1.2.1 分組
按照前瞻性雙盲隨機原則,將納入患者分為對照組和試驗組。具體方法:將患者從 1 ~ 60 編號,從隨機數字表 1~1 000 中任意一個數開始獲取 60 個隨機數字,每個患者沿同一方向順序獲取一個隨機數字;然后根據隨機數字大小排序,每 30 個數字一組,患者對應到相應的組別。在本研究中,一組研究人員和研究參與者只知道編號,不能預測研究參與者的具體入組情況,執行者為手術室及病房護理人員,病歷及臨床試驗數據管理系統由另一組研究人員進行記錄、資料收集及匯總工作。對照組:術前 10~15 min 靜脈滴注 TXA 2 g;試驗組:術前 10~15 min 靜脈滴注 TXA 2 g,在第 1 劑 TXA 靜脈滴注結束后第 3、6 小時各再次靜脈滴注 TXA 1 g。
1.2.2 手術方法
本研究所有手術均由同一組主任醫師獨立完成,患者使用全身麻醉,麻醉師控制性降壓,血壓保持在 90 / 60 mm Hg(1 mm Hg=0.133 kPa)的水平,手術中的肌松度滿意。
根據患者骨折情況選擇采用了改良的 stoppa+髂窩前方入路、Kocher-Langenbeck 后方入路(K-L 入路)和前后聯合入路的方法之一。① 改良的 stoppa+髂窩前方入路適用于除后壁、后柱骨折類型的其他髖臼復合型骨折。這種入路方式采用仰臥位,皮膚切口由臍部至恥骨聯合縱向連接中遠段約 8~10 cm,依序切開皮膚和皮下組織,顯露腹白線縱向切開,將腹直肌兩側拉開并保留止點,外推患側腹壁肌。在切開腹橫筋膜后,進入腹膜前間隙,向外側解剖,進入 Retzius 間隙,顯露結扎閉孔動靜脈與髂外或腹壁下動靜脈之間的交通支(即死亡冠血管),剝離暴露恥骨聯合至骶髂關節真性骨盆緣,顯露內側窗骨盆前環;髂窩前方入路從髂前上嵴沿髂嵴向后切開皮膚、皮下組織,緊貼髂骨內板骨膜下剝離至髂窩,顯露外側窗骨盆后環;骨折予以頂棒、骨盆復位螺釘、骨盆復位鉗等器械配合患肢牽引等方法復位,結合克氏針、螺釘等,鋼板塑形固定。C 臂透視骨折復位情況及內固定位置、長度,確定內固定物未進入髖臼。② K-L 入路適用于橫行伴后壁、后柱伴后壁等骨折,這種入路方式采用俯臥位,切開皮膚、皮下組織以及闊筋膜,鈍性分離臀大肌和臀中肌,部分切斷梨狀肌和短外旋肌群,顯露并保護坐骨神經。顯露髖臼后方,通過使用頂棒、骨盆復位螺釘、骨盆復位鉗等器械,直視下復位骨折端,然后鋼板塑形進行固定。通過 C 臂透視觀察骨折復位情況以及內固定的位置和長度,確保內固定物未進入髖臼。③ 單一入路骨折無法復位或固定滿意的類型采用前后聯合入路。
1.2.3 圍手術期處理方法
在本研究中,手術前后的抗凝措施遵循中國骨科大手術靜脈血栓栓塞癥預防指南[12],采用藥物聯合物理措施進行指導。術中輸血的決策是由麻醉醫師和手術醫師共同根據術中失血量及 Hb 檢查結果(術中血氣分析)來確定。術后輸血的指標是 Hb<70 g/L 或 Hct<25%[13-14]。所有患者術后均留置創腔負壓引流管,并在術后 48 h 內拔除。在創腔引流量增多、Hb 或 Hct 進行性下降的情況下,暫停抗凝治療,直至患者的 Hb 或 Hct 穩定[12]。出院前,對所有患者進行雙下肢血管超聲檢查,以確認是否有血栓形成。如果住院期間患者出現下肢腫脹并伴有疼痛,立即進行下肢血管超聲檢查,以了解下肢循環情況。肺栓塞的診斷則基于患者的臨床表現和胸部 CT 造影等檢查結果[15]。在術后康復過程中,根據內固定的穩定性決定患者是否可以坐起,并鼓勵其進行早期的股四頭肌功能鍛煉及踝泵鍛煉。此外,一旦雙下肢血管超聲檢查排除了血栓形成,采用氣壓泵對患者進行治療,以進一步預防血栓形成,促進其術后康復。
1.3 觀察指標
1.3.1 一般資料
患者性別、年齡、體質量指數、手術入路和手術時長。
1.3.2 有效性評價指標
患者的血容量、失血量、隱形失血量、輸血率。血容量根據 Nadler 方程[16]計算;記錄術前、術后第 1 天及第 3 天 Hb、Hct;總失血量根據 Gross 方程[17]計算;隱性失血量=(總失血量+輸血量)-(術中失血量+術后 48 h 內引流量);每組患者輸血率=(術中輸血患者例數+術后輸血患者例數)/每組總例數。
1.3.3 纖溶指標
術前、術后第 1 天及第 3 天的纖維蛋白原(fibrinogen, Fib)以及 D-二聚體。
1.3.4 安全性評價指標
靜脈血栓事件發生率:下肢靜脈彩超報告的靜脈血栓分深靜脈血栓(deep vein thrombosis, DVT)和肌間靜脈血栓(intramuscular vein thrombosis, IVT)兩類統計。
1.4 統計學方法
采用 SPSS 25.0軟件分析數據。正態分布的計量資料采用均數±標準差表示,組間比較采用獨立樣本 t 檢驗;非正態分布的計量資料采用中位數(下四分位數,上四分位數)表示,組間比較采用 Mann-Whitney 秩和檢驗;計數資料采用例數和/或百分比表示,組間比較采用χ2 檢驗。對于重復測量資料,如果滿足正態分布和方差齊性則采用重復測量方差分析(不符合 Mauchly 球形檢驗假設時采用 Greenhouse-Geisser 校正分析),否則采用 Kruskal-Wallis 非參數檢驗。雙側檢驗水準α=0.05。
2 結果
2.1 一般資料
共納入患者 60 例,每組各 30 例。所有患者均按計劃進行手術并完成相關指標檢查。兩組一般資料比較見表1。可見,兩組患者的性別、年齡、體質量指數、手術入路及手術時長比較,差異均無統計學意義(P>0.05)。
2.2 有效性評價
2.2.1 Hb 與 Hct
兩組患者的 Hb 和 Hct 變化趨勢見圖1。可見,術前,對照組和試驗組的 Hb[(114.93±16.35) vs.(116.20±17.92) g/L]、Hct[(34.90±4.98)% vs.(36.33±5.52)%]比較,差異均無統計學意義(P>0.05);術后第 1 天,對照組的 Hb[(93.33±16.29)g/L vs.(101.43±14.88)g/L]、Hct[(28.57±5.16)% vs.(31.70±4.40)%]均低于試驗組(P<0.05);術后第 3 天,對照組的 Hb[(88.60±17.04)g/L vs.(97.03±14.73)g/L]、Hct[(26.70±4.95)% vs.(29.73±4.02)%]均低于試驗組(P<0.05)。組內比較顯示,兩組患者術后第 1 天及術后第 3 天的 Hb 及 Hct 均較術前下降(P<0.05); 術后第 1 天與術后 第 3 天的 Hb 及 Hct 比較,差異均無統計學意義 (P>0.05)。兩組患者 Hb 及 Hct 值的重復測量方差分析不符合球形檢驗球對稱性(P<0.05),校正分析結果顯示,Hb 及 Hct 時間效應有統計學意義(F=88.485、106.426,P<0.001),組別效應無統計學意義(F=2.388、4.964,P=0.128、0.229),組別與時間不存在交互作用(F=2.547、2.531,P=0.087、0.117)。
 圖1
兩組患者的 Hb 和 Hct 變化趨勢(n=30)
圖1
兩組患者的 Hb 和 Hct 變化趨勢(n=30)
a. Hb;b. Hct
2.2.2 失血相關指標
兩組患者失血相關指標比較見表2。可見,除血容量、術中失血量外(P>0.05),兩組的術后 48 h 引流量、總失血量、隱形失血量和輸血率比較,差異均有統計學意義(P<0.05)。
2.3 纖溶指標
兩組患者的 Fib 和 D-二聚體變化趨勢見圖2。可見,術前,對照組和試驗組的 Fib[(4.40±1.81) vs.(5.11±1.61) g/L]、D-二聚體[(7.28±3.89)% vs.(5.69±2.81)%]比較,差異均無統計學意義(P>0.05);術后第 1 天,對照組的 Fib[(5.23±1.45) vs.(4.51±1.21) g/L]、D-二聚體[(6.16±3.42)% vs.(3.32±1.57)%]均高于試驗組(P<0.05);術后第 3 天,對照組和試驗組的 Fib[(5.85±1.85) vs.(6.07±1.20) g/L]、D-二聚體[(5.36±2.83)% vs.(4.15±2.06)%]比較,差異均無統計學意義(P>0.05)。組內比較顯示,對照組術后第 1 天的 Fib 較術前上升、D-二聚體較術前下降,試驗組術后第 1 天的 Fib 較術前下降,但差異均無統計學意義(P>0.05);與術前比較,試驗組術后第 1 天的 D-二聚體下降(P<0.05),兩組術后第 3 天的 Fib 均升高、D-二聚體均下降(P<0.05);試驗組術后第 3 天的 Fib 高于術后第 1 天(P<0.05);對照組術后第 1 天與術后第 3 天的 Fib 和 D-二聚體比較,試驗組術后第 1 天與術后第 3 天的 D-二聚體比較,差異均無統計學意義(P>0.05)。兩組患者 Fib 重復測量方差分析不符合球形檢驗球對稱性(P<0.05),進行校正分析結果顯示,時間效應有統計學意義(F=29.716,P<0.001),組別效應無統計學意義(F=0.041,P=0.841),組別與時間存在交互作用(F=12.227,P<0.001)。兩組患者 D-二聚體的重復測量方差分析符合球形檢驗球對稱性(P=0.244),分析結果顯示,時間效應有統計學意義(F=17.375,P<0.001),組別效應無統計學意義(F=3.154,P=0.081),組別與時間存在交互作用(F=8.933,P<0.001)。
 圖2
兩組患者的 Fib 和 D-二聚體變化趨勢(n=30)
圖2
兩組患者的 Fib 和 D-二聚體變化趨勢(n=30)
a. Fib;b. D-二聚體
2.4 安全性評價
兩組患者術后血栓發生率比較見表3。可見,患者術前下肢血管彩超中均未發現 DVT,兩組 IVT 發生率差異無統計學意義(P>0.05)。術后兩組的 DVT 及 IVT 發生率比較,差異均無統計學意義(P>0.05),且患者均未出現肺栓塞情況。
3 討論
復合型髖臼骨折的切開復位內固定術因髖部解剖結構的復雜性以及周圍豐富的血管網,導致圍手術期失血量多,輸血率高[6-9]。為了解決這一問題,通過采取血液稀釋、自體血回輸、圍手術期注射重組人促紅細胞生成素以及蔗糖鐵等方法被用于減少髖臼骨折圍手術期失血。盡管 Bigsby 等[18]表明自體血回輸相對輸注同種異體血具有一定成本效益,但實際治療費用仍較高;而重組人促紅細胞生成素、蔗糖鐵等方法的使用周期相對長、監測指標多等[19]。對于復合型髖臼骨折患者,找到一種更為經濟、方便、有效、安全的治療方法是骨科創傷醫生所面臨的挑戰。TXA 是一種傳統的抗纖溶藥物,在骨科加速康復專家共識中明確指出其是安全有效的[10,20],因此本研究將單次靜脈滴注 TXA 作為對照組,但并沒有設置未使用 TXA 作為空白對照組。Andersson 等 [21]對 TXA 藥代動力學研究發現,靜脈滴注 5~15 min 血藥濃度達到峰值,半衰期約為 3 h。Xie 等[22]研究發現機體纖溶亢進狀態于術后 6 h 達到峰值,并持續 18~24 h。因此,本研究根據 TXA 的半衰期及纖溶峰值時間,采用成熟的關節置換多次靜脈使用 TXA 方案設置試驗組用藥,于術前第 1 劑靜脈使用 2 g TXA 后 3 h 及 6 h 各追加 1 d TXA。目前尚無復合型髖臼骨折圍手術期多次靜脈使用 TXA 的有效性和安全性的研究報告,值得進一步深入研究。
3.1 有效性評價
TXA 通過競爭性阻斷纖溶酶原的賴氨酸位點,有效阻止纖溶酶的活化,從而抑制纖維蛋白凝塊的分解,發揮抗纖溶作用并產生止血效果。因此,TXA 主要適用于各類手術或創傷后因纖維蛋白過度溶解導致的出血問題,尤其在需要精確操作的復雜骨科手術中。TXA 的使用能有效減少圍手術期的失血,節約血液制品,減少異體輸血的潛在風險,同時降低了患者的住院費用。姚歡等[23]報道多次靜脈使用 TXA 可有效且安全地減少全髖關節置換圍手術期的隱性失血和 Hb 的丟失,特別是在術后 3、6 h 多次給藥的效果更為顯著。Maniar 等[24]研究表明,在全膝關節置換圍手術期至少使用 2 次 TXA 才能減少總失血量,多次使用的止血效果優于單次使用。本研究發現,兩組的 Hb 和 Hct 在術后呈現出下降趨勢,但兩組比較差異無統計學意義(P>0.05)。然而,相比于對照組,試驗組的 Hb 和 Hct 下降幅度相對較小。這一發現說明術后多次靜脈使用 TXA 可能在一定程度上減輕了 Hb 和 Hct 的下降。此外,兩組患者在術后 48 h 引流量、總失血量及隱性失血量方面的差異進一步支持了 TXA 在減少復合型髖臼骨折圍手術期失血方面的潛在效益。
隱性失血是評估術后失血的重要指標之一,因術后血液滲透至組織間隙、溶血作用以及氧化損傷紅細胞膜等因素導致,側面說明了術后機體的纖溶反應水平。有研究報道也支持 TXA 在減少全髖關節置換術圍手術期隱性失血方面的效用[25-26]。本研究通過 Nadler 公式計算患者血容量及 Gross 方程計算患者的總失血量,結合顯性失血量及輸血量計算出隱性失血量。最終結果顯示,試驗組中多次靜脈使用 TXA 可以有效地減少復合髖臼骨折圍手術期隱形失血量。在本研究中,患者的 Fib 和 D-二聚體水平在術后隨時間發生了明顯變化。值得注意的是,盡管兩組患者在 Fib 和 D-二聚體的整體水平上沒有表現出顯著差異,但它們隨時間的變化模式卻呈現不同趨勢。術后,Fib 在對照組中呈上升趨勢,而在試驗組中則呈先下降后上升趨勢;D-二聚體在對照組中呈下降趨勢,而在試驗組中則呈先下降后上升趨勢。這些趨勢在術后第 1 天表現得尤為顯著,但到了術后第 3 天,差異性不再具有統計學意義。這一趨勢表明,多次靜脈使用 TXA 在術后初期對 Fib 和 D-二聚體的纖溶指標產生了影響,但這種影響在術后第 3 天逐漸減弱。這一發現意味著,多次靜脈使用 TXA 在術后初期對于纖溶指標具有顯著影響,更能夠有效地降低機體的纖溶水平,同上述文獻報道一致,解釋了多次靜脈使用 TXA 減少復合型髖臼骨折圍手術期總失血量方面的作用。
3.2 安全性評價
使用TXA實現止血效果的同時,是否會增加下肢深靜脈血栓形成的風險,其安全性一直備受關注。然而,多中心研究已經報道了在心臟外科、婦產科、骨科等不同領域的圍手術期中,通過靜脈滴注TXA的應用是安全有效的[27-28]。甚至在 VTE 高危患者中,TXA 的應用也被證明是安全有效的[29]。目前 TXA 在骨科各亞專業如關節外科、脊柱外科和創傷醫學中得到了廣泛應用,其應用方式包括口服、局部、靜脈及聯合應用等。一般而言,TXA 的應用時間主要集中在術后 24 h 以內,應用次數主要為術前單次,或者根據藥代動力學、藥物半衰期進行多次重復應用。TXA 的應用劑量多為 1~6 g。TXA 的相關臨床研究都涉及了其使用安全性的問題,且結果顯示 TXA 的應用并沒有明顯增加患者發生靜脈血栓栓塞等并發癥的風險[30-35]。本研究發現術后兩組患者的 DVT、IVT 發生率比較,差異均無統計學意義(P>0.05),這明確了多次靜脈使用 TXA 在復合型髖臼骨折圍手術期是安全的。
3.3 優點和不足
本研究發現復合型髖臼骨折圍手術期多次靜脈使用 TXA 可以有效地減少失血量,并且具有安全性。其原因為:① 采用前瞻性隨機對照研究設計,具備較高級別的證據水平;② 設計的納入標準和排除標準有助于減少選擇性偏倚的影響;③ 通過方程計算得出的血容量和失血量結果具有較高準確性和可靠性;④ 所有手術都由同一組醫師來完成,因此偏倚得以最小化。但本研究也存在一些不足:① 每個研究組只有 30 個樣本,樣本量較小,還需要后續更大樣本量的研究;② 不同的圍手術期輸液量可能會對總失血量產生一定的影響。
綜上所述,本研究發現對于復合型髖臼骨折圍手術期多次靜脈使用 TXA 有效減少患者總失血量、隱性失血量,減少圍手術期輸血率,且不增加靜脈血栓性疾病及手術并發癥的發生。因此,推薦復合型髖臼骨折術前 5~15 min 靜脈使用 2 g TXA,第 1 劑后 3、6 h 再次靜脈使用 1 g TXA。
利益沖突:所有作者聲明不存在利益沖突。