引用本文: 徐心峰, 聞偉, 朱全, 陳亮. 右上肺跨亞段動脈分型的單中心回顧性研究. 中國胸心血管外科臨床雜志, 2023, 30(12): 1737-1742. doi: 10.7507/1007-4848.202306030 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
隨著低劑量CT(low-dose computed tomography,LDCT)技術的發展,肺癌被大量篩出。在肺癌高危人群中,LDCT篩查可使肺癌病死率下降約20%[1]。在非肺癌高危人群中,LDCT篩查仍可發現約2.1%的肺癌患者,其中,約95.5%的病灶表現為磨玻璃結節[2]。持續存在的磨玻璃結節被證實為低度惡性腫瘤[3],亞肺葉切除是此類病灶的首選治療方案[4-5]。直徑≤2 cm的早期肺癌中,肺段切除的預后價值已得到胸外科醫生的認可[6-8]。隨著肺段手術的進步及更高的肺功能保護需求[9-10],肺段手術開始由簡單肺段逐漸向復雜肺段手術過渡[11]。部分臨床研究[12-13]證實,亞段及次亞段切除安全性與肺段切除相似。因此,亞段及次亞段作為更深層次的解剖單位已進入胸外科醫生關注的領域[14]。
肺部腫瘤所在靶段是肺段切除的核心,而靶段段間平面是保證腫瘤安全切緣的重中之重[15]。亞段切除相較于肺段切除,其切除范圍更小,肺亞段平面判定應更為精確。目前,吲哚菁綠(indocyanine green,ICG)熒光顯影[16]及改良膨脹萎陷法[17]是最常用的段間平面判斷方案,但其依賴于動脈判斷的準確性,意外損傷、遺漏或錯斷動脈分支將導致切除靶段平面的成像變化,從而影響手術切緣及預后[18]。因此,術中亞段動脈及其分支的準確辨識對肺亞段的精準切除及預后具有極為關鍵的作用。本研究基于右上肺支氣管分型,分析右上肺肺段內、肺段間跨亞段動脈的發生比例,并進一步細化跨亞段動脈類型,以提高肺亞段手術的精準性。
1 資料與方法
1.1 臨床資料
收集2021年1月—2022年6月于南京醫科大學第一附屬醫院胸外科行右上肺肺動脈CT血管造影(CT angiography,CTA)患者的影像學資料,對其肺亞段支氣管及亞段動脈分型進行分析。納入標準:(1)患者性別、年齡、手術方式不限,臨床資料完整;(2)完成我院肺動脈CTA檢查,縱隔窗、肺窗層厚為1 mm;(3)肺動脈CTA數據需進行三維CT 支氣管血管成像(3D computed tomography bronchography and angiography,3D-CTBA)重建;(4)3D-CTBA需完整展示右上肺亞段支氣管及相應動靜脈。排除標準:CTA數據發現右上肺存在炎癥、肺不張、偽影、較大病灶等,導致3D-CTBA無法清晰顯示右上肺解剖結構。
1.2 肺動脈CTA檢查方法
肺動脈CTA檢查使用64排螺旋CT,高壓注射器注入40~60 mL非離子型對比劑,隨后追加20 mL生理鹽水,用團注追蹤法設定掃描開始的時間。掃描時準直器厚度為0.6 mm或0.625 mm,掃描后重建的軸位圖像層厚為1 mm,重建的卷積核算法為軟組織算法,層間距為0.8~1.0 mm,重建后圖像載入Deepinsight軟件進行3D-CTBA重建[19]。3D-CTBA需要完整展示右上肺亞段支氣管及相應動靜脈。患者1 mm薄層CT肺窗用于對比分析右上肺亞段及以下解剖結構。
1.3 肺段、亞段及亞段以下解剖結構命名
支氣管分級中,肺葉支氣管為Ⅰ級,肺段支氣管為Ⅱ級,亞段支氣管為Ⅲ級,次亞段支氣管為Ⅳ級,依次類推。支氣管命名依據肺段、亞段及次亞段等支氣管在肺葉、肺段及亞段內分布范圍進行定義,其中,第一優先級為上、下關系,第二級關系為后、前關系,第三級優先級為外、內關系。支氣管以B命名,肺段支氣管以阿拉伯數字右上標表示,亞段支氣管以小寫英文字母表示,緊隨亞段支氣管小寫英文字母后的小寫羅馬數字表示次亞段支氣管,例如B1ai為次亞段命名[20]。因B1缺失后,B1a與B1b分別異位于B2、B3,出現二分支B1a+B2;B1b+B3分型,在解剖研究中易出現統計分歧,本研究中排除此類變異支氣管分型[21-22]。
肺段、亞段、次亞段動脈與伴行支氣管命名規則相同,均以A表示,肺段動脈以阿拉伯數字右上標表示,亞段動脈以小寫英文字母表示,次亞段動脈使用小寫羅馬數字表示,如A1ai為次亞段動脈命名。本研究中跨亞段動脈為次亞段及以下結構,統一使用t(trans-subsegmental artery)表示,如A1at。
1.4 跨亞段動脈的相關定義
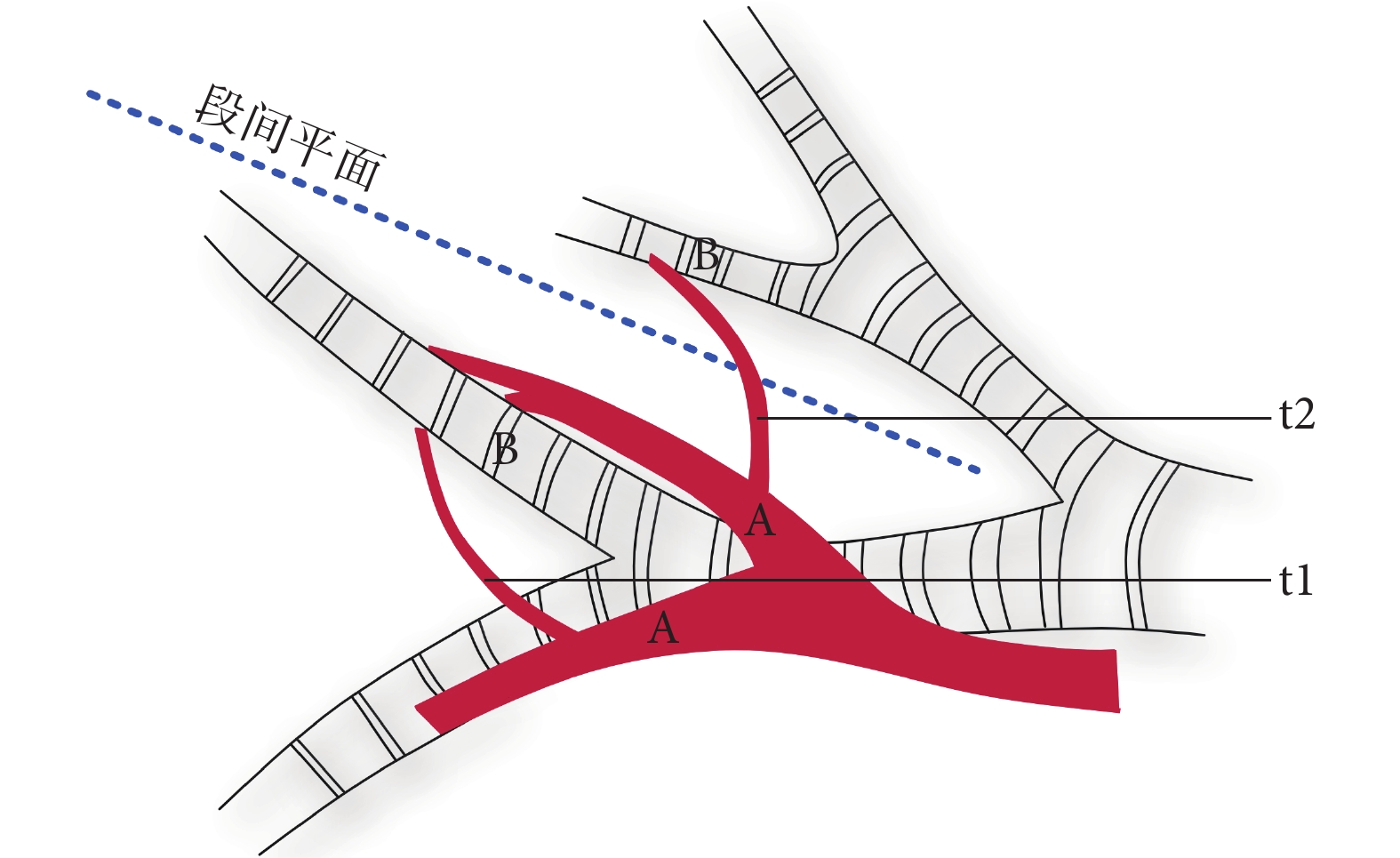
跨亞段動脈定義為肺段、亞段動脈與對應支氣管伴行中,發出的分布于鄰近亞段的次亞段動脈及細小分支。如圖1所示,在亞段動脈A伴行亞段支氣管B走行途中,發出鄰近亞段區域的動脈為跨亞段動脈,因t1出現在肺段內,則為肺段內的跨亞段動脈(t1),當跨亞段動脈穿越段間平面進入鄰近肺段范圍時,則為肺段間的跨亞段動脈分支(t2)。
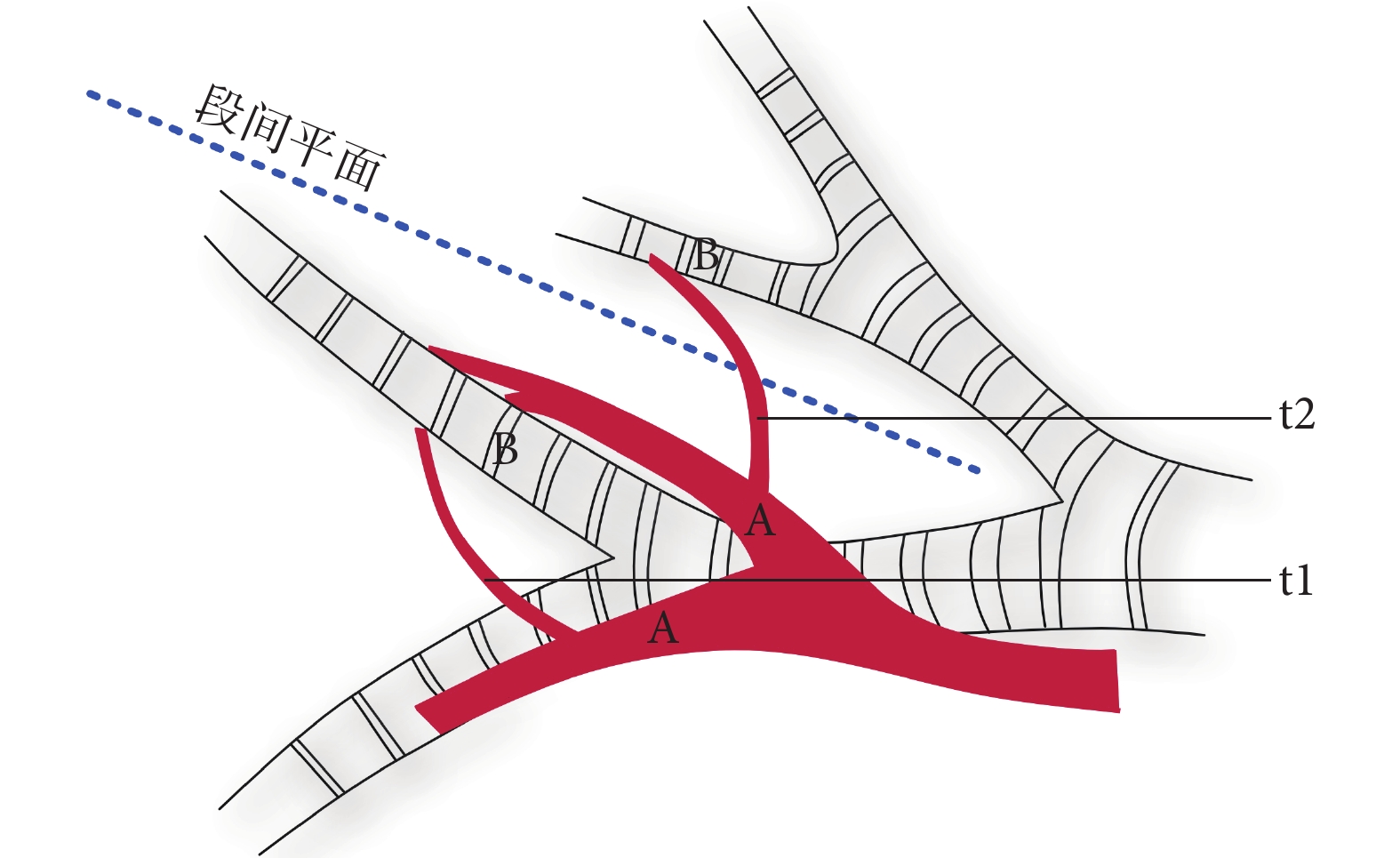 圖1
跨亞段動脈示意圖
圖1
跨亞段動脈示意圖
t:跨亞段動脈;A:亞段動脈;B:亞段支氣管;t1:肺段內的跨亞段動脈分支;t2:肺段間的跨亞段動脈分支
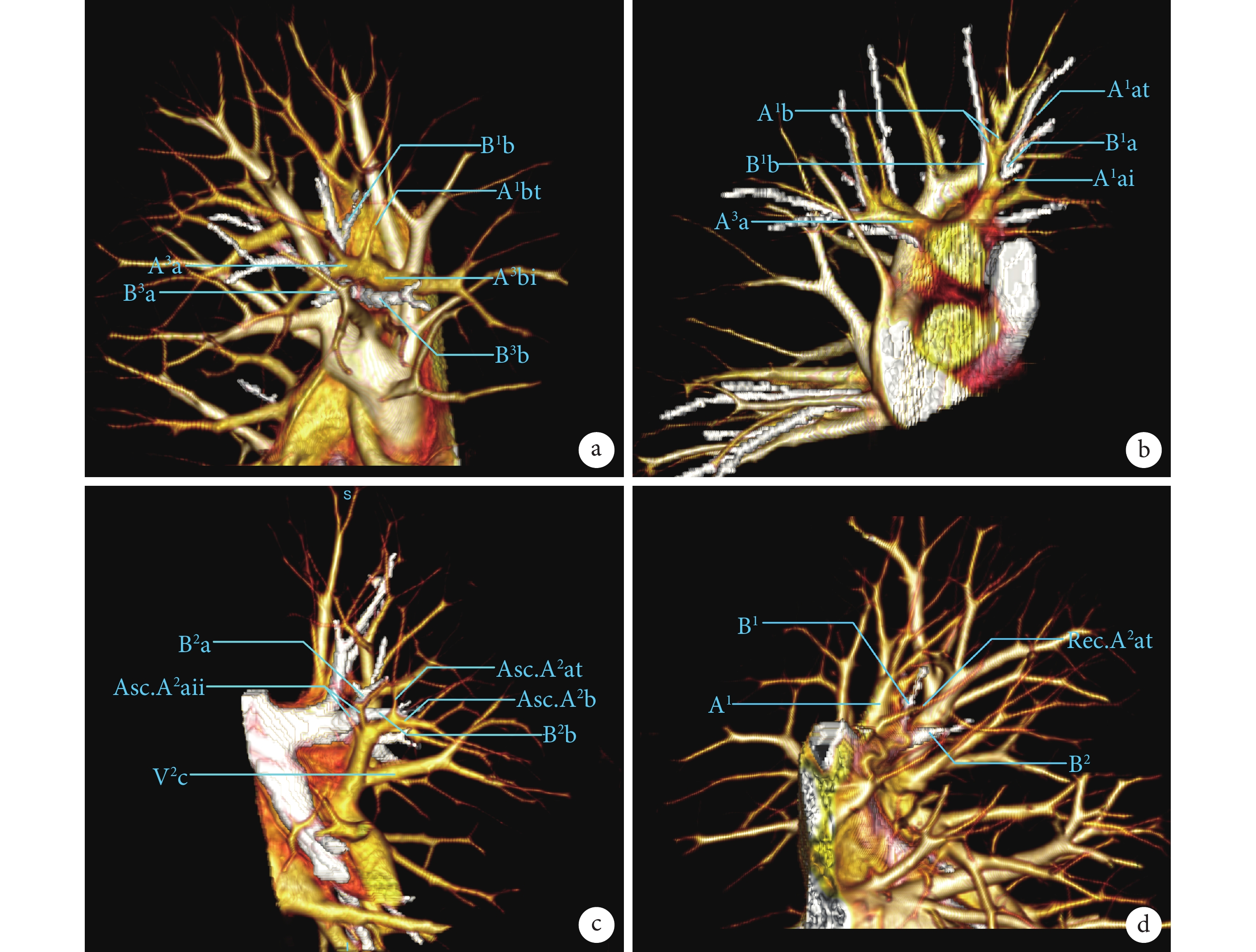
圖2展示3D-CTBA肺段內與肺段間的跨亞段動脈。圖2a顯示在前段動脈伴行支氣管走行時,發出進入S1b區域,出現S1與S3段間跨亞段動脈A1bt;A3a與次亞段動脈A3bi共干,A3bi視為S3肺段內的跨亞段動脈。圖2b顯示S1肺段內跨亞段動脈,A1b與B1b伴行途中發出進入S1a區域內的跨亞段動脈A1at。圖2c顯示S2肺段內的跨亞段動脈,Asc.A2b伴B2b走行途中,發出進入S2a區域內跨亞段動脈Asc.A2at。圖2d為S1與S2肺段間跨亞段動脈,在A1伴B1走行途中發出進入S2a的跨亞段動脈Rec.A2at。
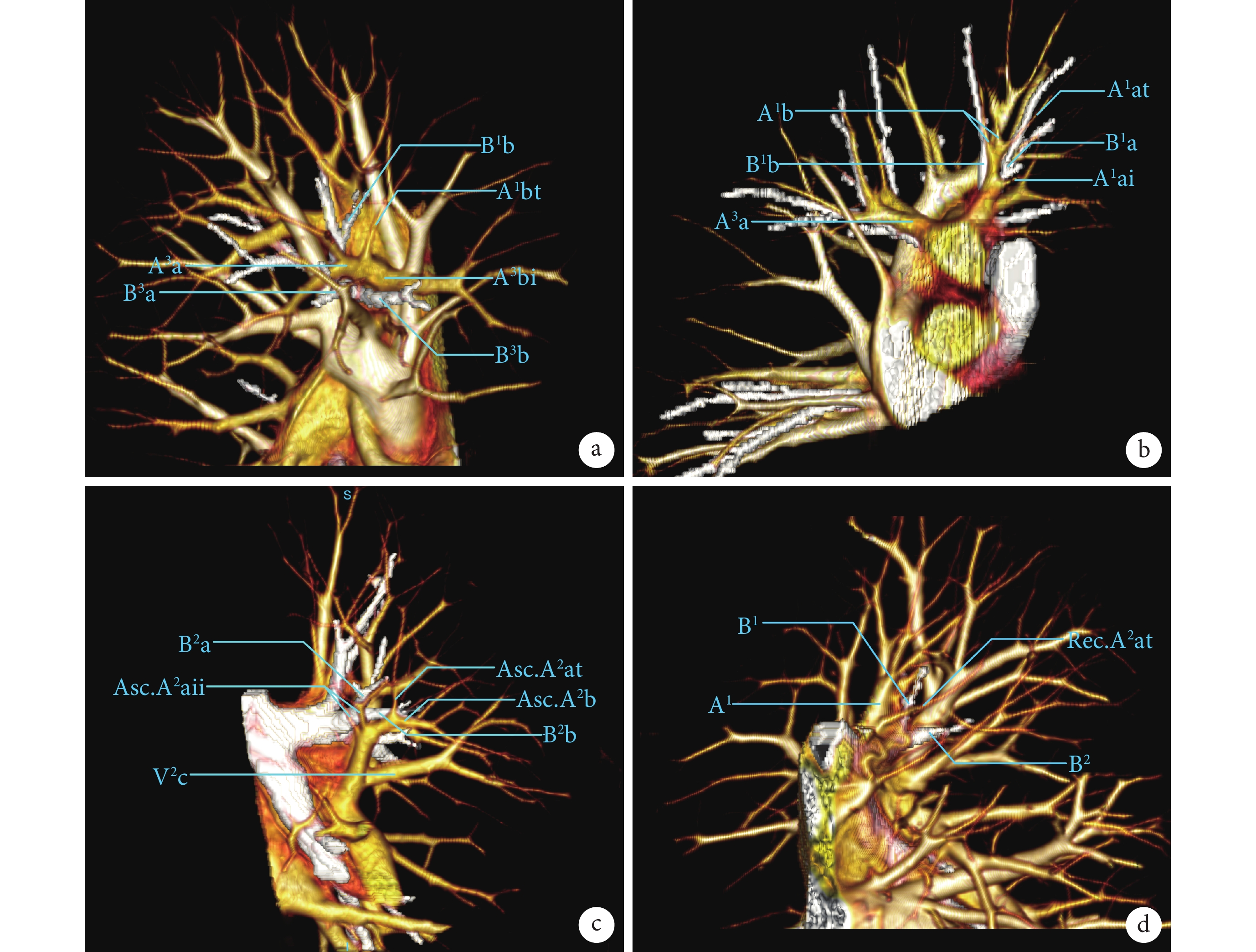 圖2
三維CT支氣管血管成像顯示右上肺亞段間動脈混雜分支
圖2
三維CT支氣管血管成像顯示右上肺亞段間動脈混雜分支
a:S1與S3段間跨亞段動脈A1bt,S3肺段內跨亞段動脈A3bi;b:S1肺段內跨亞段動脈A1at;c:S2肺段內的跨亞段動脈Asc.A2at;d:S1與S2肺段間跨亞段動脈Rec.A2at
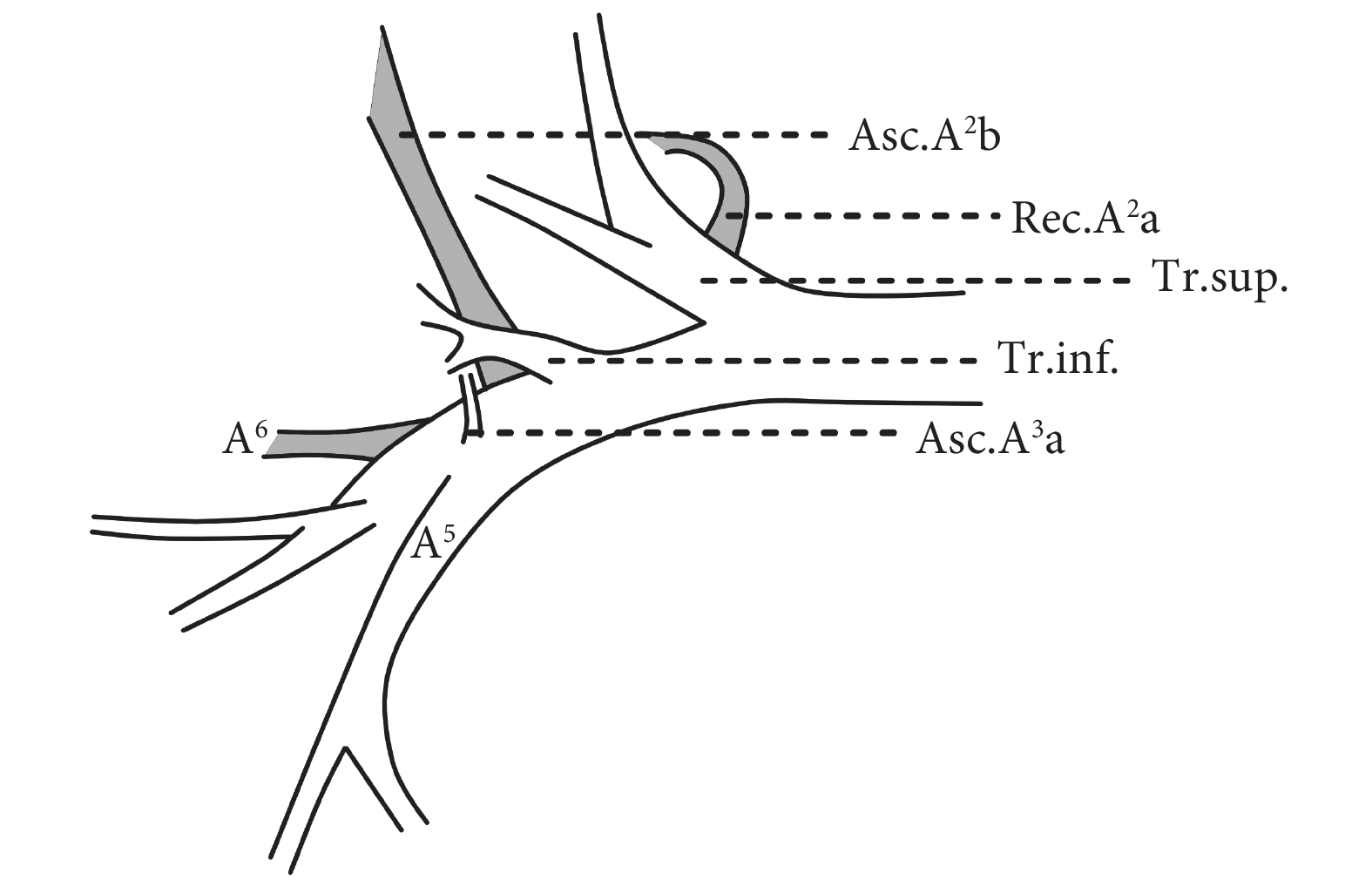
上干支動脈(trunk superior,Tr.sup.)為右肺動脈發出的第一分支,常發出S1的A1a、A1b及后段返支動脈(Rec.A2)。下干支動脈(trunk inferior,Tr.inf.)為右肺動脈發出的第二分支,發自右肺動脈主干,分布于中肺動脈與上干支動脈之間,常發出S3相關動脈,如A3及A3b等。升支動脈(ascending artery,Asc.A)發自右肺動脈的葉間部分,常發出S2及S3相關動脈,如Asc.A2b及Asc.A3a等。返支動脈(recurrent artery,Rec.A)發自上干支動脈或下干支動脈向后方走行穿行進入S2的動脈,如Rec.A2a等。圖3示右上肺動脈常見分支。因上干支動脈存在大量肺段、亞段、次亞段動脈,為減少跨亞段動脈分型,本研究僅收錄遠端支氣管伴行分支,在上干支動脈根部的共干血管,不納入跨亞段動脈分型研究。
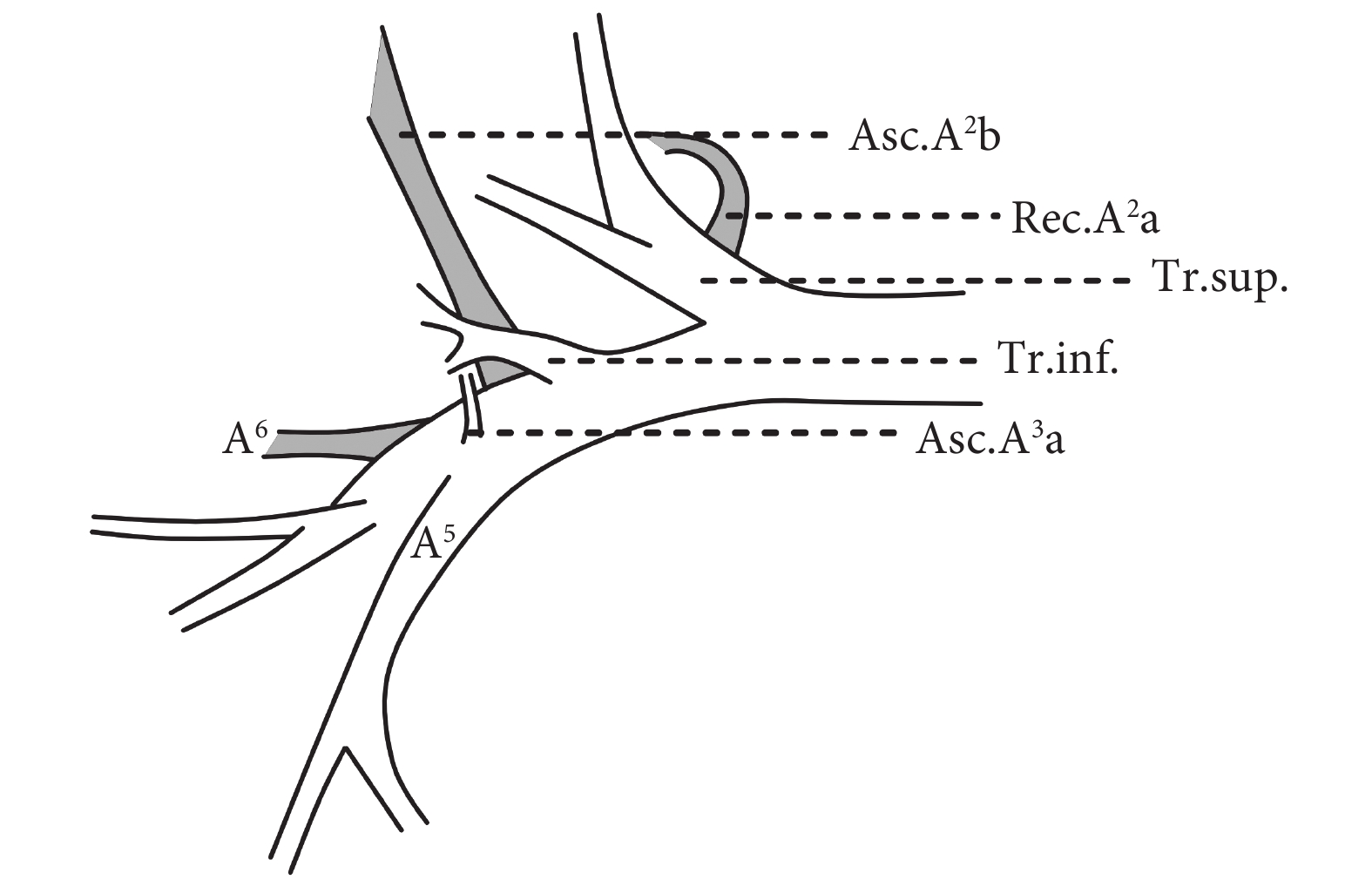 圖3
右上肺動脈命名
圖3
右上肺動脈命名
Tr.sup.:上干支動脈,右肺動脈發出的第一分支;Tr.inf.:下干支動脈,右肺動脈發出的第二分支;Asc.A2b、Asc.A3a:升支動脈,緊鄰右中肺動脈A5、A6;Rec.A2b:后段返支動脈;A5:右中肺內側段動脈;A6:右下肺上段動脈
1.5 統計學分析
統計分析軟件使用SPSS(version 23.0,SPSS Inc.,Chicago,IL)。正態分布的計量資料以均數±標準差( ±s)描述。計數資料采用例數(%)描述,組間比較采用χ2檢驗或Fisher確切概率法。P≤0.05為差異有統計學意義。
±s)描述。計數資料采用例數(%)描述,組間比較采用χ2檢驗或Fisher確切概率法。P≤0.05為差異有統計學意義。
1.6 倫理審查
本研究已通過南京醫科大學第一附屬醫院倫理委員會審批,倫理審批號:2021-SR-164。
2 結果
納入患者111例,其中男36例、女75例,平均年齡(61.83±8.91)歲。
表1顯示肺段內跨亞段動脈數量及動脈類型。右上肺跨亞段動脈共有29種類型,僅出現1次的類型比例為45%(13/29)。S1內52%(58/111)患者出現肺段內跨亞段動脈,其中發自上干支動脈的A1b+A1at類型比例高達67%(39/58)。S2內41%(45/111)患者出現肺段內跨亞段內動脈,發自后升支動脈的Asc.A2b+Asc.A2at類型較多,占53%(24/45),其次為發自上干支動脈的Rec.A2a+Rec.A2bt類型,占27%(12/45)。S3內32%(36/111)患者出現跨亞段動脈,發自上干支動脈A3b+A3at類型最多,比例為47%(17/36)。
表2顯示肺段間跨亞段動脈數量及動脈類型。在S1與S2肺段間,24%(27/111)的患者出現跨亞段動脈,最常見的類型為發自上干支動脈的A1+Rec.A2at,約為30%(8/27);Rec.A2+A1at及Rec.A2a+A1at比例均為22%(6/27)。S2與S3肺段間,僅5%(5/111)患者出現跨亞段動脈,主要為Rec.A2分支與A3分支之間的共干。S1與S3肺段間,僅8%(9/111)出現跨亞段動脈,主要為A3a與A1b動脈分支共干。
表3顯示右上肺不同支氣管分型對于肺段內、肺段間跨亞段動脈的影響。在111例患者中,右上肺支氣管分型共4種,分別為B1;B2;B3型、B1;B2+3型、B1+2;B3型、B1;B2+3型,其中,最常見的分型為B1;B2;B3型,占42%(47/111);其次為B1+2;B3型,占32%(35/111)。我們對不同支氣管分型肺段內及肺段間跨亞段動脈發生比例進行比較,結果發現,4種支氣管分型在S1、S2及S3肺段內出現跨亞段動脈比例差異均無統計學意義(P=0.590,0.868,0.399);在S1與S2、S2與S3及S1與S3肺段間,4種支氣管分型出現跨亞段動脈比例差異亦無統計學意義(P=0.294,0.879,0.821)。表明右上肺支氣管分型未影響跨亞段動脈的發生比例。
3 討論
LDCT篩查發現的早期肺癌具有病灶小(直徑≤2 cm)、多含有磨玻璃成分等特點,此類病灶多為低度惡性腫瘤[2],優選手術方案為肺段或肺亞段切除。但肺段及亞段動脈存在大量跨亞段動脈,分支細小且復雜。本研究明確了跨亞段動脈的定義,并分析在右上肺肺段內、肺段間的分布,進一步精細化肺段或亞段手術。
以往研究中,Boyden等[23]在肺段解剖關于穿越段間平面的動脈中,記錄A1、A2和A3部分分支的關系,但無詳細具體動脈構成。其中A1b分支發自A3比例約10%,A3分支發自A1b比例約8%。A3和A2分支共干比例達30%。Yamashita[24]在亞段解剖中使用了“混雜分支”作為部分亞段及次亞段動脈命名不清的代名詞。本研究在明確跨亞段動脈概念基礎上,對其進一步細分,并分析支氣管分型對于跨亞段動脈的影響。
S1內跨亞段動脈比例為52%,S2內比例為41%,S3內比例為32%。伴隨著跨亞段動脈的出現,亞段間的關系更為緊密,S1內跨亞段動脈比例最高,S1a亞段與S1b亞段相互關聯,單亞段切除難度相對較大。在單亞段切除中,Kato等[25]報道6例S1內單亞段切除。本研究顯示肺段間跨亞段動脈比例最高出現在S1與S2之間,比例為25%,且S1內及S2內均有較高比例的肺段內跨亞段動脈。因此,針對S1、S2內單亞段及聯合亞段的常見手術方式[9,26-27],術中極易出現跨亞段動脈的損傷、誤斷或漏斷。在S2與S3之間跨亞段動脈Rec.A2bt多出現于上干支,同時上干支存在大量肺段內跨亞段動脈,S3相關手術容易出現意外損傷。
切緣是肺部腫瘤預后的重要影響因素[28-30]。在肺段或亞段切除中,靶段平面的顯示是保證切緣距離的重要環節。在近期JCOG0802研究[8]中,肺段切除組出現了5例切緣陽性患者,原因可能為肺段切除組無術前3D-CTBA的精細解剖展示及切緣模擬。3D-CTBA對于動脈的清晰展示是動脈依賴型段間平面顯示方法的必要條件。ICG熒光顯影[16]及改良膨脹萎陷法[17]均依賴肺段動脈。跨亞段動脈可與肺段動脈或肺亞段動脈共干,肺段切除、亞段切除均可能誤斷跨亞段動脈,導致靶段平面顯示向外擴展增加切緣。但鄰近亞段會因此出現氣血比例失調,進而加重肺功能損失[14]。由于跨亞段動脈不依據支氣管分型出現變化,相對固定發生。在肺段切除或亞段切除中,同樣可能漏斷跨亞段動脈,從而導致靶段段間平面顯示縮小,最終減少切緣范圍,影響患者腫瘤學療效[31-32]。
本研究為回顧性單中心研究,納入的樣本量相對較少,樣本收集時間跨度窄,且僅分析了右上肺解剖,結果及結論存在一定偏倚。跨亞段動脈為次亞段及以下結構,由于解剖的復雜性和次亞段命名的爭議,本研究未對次亞段動脈進行充分命名,降低了部分手術的指導意義。
綜上,右上肺跨亞段動脈發生比例高,類型多樣。肺段切除、肺亞段切除是極為個性化的手術過程。
利益沖突:無。
作者貢獻:徐心峰負責數據收集和論文撰寫;聞偉、朱全負責數據審核;陳亮負責寫作指導和論文審閱。
隨著低劑量CT(low-dose computed tomography,LDCT)技術的發展,肺癌被大量篩出。在肺癌高危人群中,LDCT篩查可使肺癌病死率下降約20%[1]。在非肺癌高危人群中,LDCT篩查仍可發現約2.1%的肺癌患者,其中,約95.5%的病灶表現為磨玻璃結節[2]。持續存在的磨玻璃結節被證實為低度惡性腫瘤[3],亞肺葉切除是此類病灶的首選治療方案[4-5]。直徑≤2 cm的早期肺癌中,肺段切除的預后價值已得到胸外科醫生的認可[6-8]。隨著肺段手術的進步及更高的肺功能保護需求[9-10],肺段手術開始由簡單肺段逐漸向復雜肺段手術過渡[11]。部分臨床研究[12-13]證實,亞段及次亞段切除安全性與肺段切除相似。因此,亞段及次亞段作為更深層次的解剖單位已進入胸外科醫生關注的領域[14]。
肺部腫瘤所在靶段是肺段切除的核心,而靶段段間平面是保證腫瘤安全切緣的重中之重[15]。亞段切除相較于肺段切除,其切除范圍更小,肺亞段平面判定應更為精確。目前,吲哚菁綠(indocyanine green,ICG)熒光顯影[16]及改良膨脹萎陷法[17]是最常用的段間平面判斷方案,但其依賴于動脈判斷的準確性,意外損傷、遺漏或錯斷動脈分支將導致切除靶段平面的成像變化,從而影響手術切緣及預后[18]。因此,術中亞段動脈及其分支的準確辨識對肺亞段的精準切除及預后具有極為關鍵的作用。本研究基于右上肺支氣管分型,分析右上肺肺段內、肺段間跨亞段動脈的發生比例,并進一步細化跨亞段動脈類型,以提高肺亞段手術的精準性。
1 資料與方法
1.1 臨床資料
收集2021年1月—2022年6月于南京醫科大學第一附屬醫院胸外科行右上肺肺動脈CT血管造影(CT angiography,CTA)患者的影像學資料,對其肺亞段支氣管及亞段動脈分型進行分析。納入標準:(1)患者性別、年齡、手術方式不限,臨床資料完整;(2)完成我院肺動脈CTA檢查,縱隔窗、肺窗層厚為1 mm;(3)肺動脈CTA數據需進行三維CT 支氣管血管成像(3D computed tomography bronchography and angiography,3D-CTBA)重建;(4)3D-CTBA需完整展示右上肺亞段支氣管及相應動靜脈。排除標準:CTA數據發現右上肺存在炎癥、肺不張、偽影、較大病灶等,導致3D-CTBA無法清晰顯示右上肺解剖結構。
1.2 肺動脈CTA檢查方法
肺動脈CTA檢查使用64排螺旋CT,高壓注射器注入40~60 mL非離子型對比劑,隨后追加20 mL生理鹽水,用團注追蹤法設定掃描開始的時間。掃描時準直器厚度為0.6 mm或0.625 mm,掃描后重建的軸位圖像層厚為1 mm,重建的卷積核算法為軟組織算法,層間距為0.8~1.0 mm,重建后圖像載入Deepinsight軟件進行3D-CTBA重建[19]。3D-CTBA需要完整展示右上肺亞段支氣管及相應動靜脈。患者1 mm薄層CT肺窗用于對比分析右上肺亞段及以下解剖結構。
1.3 肺段、亞段及亞段以下解剖結構命名
支氣管分級中,肺葉支氣管為Ⅰ級,肺段支氣管為Ⅱ級,亞段支氣管為Ⅲ級,次亞段支氣管為Ⅳ級,依次類推。支氣管命名依據肺段、亞段及次亞段等支氣管在肺葉、肺段及亞段內分布范圍進行定義,其中,第一優先級為上、下關系,第二級關系為后、前關系,第三級優先級為外、內關系。支氣管以B命名,肺段支氣管以阿拉伯數字右上標表示,亞段支氣管以小寫英文字母表示,緊隨亞段支氣管小寫英文字母后的小寫羅馬數字表示次亞段支氣管,例如B1ai為次亞段命名[20]。因B1缺失后,B1a與B1b分別異位于B2、B3,出現二分支B1a+B2;B1b+B3分型,在解剖研究中易出現統計分歧,本研究中排除此類變異支氣管分型[21-22]。
肺段、亞段、次亞段動脈與伴行支氣管命名規則相同,均以A表示,肺段動脈以阿拉伯數字右上標表示,亞段動脈以小寫英文字母表示,次亞段動脈使用小寫羅馬數字表示,如A1ai為次亞段動脈命名。本研究中跨亞段動脈為次亞段及以下結構,統一使用t(trans-subsegmental artery)表示,如A1at。
1.4 跨亞段動脈的相關定義
跨亞段動脈定義為肺段、亞段動脈與對應支氣管伴行中,發出的分布于鄰近亞段的次亞段動脈及細小分支。如圖1所示,在亞段動脈A伴行亞段支氣管B走行途中,發出鄰近亞段區域的動脈為跨亞段動脈,因t1出現在肺段內,則為肺段內的跨亞段動脈(t1),當跨亞段動脈穿越段間平面進入鄰近肺段范圍時,則為肺段間的跨亞段動脈分支(t2)。
 圖1
跨亞段動脈示意圖
圖1
跨亞段動脈示意圖
t:跨亞段動脈;A:亞段動脈;B:亞段支氣管;t1:肺段內的跨亞段動脈分支;t2:肺段間的跨亞段動脈分支
圖2展示3D-CTBA肺段內與肺段間的跨亞段動脈。圖2a顯示在前段動脈伴行支氣管走行時,發出進入S1b區域,出現S1與S3段間跨亞段動脈A1bt;A3a與次亞段動脈A3bi共干,A3bi視為S3肺段內的跨亞段動脈。圖2b顯示S1肺段內跨亞段動脈,A1b與B1b伴行途中發出進入S1a區域內的跨亞段動脈A1at。圖2c顯示S2肺段內的跨亞段動脈,Asc.A2b伴B2b走行途中,發出進入S2a區域內跨亞段動脈Asc.A2at。圖2d為S1與S2肺段間跨亞段動脈,在A1伴B1走行途中發出進入S2a的跨亞段動脈Rec.A2at。
 圖2
三維CT支氣管血管成像顯示右上肺亞段間動脈混雜分支
圖2
三維CT支氣管血管成像顯示右上肺亞段間動脈混雜分支
a:S1與S3段間跨亞段動脈A1bt,S3肺段內跨亞段動脈A3bi;b:S1肺段內跨亞段動脈A1at;c:S2肺段內的跨亞段動脈Asc.A2at;d:S1與S2肺段間跨亞段動脈Rec.A2at
上干支動脈(trunk superior,Tr.sup.)為右肺動脈發出的第一分支,常發出S1的A1a、A1b及后段返支動脈(Rec.A2)。下干支動脈(trunk inferior,Tr.inf.)為右肺動脈發出的第二分支,發自右肺動脈主干,分布于中肺動脈與上干支動脈之間,常發出S3相關動脈,如A3及A3b等。升支動脈(ascending artery,Asc.A)發自右肺動脈的葉間部分,常發出S2及S3相關動脈,如Asc.A2b及Asc.A3a等。返支動脈(recurrent artery,Rec.A)發自上干支動脈或下干支動脈向后方走行穿行進入S2的動脈,如Rec.A2a等。圖3示右上肺動脈常見分支。因上干支動脈存在大量肺段、亞段、次亞段動脈,為減少跨亞段動脈分型,本研究僅收錄遠端支氣管伴行分支,在上干支動脈根部的共干血管,不納入跨亞段動脈分型研究。
 圖3
右上肺動脈命名
圖3
右上肺動脈命名
Tr.sup.:上干支動脈,右肺動脈發出的第一分支;Tr.inf.:下干支動脈,右肺動脈發出的第二分支;Asc.A2b、Asc.A3a:升支動脈,緊鄰右中肺動脈A5、A6;Rec.A2b:后段返支動脈;A5:右中肺內側段動脈;A6:右下肺上段動脈
1.5 統計學分析
統計分析軟件使用SPSS(version 23.0,SPSS Inc.,Chicago,IL)。正態分布的計量資料以均數±標準差( ±s)描述。計數資料采用例數(%)描述,組間比較采用χ2檢驗或Fisher確切概率法。P≤0.05為差異有統計學意義。
±s)描述。計數資料采用例數(%)描述,組間比較采用χ2檢驗或Fisher確切概率法。P≤0.05為差異有統計學意義。
1.6 倫理審查
本研究已通過南京醫科大學第一附屬醫院倫理委員會審批,倫理審批號:2021-SR-164。
2 結果
納入患者111例,其中男36例、女75例,平均年齡(61.83±8.91)歲。
表1顯示肺段內跨亞段動脈數量及動脈類型。右上肺跨亞段動脈共有29種類型,僅出現1次的類型比例為45%(13/29)。S1內52%(58/111)患者出現肺段內跨亞段動脈,其中發自上干支動脈的A1b+A1at類型比例高達67%(39/58)。S2內41%(45/111)患者出現肺段內跨亞段內動脈,發自后升支動脈的Asc.A2b+Asc.A2at類型較多,占53%(24/45),其次為發自上干支動脈的Rec.A2a+Rec.A2bt類型,占27%(12/45)。S3內32%(36/111)患者出現跨亞段動脈,發自上干支動脈A3b+A3at類型最多,比例為47%(17/36)。
表2顯示肺段間跨亞段動脈數量及動脈類型。在S1與S2肺段間,24%(27/111)的患者出現跨亞段動脈,最常見的類型為發自上干支動脈的A1+Rec.A2at,約為30%(8/27);Rec.A2+A1at及Rec.A2a+A1at比例均為22%(6/27)。S2與S3肺段間,僅5%(5/111)患者出現跨亞段動脈,主要為Rec.A2分支與A3分支之間的共干。S1與S3肺段間,僅8%(9/111)出現跨亞段動脈,主要為A3a與A1b動脈分支共干。
表3顯示右上肺不同支氣管分型對于肺段內、肺段間跨亞段動脈的影響。在111例患者中,右上肺支氣管分型共4種,分別為B1;B2;B3型、B1;B2+3型、B1+2;B3型、B1;B2+3型,其中,最常見的分型為B1;B2;B3型,占42%(47/111);其次為B1+2;B3型,占32%(35/111)。我們對不同支氣管分型肺段內及肺段間跨亞段動脈發生比例進行比較,結果發現,4種支氣管分型在S1、S2及S3肺段內出現跨亞段動脈比例差異均無統計學意義(P=0.590,0.868,0.399);在S1與S2、S2與S3及S1與S3肺段間,4種支氣管分型出現跨亞段動脈比例差異亦無統計學意義(P=0.294,0.879,0.821)。表明右上肺支氣管分型未影響跨亞段動脈的發生比例。
3 討論
LDCT篩查發現的早期肺癌具有病灶小(直徑≤2 cm)、多含有磨玻璃成分等特點,此類病灶多為低度惡性腫瘤[2],優選手術方案為肺段或肺亞段切除。但肺段及亞段動脈存在大量跨亞段動脈,分支細小且復雜。本研究明確了跨亞段動脈的定義,并分析在右上肺肺段內、肺段間的分布,進一步精細化肺段或亞段手術。
以往研究中,Boyden等[23]在肺段解剖關于穿越段間平面的動脈中,記錄A1、A2和A3部分分支的關系,但無詳細具體動脈構成。其中A1b分支發自A3比例約10%,A3分支發自A1b比例約8%。A3和A2分支共干比例達30%。Yamashita[24]在亞段解剖中使用了“混雜分支”作為部分亞段及次亞段動脈命名不清的代名詞。本研究在明確跨亞段動脈概念基礎上,對其進一步細分,并分析支氣管分型對于跨亞段動脈的影響。
S1內跨亞段動脈比例為52%,S2內比例為41%,S3內比例為32%。伴隨著跨亞段動脈的出現,亞段間的關系更為緊密,S1內跨亞段動脈比例最高,S1a亞段與S1b亞段相互關聯,單亞段切除難度相對較大。在單亞段切除中,Kato等[25]報道6例S1內單亞段切除。本研究顯示肺段間跨亞段動脈比例最高出現在S1與S2之間,比例為25%,且S1內及S2內均有較高比例的肺段內跨亞段動脈。因此,針對S1、S2內單亞段及聯合亞段的常見手術方式[9,26-27],術中極易出現跨亞段動脈的損傷、誤斷或漏斷。在S2與S3之間跨亞段動脈Rec.A2bt多出現于上干支,同時上干支存在大量肺段內跨亞段動脈,S3相關手術容易出現意外損傷。
切緣是肺部腫瘤預后的重要影響因素[28-30]。在肺段或亞段切除中,靶段平面的顯示是保證切緣距離的重要環節。在近期JCOG0802研究[8]中,肺段切除組出現了5例切緣陽性患者,原因可能為肺段切除組無術前3D-CTBA的精細解剖展示及切緣模擬。3D-CTBA對于動脈的清晰展示是動脈依賴型段間平面顯示方法的必要條件。ICG熒光顯影[16]及改良膨脹萎陷法[17]均依賴肺段動脈。跨亞段動脈可與肺段動脈或肺亞段動脈共干,肺段切除、亞段切除均可能誤斷跨亞段動脈,導致靶段平面顯示向外擴展增加切緣。但鄰近亞段會因此出現氣血比例失調,進而加重肺功能損失[14]。由于跨亞段動脈不依據支氣管分型出現變化,相對固定發生。在肺段切除或亞段切除中,同樣可能漏斷跨亞段動脈,從而導致靶段段間平面顯示縮小,最終減少切緣范圍,影響患者腫瘤學療效[31-32]。
本研究為回顧性單中心研究,納入的樣本量相對較少,樣本收集時間跨度窄,且僅分析了右上肺解剖,結果及結論存在一定偏倚。跨亞段動脈為次亞段及以下結構,由于解剖的復雜性和次亞段命名的爭議,本研究未對次亞段動脈進行充分命名,降低了部分手術的指導意義。
綜上,右上肺跨亞段動脈發生比例高,類型多樣。肺段切除、肺亞段切除是極為個性化的手術過程。
利益沖突:無。
作者貢獻:徐心峰負責數據收集和論文撰寫;聞偉、朱全負責數據審核;陳亮負責寫作指導和論文審閱。