隨著腔內治療技術的發展,胸主動脈腔內修復術(thoracic endovascular aortic repair,TEVAR)的應用已擴展到主動脈弓疾病。對于需要將錨定區延長到Z1區的病例,需要同時重建左頸總動脈(left common carotid artery,LCCA)及左鎖骨下動脈(left subclavian artery,LSA),仍是主動脈弓部病變腔內治療需要面對的困難。本中心近期在5例需要行Z1區錨定的主動脈弓部病變中,采用了Castor單分支支架聯合平行支架技術進行了全腔內修復,取得良好臨床效果,現報道如下。
1 資料與方法
1.1 臨床資料
回顧性分析2022年4月—2022年8月中國科學技術大學附屬第一醫院心臟大血管外科收治的采用單分支支架聯合平行支架技術進行Z1區錨定,全腔內修復治療的主動脈弓部疾病患者的臨床資料。納入標準:(1)均經計算機斷層掃描血管造影(computed tomographic angiography,CTA)確診為主動脈弓部病變需行LCCA和LSA重建:包括主動脈夾層(aortic dissection,AD)和胸主動脈瘤;(2)主體近端錨定區直徑<40 mm;(3)夾層原發破口或主動脈瘤體前緣距離LCCA開口后緣小于15 mm;(4)病變遠離主動脈弓大彎側;(5)LCCA及LSA近端直徑6~12 mm。排除標準:(1)結締組織病;(2)主動脈Z0區、Z1區血管病變;(3)髂、股動脈入路重度扭曲,直徑<7 mm;(4)有需要手術處理的心臟瓣膜病變;(5)有凝血功能障礙、出血、造影劑過敏病史。
1.2 術前評估
術前將CTA檢查DICOM文件導入Endosize工作站(Therenva SAS, Rennes, France)進行三維重建。評估病變位置、大小、形態、累及范圍等。主要測量數據包括病變與 LSA開口遠端 的距離(L1,病變位于Z3區為正值,位于Z2區為負值),病變與LCCA開口遠端距離(L2),LCCA開口遠端與LSA開口近端距離(L3),近遠端錨定區降主動脈真腔直徑、LSA開口直徑、LCCA開口直徑、LCCA開口近端與無名動脈開口遠端距離。根據測量結果確定所選用Castor分支支架(上海微創公司)型號(近端錨定區oversize夾層為5%~10%,動脈瘤為15%~20%;遠端錨定區oversize為0%~20%;分支oversize為0%~20%),根據LCCA開口直徑選擇平行支架(oversize為0%~20%)。分支支架分支后移距離(L4)根據測量結果選擇,要求覆蓋LCCA,不影響無名動脈開口,且錨定區長度(D)>20 mm(表1)。
1.3 手術過程
所有患者均行全身麻醉,仰臥位,頭略偏向右側,暴露左側頸部。除1例主動脈夾層患者因過于肥胖切開暴露左側頸總動脈外,其余患者皆穿刺左側頸總動脈,置入6F鞘。切開暴露右側股總動脈,穿刺左側肱動脈及左側股總動脈。按照我們前期報道的方法進行Castor分支支架植入[1]。肝素化后將造影導管置入升主動脈造影,確認病變與術前診斷符合。經左側肱動脈入路建立左側肱動脈與右側股動脈之間軌道后,將多功能導管從左側肱動脈置入,經主動脈真腔,由右側股總動脈穿出。Lunderquist超硬導絲經右側股總動脈及主動脈真腔進入升主動脈作為主體支架支撐導絲;造影導管經左側股總動脈進入主動脈真腔,用于術中造影。加硬導絲經過左頸總動脈置入升主動脈,根據病變位置確定加硬導絲位于主動脈弓的前壁或后壁,經加硬導絲將Luminexx裸支架(美國巴德公司)由LCCA置入主動脈弓。分支導絲經多功能導管由左側肱動脈穿出,主體支架由超硬導絲導引進入降主動脈,確認分支導絲與主體支架無纏繞,將分支拉入LSA,主體支架前端錨定于無名動脈與LCCA之間,造影確認位置無誤,順序釋放主體支架及分支支架。Castor支架釋放完畢后,確認平行支架前段超出主體支架前端約1 cm,釋放左頸總動脈內的平行支架。再次造影證實支架位置、重建弓上分支及內漏情況,撤出輸送系統及導絲導管。縫合手術切口并按壓穿刺點止血后于雜交手術室復蘇,拔除氣管插管,返回普通病房。術后阿司匹林、氯吡格雷雙抗治療半年后,改為阿司匹林長期口服。
1.4 觀察指標
觀察指標主要有手術成功率,住院時間,圍手術期和隨訪期間并發癥發生率、分支支架和平行支架通暢率。術后1、6、12個月門診隨訪,復查主動脈CTA。
1.5 倫理審查
本研究已通過中國科學技術大學第一附屬醫院(安徽省立醫院)倫理委員會審查,批準號為2023-RE-270。
2 結果
2.1 患者一般資料
本研究納入2022年5月—2022年8月中國科學技術大學附屬第一醫院心臟大血管外科應用Castor單分支支架聯合平行支架技術治療需Z1區錨定的5例主動脈弓病變患者臨床資料。其中男4例、女1例,年齡24~71(46.2±18.6)歲。有高血壓病史3例,糖尿病史1例,冠心病史1例。急性非A非B型主動脈夾層4例,1列夾層患者原發破口位于Z3區,血腫逆撕至Z2區,3例夾層患者原發破口均位于Z2區;主動脈弓動脈瘤1例,病變累及Z2區。5例病變與LCCA開口遠端距離均<15 mm;見表1。
2.2 術中術后情況
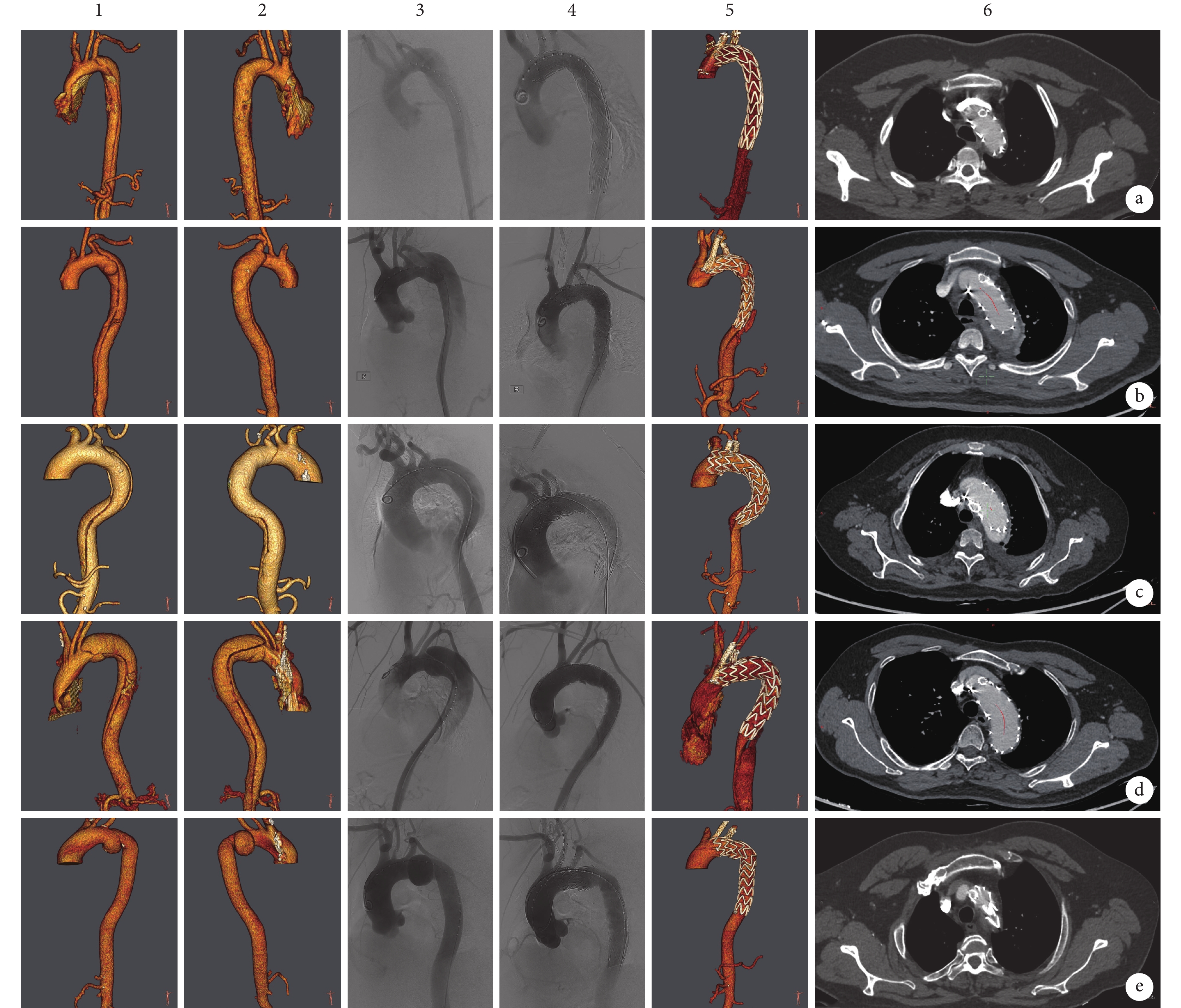
5例患者手術均成功。病變與左頸總動脈開口遠端距離(L2)為(9.4±3.5)mm,主體支架前緣與分支距離(L4)為(24.2±6.5)mm,錨定區長度(D)為(28.4±5.0)mm。平行支架直徑(9.2±1.2) mm,長度(49.7±11.5)mm。術中造影Castor分支支架定位精確,病變隔絕滿意,未見明顯Ⅰa型內漏,平行支架位置形態良好,造影LCCA及LSA通暢,無狹窄(圖1)。手術時間為125~196(132.3±45.1)min。圍術期未發生死亡、腦梗死、腎功能不全、上肢缺血及外周并發癥,均順利出院,術后平均住院時間(7.2±2.5)d。術后隨訪12~15個月,隨訪期間均無明顯胸痛、上肢缺血癥狀及神經系統癥狀,未進行再次手術。隨訪CTA顯示支架形態良好,無明顯移位,夾層患者未見明顯近端內漏,主動脈弓降部真腔明顯增大,假腔明顯減少,假腔內血栓化滿意;動脈瘤患者瘤體隔絕滿意,瘤腔內完全血栓化。LCCA及LSA血流通暢,分支及平行支架未見折斷、狹窄、閉塞、移位(圖1)。
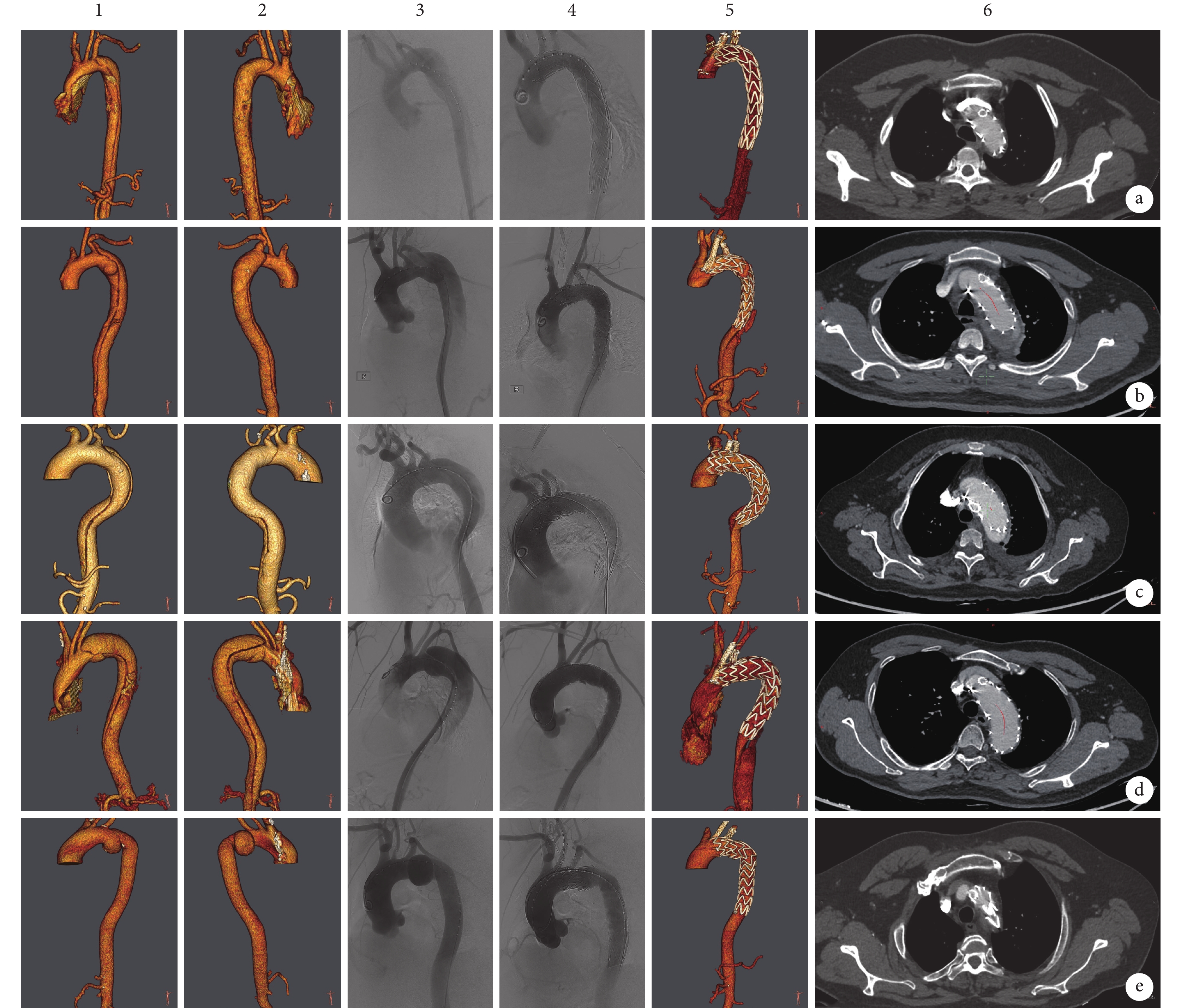 圖1
患者術前、術中、術后影像資料
圖1
患者術前、術中、術后影像資料
a~d:急性非A非B型主動脈夾層病例;e:主動脈弓部瘤病例;1~2:病變術前三維重建;3:術中支架植入前病變造影;4:術中支架植入后造影;5:術后1年CT血管造影復查三維重建;6:術后1年復查分支支架通暢情況
3 討論
主動脈弓部病變的治療對心臟外科和血管外科醫生來說仍是一個挑戰。體外循環與深低溫停循環技術支持下的傳統開放手術能夠在直視下完全切除主動脈弓病灶并重建受累弓上分支,療效確切,仍然是治療主動脈弓病變的標準術式,但該術式手術創傷大,并發癥發生率和死亡率較高[2]。與傳統的開放手術相比,TEVAR的圍手術期發病率和死亡率顯著降低[3-4]。然而,由于主動脈弓的解剖彎曲、弓上分支的存在、血流動力學以及心臟收縮和呼吸周期的特性,TEVAR治療主動脈弓部病變技術要求較高,仍然只能在少數經驗豐富的中心開展[5]。足夠的近端錨定區對于TEVAR治療的療效至關重要,一般認為近端錨定區應≥20 mm。只有覆蓋弓上分支方能獲得足夠的近端錨定區以實現主動脈弓部病變的TEVAR治療,因此弓上分支的重建對于主動脈弓部病變的TEVAR治療至關重要。重建LSA以延長近端錨定區到Z2區的技術已經比較成熟。如果將錨定區延長到Z1區,則必須通過重建LCCA以及LSA方能實現。雜交手術是進行弓上雙分支外科重建以延長錨定區的經典手術,方法為經頸部切口進行右側頸總動脈至LCCA的轉流以及進行LCCA到LSA的轉流,或開胸進行升主動脈到LCCA和LSA的轉流。雖然比傳統的開放手術創傷小,但相比于全腔內技術,雜交手術仍有相關手術并發癥[6]。隨著腔內技術的進步,平行支架技術、開窗技術及分支支架技術逐漸應用于弓上兩分支的全腔內重建,以延長錨定區到Z1區。平行支架技術相對簡單、對耗材要求低,但由于支架間縫隙的存在,平行支架所致的Ⅰa型內漏較難避免。對于Z1區病變,應用單個平行支架的內漏發生率明顯低于應用兩個平行支架[7]。開窗技術包括體外開窗技術與原位開窗技術。在體外開窗中,由于主動脈弓的彎曲,將開窗的移植物與弓上多個分支的開口對齊更加困難和危險[8-9]。原位開窗學習曲線長,需要特殊耗材,并可能增加腦缺血的風險[10-11]。此外開窗技術破壞了支架的完整性,其長期的耐久性和穩定性仍有待于進一步的驗證。相比于平行支架技術和開窗技術,分支支架技術因更符合正常解剖結構及血流狀態,因此一直被認為是弓上分支重建的未來解決方案[12]。Castor支架是目前國內唯一上市的分支支架產品,臨床應用最多,但是該支架僅被設計應用于左鎖骨下動脈的重建。目前有結合開窗技術應用該產品進行弓上多分支重建的報道,但開窗破壞了分支支架的結構,屬于超適應癥使用,遠期效果有待于進一步驗證且存在倫理風險[13-14]。聯合應用Castor分支支架和平行支架技術可以在不破壞支架完整性的情況下充分延長近端錨定區至Z1區,本組病例平均近端錨定區達到了28.4 mm,從而為避免Ⅰa型內漏和逆撕等嚴重并發癥,提供了堅實的技術基礎。我們僅在左頸總動脈重建中應用單個平行支架,較之多平行支架技術重建弓上分支,降低了內漏的發生率。應避免將該技術應用于主動脈弓大彎側病變,對于病變位于主動脈側壁的病變,將平行支架置于病變對側,避免了內漏的發生,本組病例中未發生Ⅰa型內漏。主動脈弓部過多操作可能導致卒中或血管壁損傷[15-16]。相比于雜交手術、多平行支架技術、多分支支架技術以及原位開窗技術、該技術較為簡單,無需在弓部做額外的操作,也無需中斷弓上分支血流,減少了腦部并發癥的風險,本組病例未發生嚴重腦部并發癥。
本研究結果表明,對于Z1區TEVAR,聯合應用Castor分支支架和平行支架技術操作簡單、安全有效,短中期效果滿意,為主動脈弓疾病提供了有價值的治療選擇。本研究為單中心回顧性研究,樣本例數較少,仍需進一步積累經驗,擴大樣本量,增加隨訪時間,以進一步驗證上述結論。
利益沖突:無。
作者貢獻:孔祥負責研究設計,論文撰寫;阮鵬、余繼全負責資料收集,數據統計;孔祥、葛建軍負責論文指導。
隨著腔內治療技術的發展,胸主動脈腔內修復術(thoracic endovascular aortic repair,TEVAR)的應用已擴展到主動脈弓疾病。對于需要將錨定區延長到Z1區的病例,需要同時重建左頸總動脈(left common carotid artery,LCCA)及左鎖骨下動脈(left subclavian artery,LSA),仍是主動脈弓部病變腔內治療需要面對的困難。本中心近期在5例需要行Z1區錨定的主動脈弓部病變中,采用了Castor單分支支架聯合平行支架技術進行了全腔內修復,取得良好臨床效果,現報道如下。
1 資料與方法
1.1 臨床資料
回顧性分析2022年4月—2022年8月中國科學技術大學附屬第一醫院心臟大血管外科收治的采用單分支支架聯合平行支架技術進行Z1區錨定,全腔內修復治療的主動脈弓部疾病患者的臨床資料。納入標準:(1)均經計算機斷層掃描血管造影(computed tomographic angiography,CTA)確診為主動脈弓部病變需行LCCA和LSA重建:包括主動脈夾層(aortic dissection,AD)和胸主動脈瘤;(2)主體近端錨定區直徑<40 mm;(3)夾層原發破口或主動脈瘤體前緣距離LCCA開口后緣小于15 mm;(4)病變遠離主動脈弓大彎側;(5)LCCA及LSA近端直徑6~12 mm。排除標準:(1)結締組織病;(2)主動脈Z0區、Z1區血管病變;(3)髂、股動脈入路重度扭曲,直徑<7 mm;(4)有需要手術處理的心臟瓣膜病變;(5)有凝血功能障礙、出血、造影劑過敏病史。
1.2 術前評估
術前將CTA檢查DICOM文件導入Endosize工作站(Therenva SAS, Rennes, France)進行三維重建。評估病變位置、大小、形態、累及范圍等。主要測量數據包括病變與 LSA開口遠端 的距離(L1,病變位于Z3區為正值,位于Z2區為負值),病變與LCCA開口遠端距離(L2),LCCA開口遠端與LSA開口近端距離(L3),近遠端錨定區降主動脈真腔直徑、LSA開口直徑、LCCA開口直徑、LCCA開口近端與無名動脈開口遠端距離。根據測量結果確定所選用Castor分支支架(上海微創公司)型號(近端錨定區oversize夾層為5%~10%,動脈瘤為15%~20%;遠端錨定區oversize為0%~20%;分支oversize為0%~20%),根據LCCA開口直徑選擇平行支架(oversize為0%~20%)。分支支架分支后移距離(L4)根據測量結果選擇,要求覆蓋LCCA,不影響無名動脈開口,且錨定區長度(D)>20 mm(表1)。
1.3 手術過程
所有患者均行全身麻醉,仰臥位,頭略偏向右側,暴露左側頸部。除1例主動脈夾層患者因過于肥胖切開暴露左側頸總動脈外,其余患者皆穿刺左側頸總動脈,置入6F鞘。切開暴露右側股總動脈,穿刺左側肱動脈及左側股總動脈。按照我們前期報道的方法進行Castor分支支架植入[1]。肝素化后將造影導管置入升主動脈造影,確認病變與術前診斷符合。經左側肱動脈入路建立左側肱動脈與右側股動脈之間軌道后,將多功能導管從左側肱動脈置入,經主動脈真腔,由右側股總動脈穿出。Lunderquist超硬導絲經右側股總動脈及主動脈真腔進入升主動脈作為主體支架支撐導絲;造影導管經左側股總動脈進入主動脈真腔,用于術中造影。加硬導絲經過左頸總動脈置入升主動脈,根據病變位置確定加硬導絲位于主動脈弓的前壁或后壁,經加硬導絲將Luminexx裸支架(美國巴德公司)由LCCA置入主動脈弓。分支導絲經多功能導管由左側肱動脈穿出,主體支架由超硬導絲導引進入降主動脈,確認分支導絲與主體支架無纏繞,將分支拉入LSA,主體支架前端錨定于無名動脈與LCCA之間,造影確認位置無誤,順序釋放主體支架及分支支架。Castor支架釋放完畢后,確認平行支架前段超出主體支架前端約1 cm,釋放左頸總動脈內的平行支架。再次造影證實支架位置、重建弓上分支及內漏情況,撤出輸送系統及導絲導管。縫合手術切口并按壓穿刺點止血后于雜交手術室復蘇,拔除氣管插管,返回普通病房。術后阿司匹林、氯吡格雷雙抗治療半年后,改為阿司匹林長期口服。
1.4 觀察指標
觀察指標主要有手術成功率,住院時間,圍手術期和隨訪期間并發癥發生率、分支支架和平行支架通暢率。術后1、6、12個月門診隨訪,復查主動脈CTA。
1.5 倫理審查
本研究已通過中國科學技術大學第一附屬醫院(安徽省立醫院)倫理委員會審查,批準號為2023-RE-270。
2 結果
2.1 患者一般資料
本研究納入2022年5月—2022年8月中國科學技術大學附屬第一醫院心臟大血管外科應用Castor單分支支架聯合平行支架技術治療需Z1區錨定的5例主動脈弓病變患者臨床資料。其中男4例、女1例,年齡24~71(46.2±18.6)歲。有高血壓病史3例,糖尿病史1例,冠心病史1例。急性非A非B型主動脈夾層4例,1列夾層患者原發破口位于Z3區,血腫逆撕至Z2區,3例夾層患者原發破口均位于Z2區;主動脈弓動脈瘤1例,病變累及Z2區。5例病變與LCCA開口遠端距離均<15 mm;見表1。
2.2 術中術后情況
5例患者手術均成功。病變與左頸總動脈開口遠端距離(L2)為(9.4±3.5)mm,主體支架前緣與分支距離(L4)為(24.2±6.5)mm,錨定區長度(D)為(28.4±5.0)mm。平行支架直徑(9.2±1.2) mm,長度(49.7±11.5)mm。術中造影Castor分支支架定位精確,病變隔絕滿意,未見明顯Ⅰa型內漏,平行支架位置形態良好,造影LCCA及LSA通暢,無狹窄(圖1)。手術時間為125~196(132.3±45.1)min。圍術期未發生死亡、腦梗死、腎功能不全、上肢缺血及外周并發癥,均順利出院,術后平均住院時間(7.2±2.5)d。術后隨訪12~15個月,隨訪期間均無明顯胸痛、上肢缺血癥狀及神經系統癥狀,未進行再次手術。隨訪CTA顯示支架形態良好,無明顯移位,夾層患者未見明顯近端內漏,主動脈弓降部真腔明顯增大,假腔明顯減少,假腔內血栓化滿意;動脈瘤患者瘤體隔絕滿意,瘤腔內完全血栓化。LCCA及LSA血流通暢,分支及平行支架未見折斷、狹窄、閉塞、移位(圖1)。
 圖1
患者術前、術中、術后影像資料
圖1
患者術前、術中、術后影像資料
a~d:急性非A非B型主動脈夾層病例;e:主動脈弓部瘤病例;1~2:病變術前三維重建;3:術中支架植入前病變造影;4:術中支架植入后造影;5:術后1年CT血管造影復查三維重建;6:術后1年復查分支支架通暢情況
3 討論
主動脈弓部病變的治療對心臟外科和血管外科醫生來說仍是一個挑戰。體外循環與深低溫停循環技術支持下的傳統開放手術能夠在直視下完全切除主動脈弓病灶并重建受累弓上分支,療效確切,仍然是治療主動脈弓病變的標準術式,但該術式手術創傷大,并發癥發生率和死亡率較高[2]。與傳統的開放手術相比,TEVAR的圍手術期發病率和死亡率顯著降低[3-4]。然而,由于主動脈弓的解剖彎曲、弓上分支的存在、血流動力學以及心臟收縮和呼吸周期的特性,TEVAR治療主動脈弓部病變技術要求較高,仍然只能在少數經驗豐富的中心開展[5]。足夠的近端錨定區對于TEVAR治療的療效至關重要,一般認為近端錨定區應≥20 mm。只有覆蓋弓上分支方能獲得足夠的近端錨定區以實現主動脈弓部病變的TEVAR治療,因此弓上分支的重建對于主動脈弓部病變的TEVAR治療至關重要。重建LSA以延長近端錨定區到Z2區的技術已經比較成熟。如果將錨定區延長到Z1區,則必須通過重建LCCA以及LSA方能實現。雜交手術是進行弓上雙分支外科重建以延長錨定區的經典手術,方法為經頸部切口進行右側頸總動脈至LCCA的轉流以及進行LCCA到LSA的轉流,或開胸進行升主動脈到LCCA和LSA的轉流。雖然比傳統的開放手術創傷小,但相比于全腔內技術,雜交手術仍有相關手術并發癥[6]。隨著腔內技術的進步,平行支架技術、開窗技術及分支支架技術逐漸應用于弓上兩分支的全腔內重建,以延長錨定區到Z1區。平行支架技術相對簡單、對耗材要求低,但由于支架間縫隙的存在,平行支架所致的Ⅰa型內漏較難避免。對于Z1區病變,應用單個平行支架的內漏發生率明顯低于應用兩個平行支架[7]。開窗技術包括體外開窗技術與原位開窗技術。在體外開窗中,由于主動脈弓的彎曲,將開窗的移植物與弓上多個分支的開口對齊更加困難和危險[8-9]。原位開窗學習曲線長,需要特殊耗材,并可能增加腦缺血的風險[10-11]。此外開窗技術破壞了支架的完整性,其長期的耐久性和穩定性仍有待于進一步的驗證。相比于平行支架技術和開窗技術,分支支架技術因更符合正常解剖結構及血流狀態,因此一直被認為是弓上分支重建的未來解決方案[12]。Castor支架是目前國內唯一上市的分支支架產品,臨床應用最多,但是該支架僅被設計應用于左鎖骨下動脈的重建。目前有結合開窗技術應用該產品進行弓上多分支重建的報道,但開窗破壞了分支支架的結構,屬于超適應癥使用,遠期效果有待于進一步驗證且存在倫理風險[13-14]。聯合應用Castor分支支架和平行支架技術可以在不破壞支架完整性的情況下充分延長近端錨定區至Z1區,本組病例平均近端錨定區達到了28.4 mm,從而為避免Ⅰa型內漏和逆撕等嚴重并發癥,提供了堅實的技術基礎。我們僅在左頸總動脈重建中應用單個平行支架,較之多平行支架技術重建弓上分支,降低了內漏的發生率。應避免將該技術應用于主動脈弓大彎側病變,對于病變位于主動脈側壁的病變,將平行支架置于病變對側,避免了內漏的發生,本組病例中未發生Ⅰa型內漏。主動脈弓部過多操作可能導致卒中或血管壁損傷[15-16]。相比于雜交手術、多平行支架技術、多分支支架技術以及原位開窗技術、該技術較為簡單,無需在弓部做額外的操作,也無需中斷弓上分支血流,減少了腦部并發癥的風險,本組病例未發生嚴重腦部并發癥。
本研究結果表明,對于Z1區TEVAR,聯合應用Castor分支支架和平行支架技術操作簡單、安全有效,短中期效果滿意,為主動脈弓疾病提供了有價值的治療選擇。本研究為單中心回顧性研究,樣本例數較少,仍需進一步積累經驗,擴大樣本量,增加隨訪時間,以進一步驗證上述結論。
利益沖突:無。
作者貢獻:孔祥負責研究設計,論文撰寫;阮鵬、余繼全負責資料收集,數據統計;孔祥、葛建軍負責論文指導。