可穿戴設備是指一類能夠與人體緊密結合的監測裝置,其設計目的是對個體活動進行持續監測,且在此過程中不妨礙或限制使用者的正常活動。隨著芯片、傳感器及人工智能技術的迅速進步,這類設備已被廣泛應用于需要連續健康監測的心血管疾病患者。對于這類患者,不論是在疾病的前期、治療階段或恢復期,均需對多項生理指標進行持續監測以評估疾病進展、治療效果及身體恢復情況。傳統的監測方式需要患者定期到醫院,借助固定設備,并由醫生進行分析,這不僅增加了患者的經濟負擔,還會消耗醫療資源和時間。然而,可穿戴設備可實時收集數據,并通過網絡直接傳輸給醫生,從而為患者提供高效且低成本的監測方案。本文將探討可穿戴設備在心血管疾病治療中的應用、優勢與挑戰,以及對其未來應用的展望。
心血管疾病以其高發病率、致殘率和死亡率的特征為全球所關注,并已逐漸成為全球主要的死因,對人類的可持續發展構成嚴重威脅[1]。在我國,由于居民普遍存在不健康生活方式、較大的心血管疾病高危人群以及日益加速的人口老齡化,心血管疾病的發病率和死亡率持續攀升。據統計,2020年我國農村和城市心血管疾病的死亡率分別高達48%和45.86%,即每5例死亡中,有近2例死于此疾病[2]。因此,對心血管疾病指標的連續、準確監測至關重要,能為早期干預和治療提供關鍵依據。傳統的數據收集方法主要有兩種:一是基于患者回憶的報告,但此方法可能受到主觀偏見的影響;二是患者在就醫時使用醫院設備進行檢測,但此方法在急性癥狀出現時往往無法提供即時數據,導致數據不夠及時且可能不準確。為解決上述問題,可穿戴設備作為一種便捷、準確、實時和專業的監測工具應運而生,能夠在關鍵時刻為醫生提供寶貴的疾病數據。本研究旨在綜述可穿戴設備在心血管疾病領域的應用和價值。
1 可穿戴設備在心血管疾病中的應用特點
1.1 設備小型化與便攜化
近年來,材料科學的突破進展為可穿戴設備的小型化和便攜化提供了堅實基礎。先進的材料技術使得微型傳感器不但擁有高集成度,而且具有更強大的計算能力,從而更高效地處理復雜數據。目前,研究者[3-4]正嘗試將傳感器與織物結合,利用身體運動過程中傳感元件的電阻變化進行監測。這主要是通過向傳感元件注入微小的恒定電流,并使用專門的高阻抗放大器實現[5]。此外,通過將人體的物理和化學反應,如脈搏、胸部擴張和汗液等轉化為必要的能量,可穿戴設備可長時間運行,進而擺脫對重型電池的依賴。例如,采用壓力發電機或摩擦發電機將機械能轉化為電能的方法,轉換效率可達50%~85%,這主要適用于低功耗設備[6–8]。盡管目前為實現持續應用,這些發電裝置需要在較大的表面積上進行集成,但其與紡織部件的結合有望實現長時間的低采樣率應用。與此同時,利用汗液作為電化學能源的生物燃料電池適用于短時應用的表皮電子設備。該裝置的功率密度可達1~3.5 mW/cm2,能在傳感模式下為模塊供電長達5 h,從而收集匯總數據。這種生物燃料電池既具有柔韌性,又便于集成到柔性傳感系統中[9–11]。然而,由于不同用戶生理出汗量和離子濃度的變化,可能導致設備性能不穩定,并受到所使用材料的限制[12]。
1.2 實時監測與自動處理
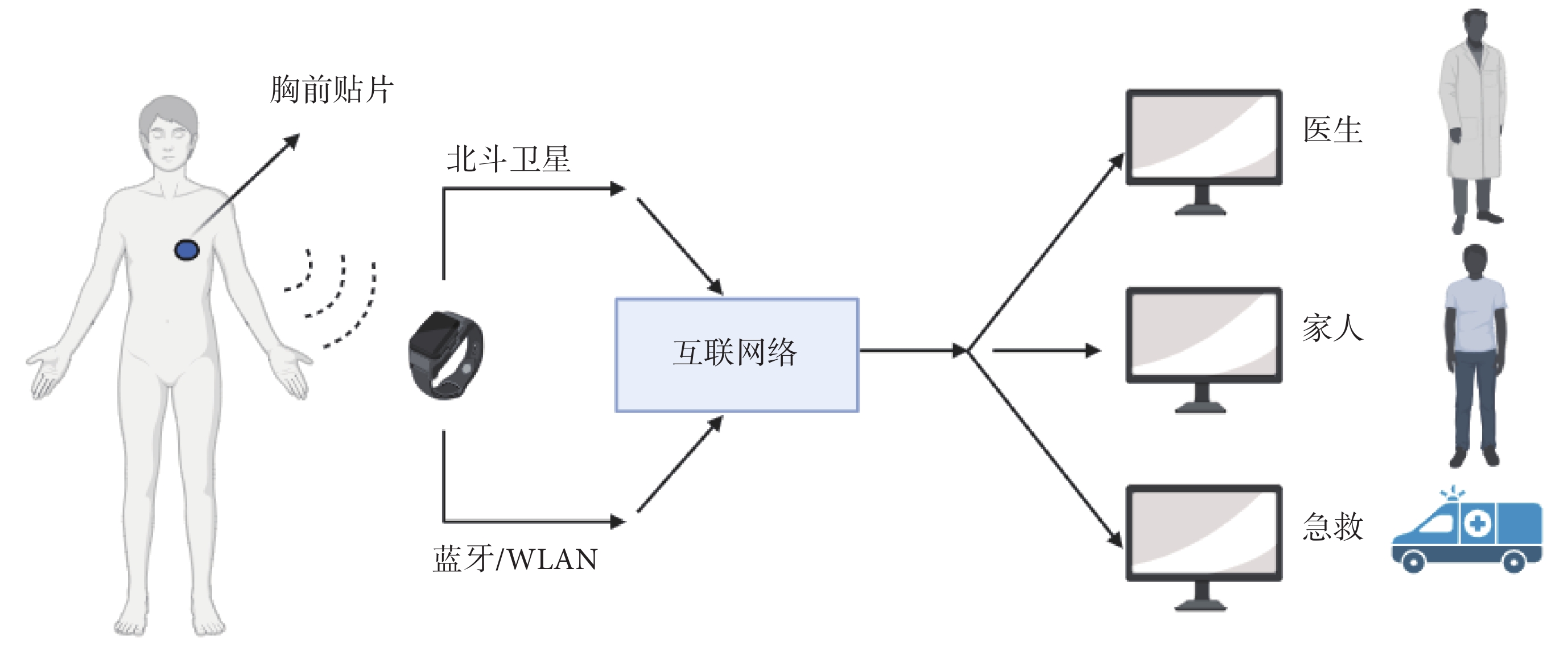
現代可穿戴設備均配備Wi-Fi功能,因此可以穩定地將監測到的數據實時上傳至云端。這些設備有能力并行監測多種生理參數,并能夠向臨床醫師發送重要的數據變化提醒。得益于網絡連接,可穿戴設備不僅能夠實時記錄并處理數據,還能將數據經整合后以用戶友好的界面展現,從而允許用戶通過智能手機、智能手表或個人計算機獲得并解讀相關信息[13];見圖1。此外,直觀且易于解讀的數據反饋可作為有效的行為干預機制,鼓勵用戶更好地遵循醫囑,形成良性循環。
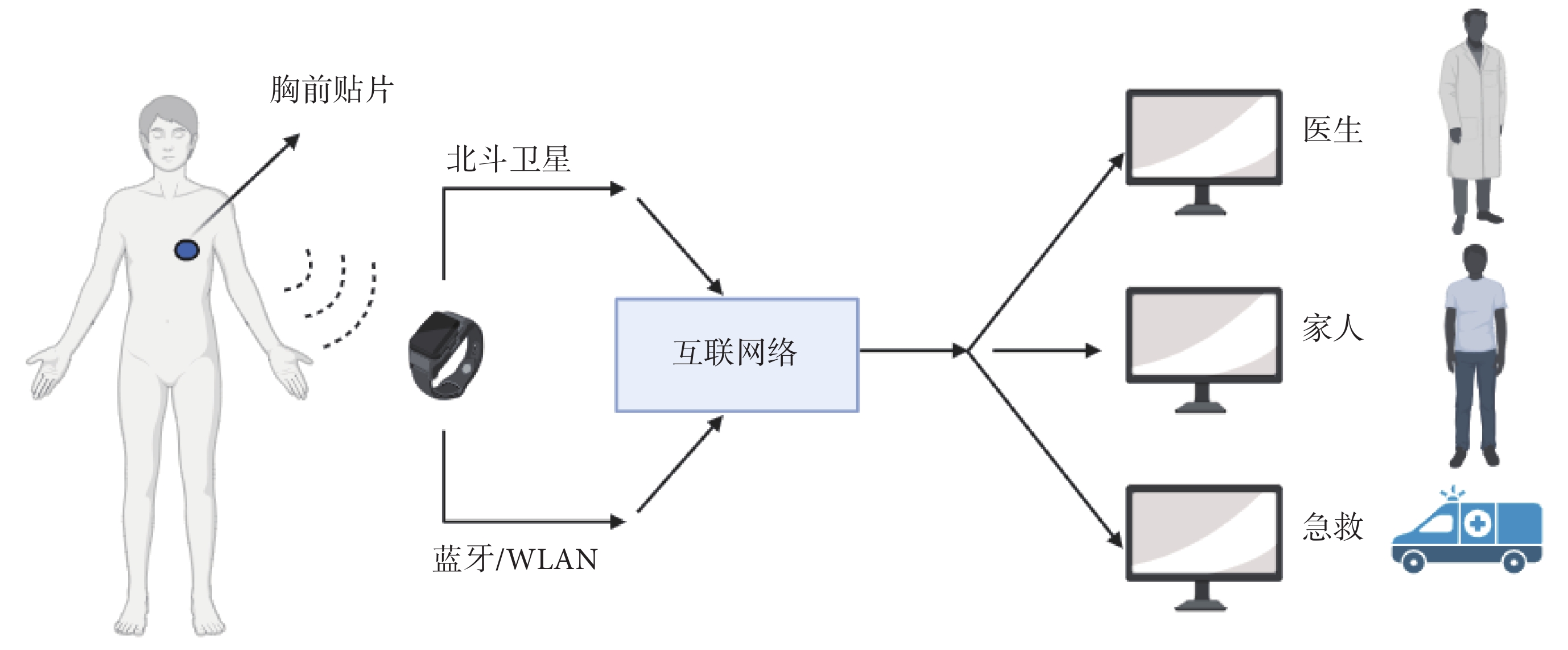 圖1
可穿戴設備工作模式
圖1
可穿戴設備工作模式
通過可穿戴傳感器監測患者運動依從性、運動表現以及相關的生理反應(即心率和呼吸頻率等),其中智能手表作為數據記錄器和網關,通過手機網絡和/或互聯網及衛星進行通信以及數據交互,使醫生、家人能夠實時觀察佩戴者的數據,發生緊急情況時急救中心可隨時根據患者定位及身體情況精準化派出救護車進行急救
相較于現有的心血管疾病監測儀器,其在運動狀態下難以實時獲取數據,從而可能遺漏了某些關鍵的實時反應[14]。而部分傳統監測數據通常是運動后獲得的,這可能導致快速的生理恢復掩蓋了應激狀態下的暫時性異常,進而產生假陰性結果。而可穿戴設備可以輕松地固定于胸部或其他部位,對用戶活動造成的限制微乎其微,從而連續記錄心臟活動,并在保障數據客觀性的同時增強用戶的安全感[15]。
從數據處理角度,可穿戴設備具備初步的數據分析功能,相較于臨床醫生面對大量數據流,其可更精確且避免不同觀察者產生的偏差。集成在可穿戴設備中的深度學習網絡,不僅在數據處理中顯示出巨大潛力,而且通過連續數據流中的關鍵信息學習與優化,可能進一步增強其泛化處理能力[16]。
1.3 數據準確性與安全性
在新技術出現的初期,媒體的廣泛關注可能會推動這些技術的快速應用。然而,對于研究人員,面對可穿戴設備在臨床場景中的迅速應用,應持審慎態度。必須承認,不準確的數據比沒有數據更具破壞性。因此,多項研究已對可穿戴設備采集的數據的準確性提出了質疑。這些設備數據的質量差異可能是由于在數字健康產品快速發展的背景下,缺乏相應的監管政策和共識。
2020年初,Coravos等[17]開發了一個實時評估傳感器準確性和效果的框架,該框架將可穿戴設備視為測試對象。這一綜合性框架概述了5個關鍵領域:驗證、分析驗證和臨床驗證,數據安全和隱私,數據管理和權利,實用性和可用性,經濟可行性。該結構化標準的目的是確保這些設備在進入市場時能獲得臨床醫生和患者的信任。之所以會有大量的未經驗證且效果和安全性存疑的產品出現在市場上,很大程度上是因為缺乏明確的監管標準和政策。
以美國為例,有心電圖功能的可穿戴設備或其他醫療相關傳感器都受到監管機構的嚴格管理。美國食品藥品監督管理局(FDA)將這些傳感器分類為Ⅰ類或Ⅱ類醫療器械,并據此實施嚴格的監管[18]。對于那些沒有明確政策監管的區域,臨床醫生在解釋由未受監管的傳感器收集的數據時必須極為謹慎,并綜合考慮多種因素,例如設備的位置、用戶的行為和具體的癥狀。與此同時,內置人工智能模型的軟件和算法正在快速發展。其對傳感器采集的復雜數據的深度分析能力也隨之增強,可以高效處理海量數據,且其分析能力遠超人類。應用增強人工智能分析臨床數據有望提升數據分析效率,并進一步提高臨床護理質量,從而提高患者的治療效果并降低醫療費用[19]。然而,人工智能算法在真實的臨床環境中仍面臨技術和倫理上的挑戰。例如:(1)算法在處理標記不足的數據時檢測混合變量的能力尚待提高;(2)算法難以完全融入常規的臨床流程;(3)算法可能加劇健康不平等現象;(4)算法可能因缺乏明確的監管而引發法律糾紛。此外,許多已公開發表的人工智能算法缺乏可復制性和透明度,這增加了其他研究者進行審核和再現的難度[20]。美國國立醫學科學院已發布了關于在臨床背景下負責任地開發和使用人工智能的指導文件。FDA也計劃通過預先認證程序來監管作為醫療器械的人工智能軟件[18]。
總之,可穿戴設備和相關的人工智能算法在醫學臨床領域的應用已越來越廣泛,但研究者和醫療工作者應持謹慎態度,確保其應用是安全、準確和有效的,以提供高質量的患者護理。
2 可穿戴設備在不同心血管疾病中的應用
2.1 心律失常
在心血管疾病的診斷與管理中,心率作為基本生理指標,不僅反映心臟功能,而且對于識別心律失常具有關鍵作用。長期維持較高水平的心率,對于心血管疾病患者往往預示著不佳的臨床預后[21]。同時,心輸出量是反映心臟泵血功能的關鍵參數,由每搏輸出量與心率的乘積確定。因此,無論在健康還是疾病狀態下,心率對于維持適當的心輸出量均具有至關重要的作用[22]。
盡管傳統的心率測量需要在專業的醫療環境下由專業人員操作,但隨著科技的發展,現已推出了各種可穿戴心率測量設備。其中,腕部可穿戴設備與胸前貼片式設備為主流選擇。此外,隨著光電容積脈搏傳感器技術的微型化,現已能夠集成至日常使用的眼鏡或戒指中[23]。這些設備多數采用了峰值檢測算法,與傳統的遙測方法相比,此算法的中位數誤差<5%[24]。然而,對于某些特定的心律失常,如心房顫動(房顫)、房性或室性早搏,峰值檢測可能會受到干擾,從而導致測量偏差。因此,已有研究者針對此問題,開發出更為精確的算法以提高心率監測的準確性。
為滿足持續心率監測的需求,新型自供電可穿戴設備已經問世。這些設備能夠通過捕捉手腕上橈動脈脈搏產生的生物力學能量,進而將機械能轉化為電能,從而實現持續的心率監測[25]。
對于心律失常,尤其是陣發性心律失常,傳統的心電圖和動態心電圖(Holter)往往無法長時間監測,并可能因此錯過關鍵診斷信息。而植入式設備,雖然可以長時間記錄,但由于其侵入性及需要專業操作的限制,普及率較低。針對心律失常開發的可穿戴設備,憑借光電容積脈搏波傳感器,其對心律失常的敏感性和特異性均可達91%~100%[26]。尤其是對于房顫,這種與卒中風險顯著相關的心律失常,及時和準確判斷顯得尤為重要。通過新型算法支持的可穿戴設備,如智能手表和智能手機,能夠實現對房顫的高效篩查。研究[27–29]顯示,基于光電容積脈搏波算法的智能手機對房顫篩查的靈敏度和特異性分別為90%~96%和85%~99%。
在中國,已有近25萬人參與一項采用智能設備進行房顫篩查的研究[30],其中超過18萬人使用專為此目的開發的手機應用程序。結果顯示,0.23%的參與者收到了房顫警示,而經驗證,這些警示的陽性預測值高達91.6%。
盡管基于光電容積技術的可穿戴設備在心律失常篩查中展現了強大的潛力,但其仍然存在一定的局限性。例如,對于患有心臟期前收縮或皮膚色素沉著的患者,設備的準確性可能會受到影響。因此,為確保最佳的臨床效果,繼續研究與優化這些設備仍然至關重要[31-32]。
2.2 高血壓
血壓測量在眾多臨床疾病的治療與管理中均具有核心地位。高血壓與多種慢性疾病存在緊密關系,且它是全球疾病的主要發病與致死因素[33]。盡管大眾普遍認為血壓是動態變化的參數,但高血壓治療指南依然建議以靜態血壓的平均值為測量標準,旨在對波動及尖峰進行平衡處理[34]。傳統血壓測量方法主要分為有創和無創兩大類。其中,動脈置管被視為有創的金標準,即通過在大動脈中置入一個壓力傳感器來獲取血壓波形圖[35-36]。而標準的無創方法則為人工聽診,醫生將聽診器放置于肱動脈上并使用水銀壓力計的袖帶對上臂施加壓力,通過觀察袖帶內壓并同時監聽Korotkoff聲音來測定收縮壓與舒張壓[37]。但由于血壓測量數據存在持續性波動,當前的測量方法均無法實現完美的數值重復。因此,亟需能在日常中進行頻繁準確測量的便攜式或可穿戴式設備。光電容積脈搏波描記法(PPG)作為一種主流方法,隨著技術進步,其成本逐漸降低,并更加便攜、微型化,更易于集成入手表或智能手機等可穿戴設備,促進其在市場上的推廣。該技術可以追溯至20世紀30年代,原理為通過血管對光的吸收與反射量來估計血液體積[38]。Aktiia手環作為一款基于PPG技術的無袖帶血壓測量裝置,需要用戶初次使用時進行校準,并進行定期的復核以確保測量準確性[39]。另有設備集成了多種技術和參數,如脈搏傳導時間、脈搏波分析及PPG等,能夠持續記錄血壓數據,為用戶提供豐富的血壓變化信息[40]。這些設備為高血壓的監測、診斷、控制和長期隨訪提供了極大的助力。但盡管如此,數據校準等問題仍是其在日常使用中所面臨的主要挑戰。當前對這些設備進行數據校準的方法尚缺乏大量的證據支持其可靠性。
2.3 心力衰竭
心力衰竭是一種臨床病癥,其經濟負擔重大并具有較高的患病率。相較于同年齡人群,心力衰竭患者的生存率明顯降低。作為多數心血管疾病的終末階段,心力衰竭的發病有時可能突如其來,且在一系列癥狀和體征惡化之后,迅速進入失代償狀態[41]。然而,許多心力衰竭的典型癥狀(如呼吸困難、疲勞等)和體征(如外周水腫等)并不特異,特別是在老年人中,這些癥狀和體征可能由其他疾病或治療副作用引發。而頸靜脈怒張、心臟擴大及第三心音等體征較為特異,卻在臨床實踐中并不常見[42–44]。
確診心力衰竭,尤其是明確左心室的功能狀態(是否存在收縮功能障礙)仍具有挑戰性。盡管對于左心室射血分數降低的心力衰竭存在明確的藥物治療方案,但在治療指南的應用和藥物劑量選擇上仍存在分歧[45]。因此,心力衰竭的診斷、管理和治療方法亟待進一步優化。在這方面,結合可穿戴技術與數字健康手段可能提供新的解決途徑。
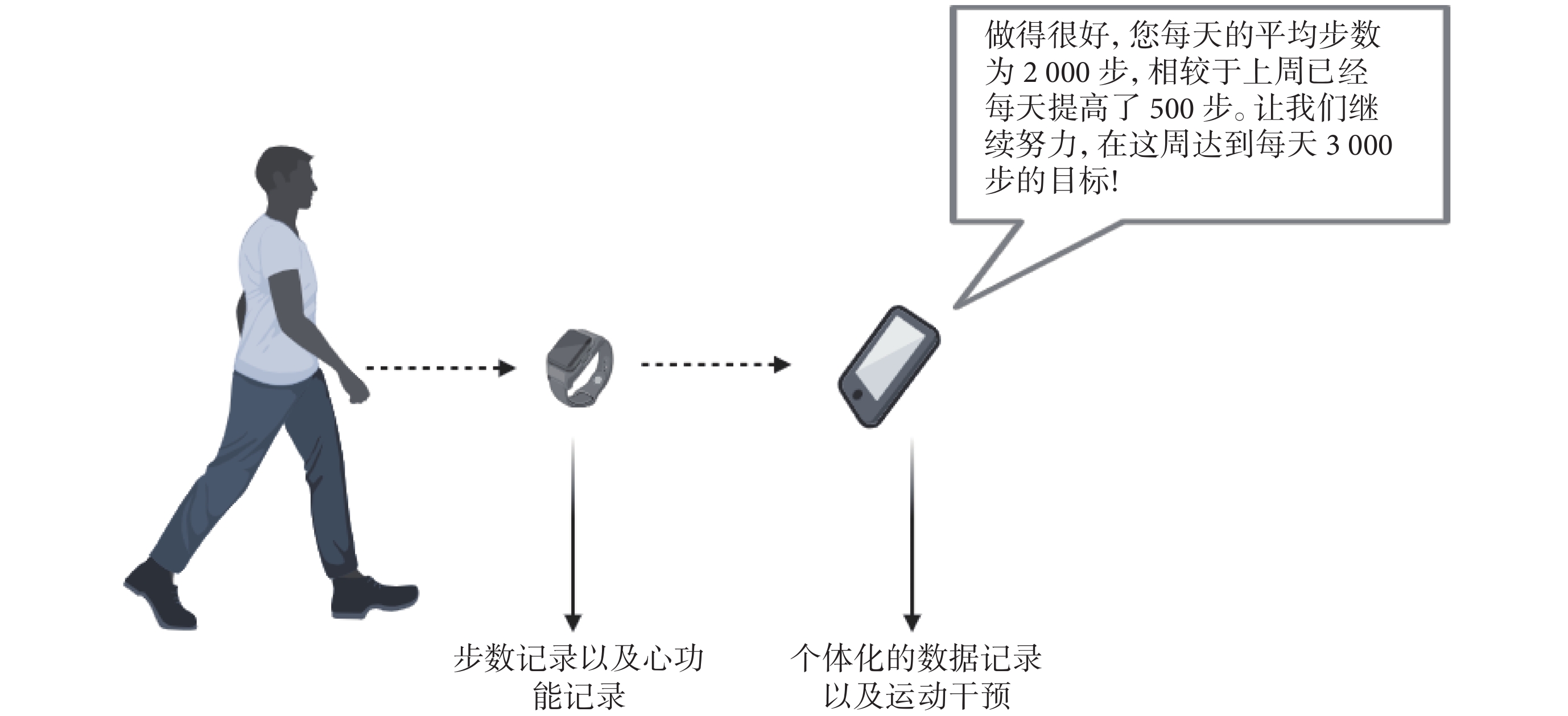
可穿戴設備的核心優勢在于其能夠超出傳統醫療環境,實時監測患者的健康數據,為醫療決策提供實證依據,同時為生活方式的干預提供數據支持。例如,在心力衰竭的預防方面,實時步數反饋和個性化健康信息有助于豐富改變生活方式的干預措施;見圖2。此外,心力衰竭患者的活動水平下降通常預示疾病進展和較差預后[46]。
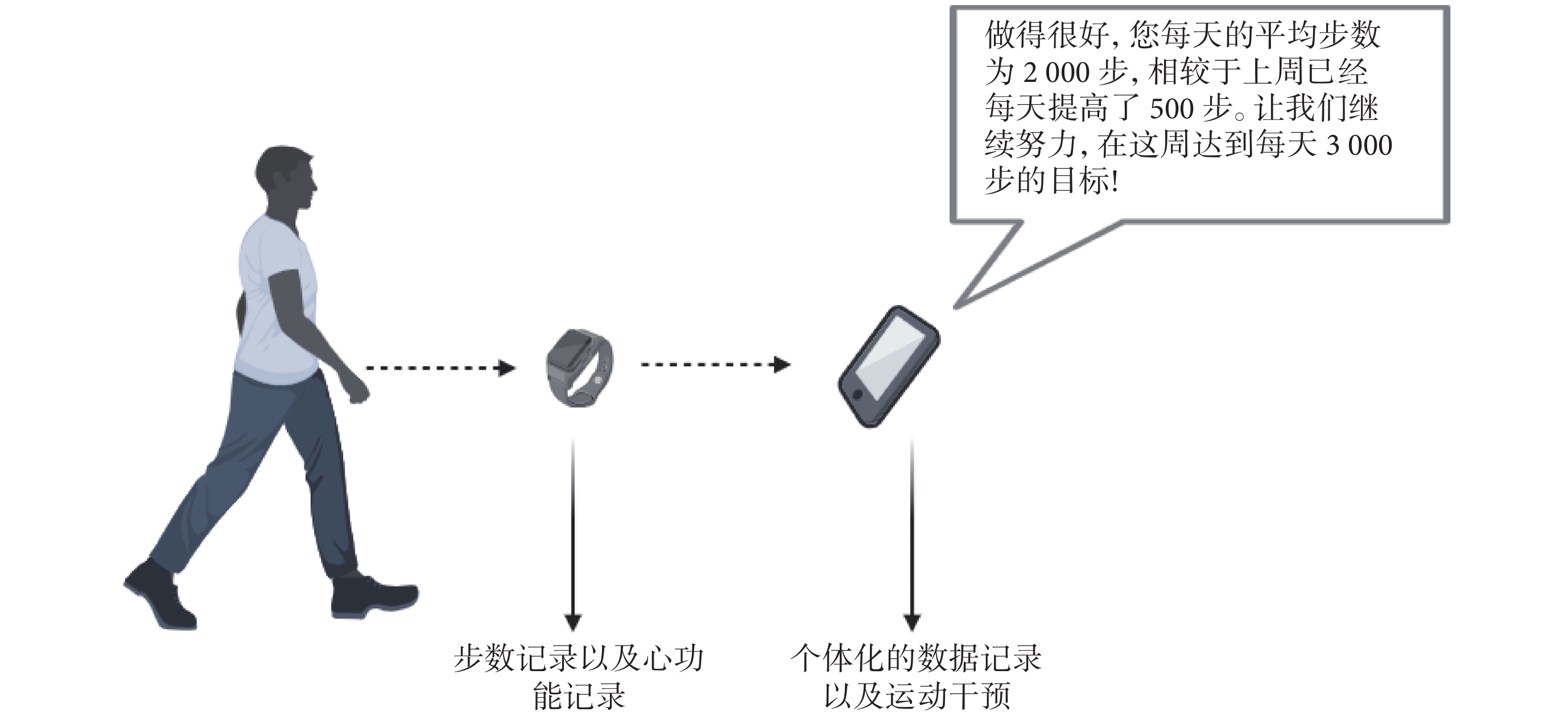 圖2
可穿戴設備作為干預方案在心力衰竭患者中的作用形式
圖2
可穿戴設備作為干預方案在心力衰竭患者中的作用形式
近期研究[47-48]利用腕帶式可穿戴設備監測心力衰竭患者的日常活動,發現低活動水平與更高的住院率密切相關。在治療策略中,盡管藥物治療仍是關鍵,但患者對治療的依從性仍不盡如人意,導致不良事件和更高的死亡率。此外,低健康素養、缺乏對藥物說明書的正確理解等問題也對藥物治療效果產生負面影響[49-50]。
最近,一項隨機對照試驗[51]探討利用可穿戴設備改善患者的服藥依從性,通過向患者提供自身活動的個性化反饋,以此來評估其服藥依從性是否會發生改變。如果此種干預在改善心力衰竭患者的臨床狀況中顯示出積極效果,那么將有必要進行更大規模的研究來全面評估其臨床效益。
2.4 外周動脈疾病
根據現有數據顯示,全球約有超過2億人受到外周動脈疾病的困擾,其中超過50%的受影響人群并未表現明顯癥狀,然而,這部分無癥狀患者在進行截肢手術的患者中占3%~4%。更為重要的是,外周動脈疾病常為冠狀動脈粥樣硬化性疾病的前驅,從而顯著提高患者發生心血管相關性死亡和心肌梗死的風險[52]。間歇性跛行是該疾病的標志性癥狀,而目前的研究表明,通過專業的運動療法可以明顯改善此癥狀。間歇性跛行的主要傳統治療方法是評估運動療法,其效果主要依賴于患者自我報告,這種方法在長期的身體活動量化上存在局限性。而現代技術,如智能手機應用與可穿戴設備相結合,提供了對患者運動療法的實時監測和反饋,從而可能增強療法的依從性和潛在的治療效果。值得注意的是,當前面向家庭運動療法的應用大多與商用健身應用同步,專為外周動脈疾病設計的應用相對較少,故僅能用作患者的監測、培訓、指導和教育。
踝肱指數被認為是評估外周動脈疾病的關鍵指標,及時、持續地對高風險人群進行踝肱指數監測,并進行早期干預,對于降低該疾病的致死率具有至關重要的意義[53]。美國國家衛生保健優化研究所與歐洲心臟病學會均建議利用踝肱指數評估外周動脈疾病的嚴重程度[54]。手持多普勒是測量踝肱指數的金標準,但該設備的使用需要經過專家培訓以便精準操作來確保準確性[55]。Watson等[56]比較了英國市場上6種測量踝肱指數的系統,結論是MESI設備因其較高的敏感性和特異性而被認為是首選。未來,對MESI設備的進一步可行性研究將為評估其對心血管健康的長期影響提供重要依據。
2.5 冠狀動脈粥樣硬化性心血管疾病
盡管在某些發達國家,冠狀動脈粥樣硬化性心血管疾病的死亡率呈下降趨勢,但該疾病在中國及其他發展中國家仍為過早發病與死亡的主導因素。在中國,由于該疾病引發的死亡人數達到約240萬,占心血管疾病相關死亡的65%及總死亡的25%。而且,鑒于風險因素如肥胖、高血壓、糖尿病和不良生活習慣等普遍存在,冠狀動脈粥樣硬化性心血管疾病的疾病負擔仍在增長[57]。因此,預防此疾病的流行顯得尤為重要。血脂異常被認為是冠狀動脈粥樣硬化病變的關鍵,眾多學者和衛生機構都強調了心肺適能(CRF)與肌肉力量在改善血脂水平的核心作用,其機制主要是降低動脈粥樣硬化相關的脂蛋白表達[58]。值得注意的是,有氧運動訓練和阻力訓練均可增強心肺適能和肌肉力量,進而降低動脈粥樣硬化相關的脂蛋白表達。Lavie等[59]的研究進一步證實,運動訓練能夠持續優化血脂和心臟的代謝狀態。目前,市場上已推出各種針對運動表現的可穿戴監測設備,能為用戶提供即時的運動效果評估,并將運動數據轉化為對血脂影響的反饋。通過深度學習技術,這些設備還能為個體制定最佳運動方案[60]。此外,對于主動脈的僵硬度監測亦被視為預測冠狀動脈粥樣硬化性心血管疾病的有效方法[61-62]。有研究[63]使用智能手表來監測腕部的脈搏波,并間接測定頸動脈至股動脈的脈搏波速度,隨后利用XGBoost算法模型進行主動脈僵硬度評估。在97名受試者中,預測的頸-股脈搏波速度與標準測量結果高度相關(r=0.927,P<0.001),所得的主動脈僵硬度評估同樣準確。考慮到此類算法在可穿戴設備上的適應性,以及高度的準確性和穩定性,應進一步完善此評估模型,使主動脈僵硬度的篩查準確率能夠超過90%,并推動其在更廣泛的人群中應用。
3 總結與展望
當前,針對可穿戴設備的研究正逐步導向家庭為中心的醫療監測新模式。此模式極大地便利了疾病的診斷、治療及護理流程,尤其是對于需長期監測生理指標的心血管疾病患者。這種創新模式不僅促進了醫療資源的優化配置,同時也顯著降低了患者的經濟與精神負擔。盡管如此,一些技術與實踐挑戰限制了可穿戴技術在心血管領域的廣泛應用。然而,伴隨傳感器和計算技術的持續進步,預計可穿戴設備將具備更為復雜的功能特性,成為心血管疾病診療過程中的重要組成部分。這不僅增強了疾病管理和干預的有效性,也為應對突發醫療情況提供了強有力的支持。可以預見的是,由可穿戴設備收集的海量數據為心血管疾病的未來研究方向提供了寶貴的參考與指導,有望為個體及社會帶來顯著的醫療獲益。
利益沖突:無。
作者貢獻:馬鑫負責論文設計,查閱文獻,論文撰寫;李慧珍負責查閱和匯總部分文獻;李勇男負責修改論文;吳向陽負責審閱及修改部分論文。
心血管疾病以其高發病率、致殘率和死亡率的特征為全球所關注,并已逐漸成為全球主要的死因,對人類的可持續發展構成嚴重威脅[1]。在我國,由于居民普遍存在不健康生活方式、較大的心血管疾病高危人群以及日益加速的人口老齡化,心血管疾病的發病率和死亡率持續攀升。據統計,2020年我國農村和城市心血管疾病的死亡率分別高達48%和45.86%,即每5例死亡中,有近2例死于此疾病[2]。因此,對心血管疾病指標的連續、準確監測至關重要,能為早期干預和治療提供關鍵依據。傳統的數據收集方法主要有兩種:一是基于患者回憶的報告,但此方法可能受到主觀偏見的影響;二是患者在就醫時使用醫院設備進行檢測,但此方法在急性癥狀出現時往往無法提供即時數據,導致數據不夠及時且可能不準確。為解決上述問題,可穿戴設備作為一種便捷、準確、實時和專業的監測工具應運而生,能夠在關鍵時刻為醫生提供寶貴的疾病數據。本研究旨在綜述可穿戴設備在心血管疾病領域的應用和價值。
1 可穿戴設備在心血管疾病中的應用特點
1.1 設備小型化與便攜化
近年來,材料科學的突破進展為可穿戴設備的小型化和便攜化提供了堅實基礎。先進的材料技術使得微型傳感器不但擁有高集成度,而且具有更強大的計算能力,從而更高效地處理復雜數據。目前,研究者[3-4]正嘗試將傳感器與織物結合,利用身體運動過程中傳感元件的電阻變化進行監測。這主要是通過向傳感元件注入微小的恒定電流,并使用專門的高阻抗放大器實現[5]。此外,通過將人體的物理和化學反應,如脈搏、胸部擴張和汗液等轉化為必要的能量,可穿戴設備可長時間運行,進而擺脫對重型電池的依賴。例如,采用壓力發電機或摩擦發電機將機械能轉化為電能的方法,轉換效率可達50%~85%,這主要適用于低功耗設備[6–8]。盡管目前為實現持續應用,這些發電裝置需要在較大的表面積上進行集成,但其與紡織部件的結合有望實現長時間的低采樣率應用。與此同時,利用汗液作為電化學能源的生物燃料電池適用于短時應用的表皮電子設備。該裝置的功率密度可達1~3.5 mW/cm2,能在傳感模式下為模塊供電長達5 h,從而收集匯總數據。這種生物燃料電池既具有柔韌性,又便于集成到柔性傳感系統中[9–11]。然而,由于不同用戶生理出汗量和離子濃度的變化,可能導致設備性能不穩定,并受到所使用材料的限制[12]。
1.2 實時監測與自動處理
現代可穿戴設備均配備Wi-Fi功能,因此可以穩定地將監測到的數據實時上傳至云端。這些設備有能力并行監測多種生理參數,并能夠向臨床醫師發送重要的數據變化提醒。得益于網絡連接,可穿戴設備不僅能夠實時記錄并處理數據,還能將數據經整合后以用戶友好的界面展現,從而允許用戶通過智能手機、智能手表或個人計算機獲得并解讀相關信息[13];見圖1。此外,直觀且易于解讀的數據反饋可作為有效的行為干預機制,鼓勵用戶更好地遵循醫囑,形成良性循環。
 圖1
可穿戴設備工作模式
圖1
可穿戴設備工作模式
通過可穿戴傳感器監測患者運動依從性、運動表現以及相關的生理反應(即心率和呼吸頻率等),其中智能手表作為數據記錄器和網關,通過手機網絡和/或互聯網及衛星進行通信以及數據交互,使醫生、家人能夠實時觀察佩戴者的數據,發生緊急情況時急救中心可隨時根據患者定位及身體情況精準化派出救護車進行急救
相較于現有的心血管疾病監測儀器,其在運動狀態下難以實時獲取數據,從而可能遺漏了某些關鍵的實時反應[14]。而部分傳統監測數據通常是運動后獲得的,這可能導致快速的生理恢復掩蓋了應激狀態下的暫時性異常,進而產生假陰性結果。而可穿戴設備可以輕松地固定于胸部或其他部位,對用戶活動造成的限制微乎其微,從而連續記錄心臟活動,并在保障數據客觀性的同時增強用戶的安全感[15]。
從數據處理角度,可穿戴設備具備初步的數據分析功能,相較于臨床醫生面對大量數據流,其可更精確且避免不同觀察者產生的偏差。集成在可穿戴設備中的深度學習網絡,不僅在數據處理中顯示出巨大潛力,而且通過連續數據流中的關鍵信息學習與優化,可能進一步增強其泛化處理能力[16]。
1.3 數據準確性與安全性
在新技術出現的初期,媒體的廣泛關注可能會推動這些技術的快速應用。然而,對于研究人員,面對可穿戴設備在臨床場景中的迅速應用,應持審慎態度。必須承認,不準確的數據比沒有數據更具破壞性。因此,多項研究已對可穿戴設備采集的數據的準確性提出了質疑。這些設備數據的質量差異可能是由于在數字健康產品快速發展的背景下,缺乏相應的監管政策和共識。
2020年初,Coravos等[17]開發了一個實時評估傳感器準確性和效果的框架,該框架將可穿戴設備視為測試對象。這一綜合性框架概述了5個關鍵領域:驗證、分析驗證和臨床驗證,數據安全和隱私,數據管理和權利,實用性和可用性,經濟可行性。該結構化標準的目的是確保這些設備在進入市場時能獲得臨床醫生和患者的信任。之所以會有大量的未經驗證且效果和安全性存疑的產品出現在市場上,很大程度上是因為缺乏明確的監管標準和政策。
以美國為例,有心電圖功能的可穿戴設備或其他醫療相關傳感器都受到監管機構的嚴格管理。美國食品藥品監督管理局(FDA)將這些傳感器分類為Ⅰ類或Ⅱ類醫療器械,并據此實施嚴格的監管[18]。對于那些沒有明確政策監管的區域,臨床醫生在解釋由未受監管的傳感器收集的數據時必須極為謹慎,并綜合考慮多種因素,例如設備的位置、用戶的行為和具體的癥狀。與此同時,內置人工智能模型的軟件和算法正在快速發展。其對傳感器采集的復雜數據的深度分析能力也隨之增強,可以高效處理海量數據,且其分析能力遠超人類。應用增強人工智能分析臨床數據有望提升數據分析效率,并進一步提高臨床護理質量,從而提高患者的治療效果并降低醫療費用[19]。然而,人工智能算法在真實的臨床環境中仍面臨技術和倫理上的挑戰。例如:(1)算法在處理標記不足的數據時檢測混合變量的能力尚待提高;(2)算法難以完全融入常規的臨床流程;(3)算法可能加劇健康不平等現象;(4)算法可能因缺乏明確的監管而引發法律糾紛。此外,許多已公開發表的人工智能算法缺乏可復制性和透明度,這增加了其他研究者進行審核和再現的難度[20]。美國國立醫學科學院已發布了關于在臨床背景下負責任地開發和使用人工智能的指導文件。FDA也計劃通過預先認證程序來監管作為醫療器械的人工智能軟件[18]。
總之,可穿戴設備和相關的人工智能算法在醫學臨床領域的應用已越來越廣泛,但研究者和醫療工作者應持謹慎態度,確保其應用是安全、準確和有效的,以提供高質量的患者護理。
2 可穿戴設備在不同心血管疾病中的應用
2.1 心律失常
在心血管疾病的診斷與管理中,心率作為基本生理指標,不僅反映心臟功能,而且對于識別心律失常具有關鍵作用。長期維持較高水平的心率,對于心血管疾病患者往往預示著不佳的臨床預后[21]。同時,心輸出量是反映心臟泵血功能的關鍵參數,由每搏輸出量與心率的乘積確定。因此,無論在健康還是疾病狀態下,心率對于維持適當的心輸出量均具有至關重要的作用[22]。
盡管傳統的心率測量需要在專業的醫療環境下由專業人員操作,但隨著科技的發展,現已推出了各種可穿戴心率測量設備。其中,腕部可穿戴設備與胸前貼片式設備為主流選擇。此外,隨著光電容積脈搏傳感器技術的微型化,現已能夠集成至日常使用的眼鏡或戒指中[23]。這些設備多數采用了峰值檢測算法,與傳統的遙測方法相比,此算法的中位數誤差<5%[24]。然而,對于某些特定的心律失常,如心房顫動(房顫)、房性或室性早搏,峰值檢測可能會受到干擾,從而導致測量偏差。因此,已有研究者針對此問題,開發出更為精確的算法以提高心率監測的準確性。
為滿足持續心率監測的需求,新型自供電可穿戴設備已經問世。這些設備能夠通過捕捉手腕上橈動脈脈搏產生的生物力學能量,進而將機械能轉化為電能,從而實現持續的心率監測[25]。
對于心律失常,尤其是陣發性心律失常,傳統的心電圖和動態心電圖(Holter)往往無法長時間監測,并可能因此錯過關鍵診斷信息。而植入式設備,雖然可以長時間記錄,但由于其侵入性及需要專業操作的限制,普及率較低。針對心律失常開發的可穿戴設備,憑借光電容積脈搏波傳感器,其對心律失常的敏感性和特異性均可達91%~100%[26]。尤其是對于房顫,這種與卒中風險顯著相關的心律失常,及時和準確判斷顯得尤為重要。通過新型算法支持的可穿戴設備,如智能手表和智能手機,能夠實現對房顫的高效篩查。研究[27–29]顯示,基于光電容積脈搏波算法的智能手機對房顫篩查的靈敏度和特異性分別為90%~96%和85%~99%。
在中國,已有近25萬人參與一項采用智能設備進行房顫篩查的研究[30],其中超過18萬人使用專為此目的開發的手機應用程序。結果顯示,0.23%的參與者收到了房顫警示,而經驗證,這些警示的陽性預測值高達91.6%。
盡管基于光電容積技術的可穿戴設備在心律失常篩查中展現了強大的潛力,但其仍然存在一定的局限性。例如,對于患有心臟期前收縮或皮膚色素沉著的患者,設備的準確性可能會受到影響。因此,為確保最佳的臨床效果,繼續研究與優化這些設備仍然至關重要[31-32]。
2.2 高血壓
血壓測量在眾多臨床疾病的治療與管理中均具有核心地位。高血壓與多種慢性疾病存在緊密關系,且它是全球疾病的主要發病與致死因素[33]。盡管大眾普遍認為血壓是動態變化的參數,但高血壓治療指南依然建議以靜態血壓的平均值為測量標準,旨在對波動及尖峰進行平衡處理[34]。傳統血壓測量方法主要分為有創和無創兩大類。其中,動脈置管被視為有創的金標準,即通過在大動脈中置入一個壓力傳感器來獲取血壓波形圖[35-36]。而標準的無創方法則為人工聽診,醫生將聽診器放置于肱動脈上并使用水銀壓力計的袖帶對上臂施加壓力,通過觀察袖帶內壓并同時監聽Korotkoff聲音來測定收縮壓與舒張壓[37]。但由于血壓測量數據存在持續性波動,當前的測量方法均無法實現完美的數值重復。因此,亟需能在日常中進行頻繁準確測量的便攜式或可穿戴式設備。光電容積脈搏波描記法(PPG)作為一種主流方法,隨著技術進步,其成本逐漸降低,并更加便攜、微型化,更易于集成入手表或智能手機等可穿戴設備,促進其在市場上的推廣。該技術可以追溯至20世紀30年代,原理為通過血管對光的吸收與反射量來估計血液體積[38]。Aktiia手環作為一款基于PPG技術的無袖帶血壓測量裝置,需要用戶初次使用時進行校準,并進行定期的復核以確保測量準確性[39]。另有設備集成了多種技術和參數,如脈搏傳導時間、脈搏波分析及PPG等,能夠持續記錄血壓數據,為用戶提供豐富的血壓變化信息[40]。這些設備為高血壓的監測、診斷、控制和長期隨訪提供了極大的助力。但盡管如此,數據校準等問題仍是其在日常使用中所面臨的主要挑戰。當前對這些設備進行數據校準的方法尚缺乏大量的證據支持其可靠性。
2.3 心力衰竭
心力衰竭是一種臨床病癥,其經濟負擔重大并具有較高的患病率。相較于同年齡人群,心力衰竭患者的生存率明顯降低。作為多數心血管疾病的終末階段,心力衰竭的發病有時可能突如其來,且在一系列癥狀和體征惡化之后,迅速進入失代償狀態[41]。然而,許多心力衰竭的典型癥狀(如呼吸困難、疲勞等)和體征(如外周水腫等)并不特異,特別是在老年人中,這些癥狀和體征可能由其他疾病或治療副作用引發。而頸靜脈怒張、心臟擴大及第三心音等體征較為特異,卻在臨床實踐中并不常見[42–44]。
確診心力衰竭,尤其是明確左心室的功能狀態(是否存在收縮功能障礙)仍具有挑戰性。盡管對于左心室射血分數降低的心力衰竭存在明確的藥物治療方案,但在治療指南的應用和藥物劑量選擇上仍存在分歧[45]。因此,心力衰竭的診斷、管理和治療方法亟待進一步優化。在這方面,結合可穿戴技術與數字健康手段可能提供新的解決途徑。
可穿戴設備的核心優勢在于其能夠超出傳統醫療環境,實時監測患者的健康數據,為醫療決策提供實證依據,同時為生活方式的干預提供數據支持。例如,在心力衰竭的預防方面,實時步數反饋和個性化健康信息有助于豐富改變生活方式的干預措施;見圖2。此外,心力衰竭患者的活動水平下降通常預示疾病進展和較差預后[46]。
 圖2
可穿戴設備作為干預方案在心力衰竭患者中的作用形式
圖2
可穿戴設備作為干預方案在心力衰竭患者中的作用形式
近期研究[47-48]利用腕帶式可穿戴設備監測心力衰竭患者的日常活動,發現低活動水平與更高的住院率密切相關。在治療策略中,盡管藥物治療仍是關鍵,但患者對治療的依從性仍不盡如人意,導致不良事件和更高的死亡率。此外,低健康素養、缺乏對藥物說明書的正確理解等問題也對藥物治療效果產生負面影響[49-50]。
最近,一項隨機對照試驗[51]探討利用可穿戴設備改善患者的服藥依從性,通過向患者提供自身活動的個性化反饋,以此來評估其服藥依從性是否會發生改變。如果此種干預在改善心力衰竭患者的臨床狀況中顯示出積極效果,那么將有必要進行更大規模的研究來全面評估其臨床效益。
2.4 外周動脈疾病
根據現有數據顯示,全球約有超過2億人受到外周動脈疾病的困擾,其中超過50%的受影響人群并未表現明顯癥狀,然而,這部分無癥狀患者在進行截肢手術的患者中占3%~4%。更為重要的是,外周動脈疾病常為冠狀動脈粥樣硬化性疾病的前驅,從而顯著提高患者發生心血管相關性死亡和心肌梗死的風險[52]。間歇性跛行是該疾病的標志性癥狀,而目前的研究表明,通過專業的運動療法可以明顯改善此癥狀。間歇性跛行的主要傳統治療方法是評估運動療法,其效果主要依賴于患者自我報告,這種方法在長期的身體活動量化上存在局限性。而現代技術,如智能手機應用與可穿戴設備相結合,提供了對患者運動療法的實時監測和反饋,從而可能增強療法的依從性和潛在的治療效果。值得注意的是,當前面向家庭運動療法的應用大多與商用健身應用同步,專為外周動脈疾病設計的應用相對較少,故僅能用作患者的監測、培訓、指導和教育。
踝肱指數被認為是評估外周動脈疾病的關鍵指標,及時、持續地對高風險人群進行踝肱指數監測,并進行早期干預,對于降低該疾病的致死率具有至關重要的意義[53]。美國國家衛生保健優化研究所與歐洲心臟病學會均建議利用踝肱指數評估外周動脈疾病的嚴重程度[54]。手持多普勒是測量踝肱指數的金標準,但該設備的使用需要經過專家培訓以便精準操作來確保準確性[55]。Watson等[56]比較了英國市場上6種測量踝肱指數的系統,結論是MESI設備因其較高的敏感性和特異性而被認為是首選。未來,對MESI設備的進一步可行性研究將為評估其對心血管健康的長期影響提供重要依據。
2.5 冠狀動脈粥樣硬化性心血管疾病
盡管在某些發達國家,冠狀動脈粥樣硬化性心血管疾病的死亡率呈下降趨勢,但該疾病在中國及其他發展中國家仍為過早發病與死亡的主導因素。在中國,由于該疾病引發的死亡人數達到約240萬,占心血管疾病相關死亡的65%及總死亡的25%。而且,鑒于風險因素如肥胖、高血壓、糖尿病和不良生活習慣等普遍存在,冠狀動脈粥樣硬化性心血管疾病的疾病負擔仍在增長[57]。因此,預防此疾病的流行顯得尤為重要。血脂異常被認為是冠狀動脈粥樣硬化病變的關鍵,眾多學者和衛生機構都強調了心肺適能(CRF)與肌肉力量在改善血脂水平的核心作用,其機制主要是降低動脈粥樣硬化相關的脂蛋白表達[58]。值得注意的是,有氧運動訓練和阻力訓練均可增強心肺適能和肌肉力量,進而降低動脈粥樣硬化相關的脂蛋白表達。Lavie等[59]的研究進一步證實,運動訓練能夠持續優化血脂和心臟的代謝狀態。目前,市場上已推出各種針對運動表現的可穿戴監測設備,能為用戶提供即時的運動效果評估,并將運動數據轉化為對血脂影響的反饋。通過深度學習技術,這些設備還能為個體制定最佳運動方案[60]。此外,對于主動脈的僵硬度監測亦被視為預測冠狀動脈粥樣硬化性心血管疾病的有效方法[61-62]。有研究[63]使用智能手表來監測腕部的脈搏波,并間接測定頸動脈至股動脈的脈搏波速度,隨后利用XGBoost算法模型進行主動脈僵硬度評估。在97名受試者中,預測的頸-股脈搏波速度與標準測量結果高度相關(r=0.927,P<0.001),所得的主動脈僵硬度評估同樣準確。考慮到此類算法在可穿戴設備上的適應性,以及高度的準確性和穩定性,應進一步完善此評估模型,使主動脈僵硬度的篩查準確率能夠超過90%,并推動其在更廣泛的人群中應用。
3 總結與展望
當前,針對可穿戴設備的研究正逐步導向家庭為中心的醫療監測新模式。此模式極大地便利了疾病的診斷、治療及護理流程,尤其是對于需長期監測生理指標的心血管疾病患者。這種創新模式不僅促進了醫療資源的優化配置,同時也顯著降低了患者的經濟與精神負擔。盡管如此,一些技術與實踐挑戰限制了可穿戴技術在心血管領域的廣泛應用。然而,伴隨傳感器和計算技術的持續進步,預計可穿戴設備將具備更為復雜的功能特性,成為心血管疾病診療過程中的重要組成部分。這不僅增強了疾病管理和干預的有效性,也為應對突發醫療情況提供了強有力的支持。可以預見的是,由可穿戴設備收集的海量數據為心血管疾病的未來研究方向提供了寶貴的參考與指導,有望為個體及社會帶來顯著的醫療獲益。
利益沖突:無。
作者貢獻:馬鑫負責論文設計,查閱文獻,論文撰寫;李慧珍負責查閱和匯總部分文獻;李勇男負責修改論文;吳向陽負責審閱及修改部分論文。