引用本文: 謝林, 吳鑄衡, 劉靖宇, 賃可. 主動脈瓣成形與Ross手術治療兒童重度主動脈瓣病變近中期效果的回顧性隊列研究. 中國胸心血管外科臨床雜志, 2024, 31(12): 1794-1802. doi: 10.7507/1007-4848.202405003 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
兒童重度主動脈瓣病變是心臟外科診療領域的一大難題,目前尚缺乏統一、普適且證據充分的外科治療策略[1]。機械瓣膜置換術后患兒將面臨包括長期抗凝、假體-患者失匹配(prosthesis-patient mismatch,PPM)及遠期再手術等風險[2]。Ozaki手術雖在成人中展現出了理想的遠期效果,但該術式在兒童中的應用仍相對有限,且術后瓣膜的耐久性仍受到質疑[3-4]。主動脈瓣成形術(aortic valve plasty/repair,AVP)與自體肺動脈瓣移植術(Ross手術)可在主動脈瓣位保留具有生長能力的瓣膜,這對兒童患者甚為重要。現有臨床證據提示,AVP及Ross手術在兒童患者中均具有相對理想的矯治效果,但兩者的優劣性及選擇時機仍不明確[5-6]。本研究回顧性分析本中心兒童患者AVP與Ross手術的近中期結局,對比兩種術式的矯治效果差異。
1 資料與方法
1.1 臨床資料和分組
回顧性納入2019年1月—2023年9月于本中心行AVP或Ross手術的主動脈瓣重度病變患兒。患兒的主動脈瓣病變類型、程度及心臟合并畸形通過經胸超聲心動圖(transthoracic echocardiography,TTE)和心臟CT明確。納入標準:(1)于我院診斷為主動脈瓣重度狹窄或重度反流的未成年患者(年齡<18歲);(2)于我院行AVP或Ross手術,且術后于我院規律隨訪。根據不同手術方式,將患兒分為AVP組和Ross手術組。
1.2 手術方法
策略選擇:所有患兒均以正中開胸入路,經由主動脈及上下腔靜脈插管建立體外循環,并通過右上肺靜脈置入左心引流管,隨后通過主動脈根部或冠狀動脈(冠脈)開口直接灌注心臟停搏液停跳心臟。在切開主動脈后,主刀醫師將對主動脈瓣進行探查,并結合循證證據及個人判斷綜合評估主動脈瓣修復成功的可能性及修復后的預期耐久性,隨后在AVP及Ross手術間進行策略選擇。
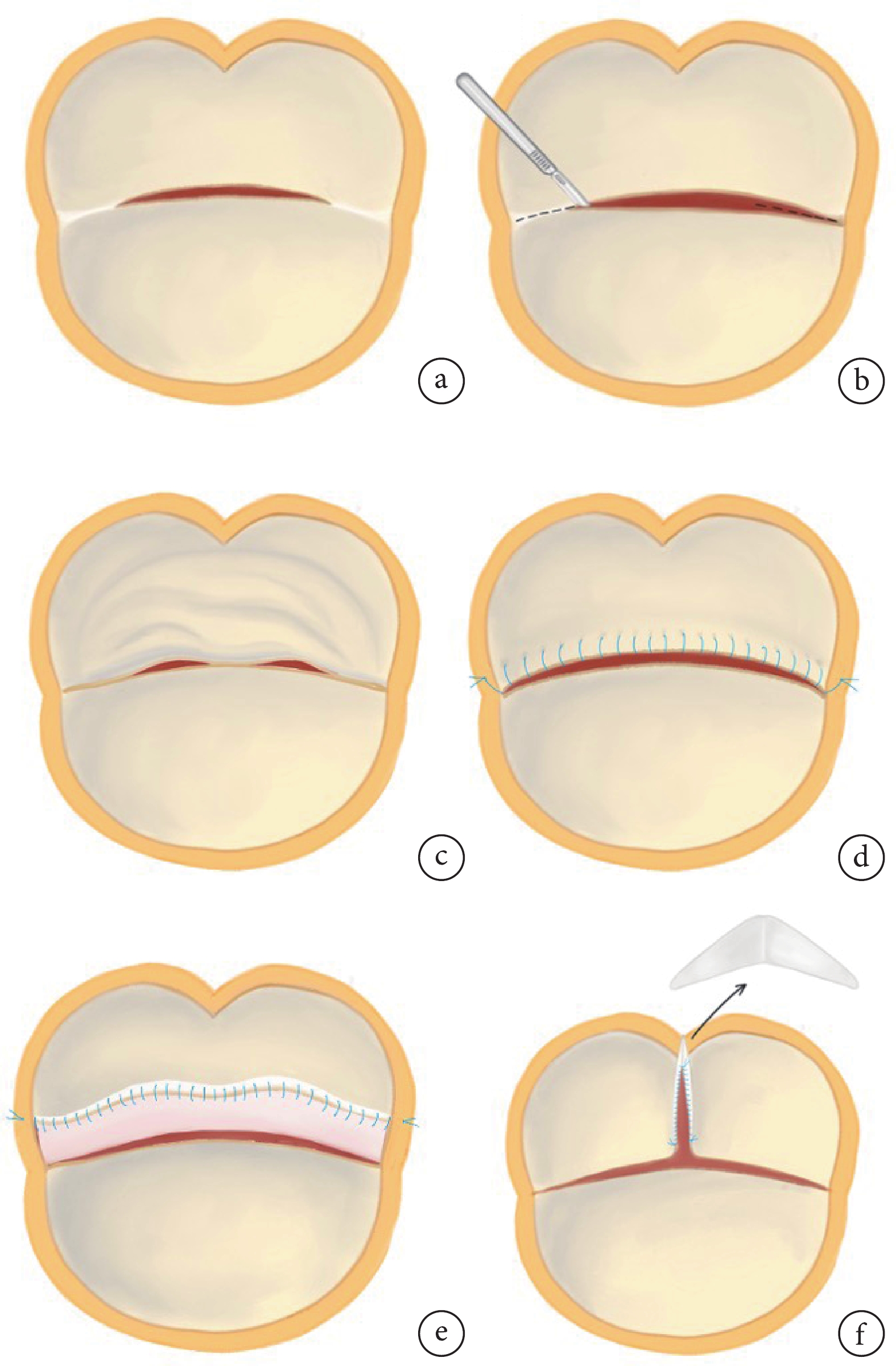
AVP:需要特別指出的是,對于主動脈瓣二葉式畸形(bicuspid aortic valve,BAV)患者,我們的修復理念與既往文獻[7-8]報道一致。總體來說,在AVP術中,本中心采取的主要策略如下:(1)瓣葉削薄:針對瓣葉增厚、鈣化的部分,將剝離/剔除增生的纖維組織及鈣化斑塊,在削減瓣葉厚度的同時改善瓣葉的活動度;(2)交界切開:當瓣葉對合緣存在融合/粘連時,常選擇切開融合部分,以改善瓣葉活動度(圖1a~b);(3)交界懸吊:當瓣葉冗長并發生脫垂時(常見于BAV及室間隔缺損的患兒中),常選擇以6-0/7-0 Prolene縫線于瓣葉游離緣進行連續縫合,并將縫線懸吊固定于瓣葉游離緣對應的主動脈壁上(圖1c~d),此種策略可在對冗余瓣葉組織進行折疊的同時提升瓣葉對合高度,進而改善瓣葉脫垂;(4)瓣葉延展:當瓣葉對合高度不足時(或在BAV患兒中行融合嵴切開轉三葉化修復時),常選取合適大小的自體/牛心包補片縫合于瓣葉游離緣(圖1e~f),延展瓣葉組織,增加對合高度;(5)單瓣葉重建:當患兒存在局限于單瓣葉的病變但修復困難或預期修復后耐久性較差時,可選擇切除病變的瓣葉,隨后以戊二醛處理的自體心包進行單瓣葉重建。
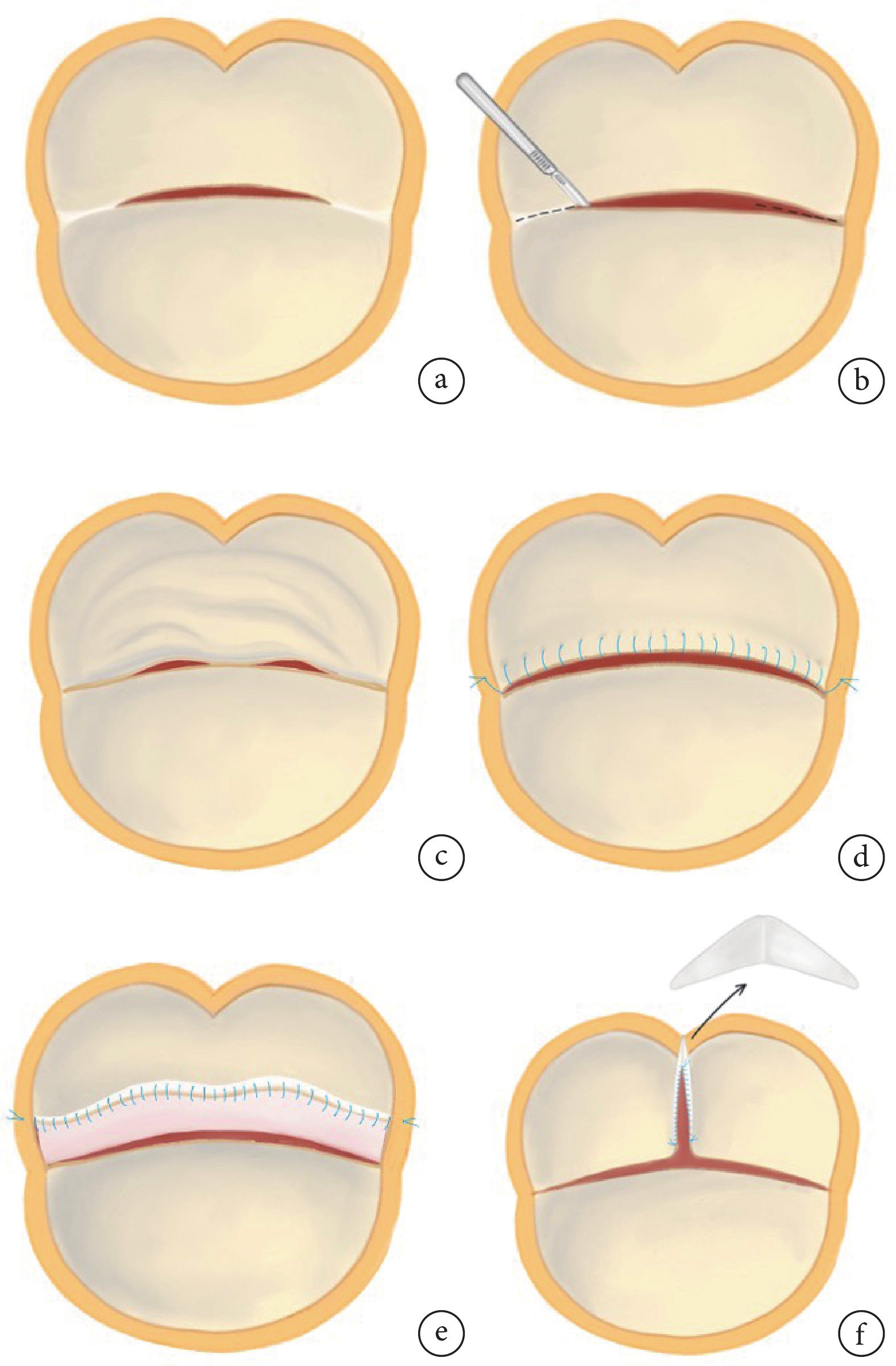 圖1
主動脈瓣成形策略
圖1
主動脈瓣成形策略
a:主動脈瓣二葉式畸形伴瓣葉交界區融合;b:交界融合切開;c:主動脈瓣二葉式畸形伴瓣葉冗長、脫垂;d:交界懸吊:以Prolene縫線于瓣葉游離緣行連續縫合,并將縫線懸吊固定于瓣葉游離緣對應的主動脈壁上,以此在折疊冗長瓣葉的同時提升對合高度;e:主動脈瓣二葉式畸形伴瓣葉短小、對合不良,取心包補片連續縫合于瓣葉游離緣,延展短小的瓣葉;f:主動脈瓣二葉式畸形轉三葉化修復中,切開融合嵴后,取合適大小“三角巾”形補片延展瓣葉對合緣
Ross手術:本中心所采用的Ross手術策略與既往文獻[9-11]報道的類似或一致。總體來說,主要策略如下:(1)根部置換策略:切除病變的主動脈瓣及原主動脈根部,同時獲取冠脈紐扣;隨后切取自體肺動脈帶瓣管道并以連續/間斷縫合的方式再植入主動脈瓣位,并將冠脈紐扣再植于新主動脈上;(2)冠脈下再植策略:切除病變的主動脈瓣;切取自體肺動脈帶瓣管道,連續縫合將自體肺動脈帶瓣管道近端再植進入原主動脈根部左心室流出道內;隨后修剪冠脈開口處對應的肺動脈壁組織,并以連續縫合的方式固定遠端;(3)外部加固策略:在根部置換策略的基礎上,為降低遠期新主動脈根部擴張的風險,常選取牛心包條/Gore-Tex補片作為加固材料,通過連續縫合使加固材料環抱于新主動脈根部外側。在右心室流出道重建方面,本中心共有3種材料選擇,即同種異體帶瓣管道、Gore-Tex帶瓣管道及牛頸靜脈帶瓣管道,其中以前兩者最為常用。
術后效果評價:在心臟復跳后,通過經食管超聲心動圖(transesophageal echocardiography,TEE)評估術后即刻的主動脈瓣功能,并依據TEE結果將術后效果分為“滿意”與“次滿意”兩類。“滿意”的術后效果定義為TEE測定的主動脈瓣峰值壓差<35 mm Hg(1 mm Hg=0.133 kPa),且反流程度為輕度及以下[12];反之則定義為“次滿意”效果。將“主動脈瓣病變復發”定義為:患兒術后隨訪期間復發中度及以上主動脈瓣反流,或術后出現主動脈瓣峰值流速>3.0 m/s,或患兒因主動脈瓣病變接受再次手術。
1.3 資料收集
患者的術前資料包括:TTE、心電圖及心臟CT檢查結果等。手術資料包括:手術時間、體外循環時間、主動脈阻斷時間、手術策略及術后即刻TEE檢查結果等;術后住院期間及隨訪期間的資料包括:住重癥監護室(intensive care unit,ICU)時間、死亡、再手術、心功能分級、心電圖及TTE檢查等。
1.4 統計學分析
統計學分析及統計圖繪制采用以SPSS 29.0及R語言(版本4.3.1)。選擇Q-Q圖及Shapiro-Wilk檢驗評價連續變量的正態性,若為正態分布,則以均數±標準差(x±s)描述,組間比較采用獨立樣本t檢驗;若為非正態分布,則以中位數(上下四分位數)[M(P25,P75)]描述,組間比較采用Wilcoxon秩和檢驗。分類變量以頻數及百分比(%)描述,組間比較采用χ2檢驗或Fisher確切概率法。采用Kaplan-Meier生存分析及log-rank檢驗比較兩組再手術及主動脈瓣病變復發的風險。以Cox回歸模型進行AVP組主動脈瓣病變復發的危險因素分析。雙側P≤0.05為差異有統計學意義。
1.5 倫理審查
本研究由四川大學華西醫院倫理委員會審批通過,審批號:2024年審(1172)號。
2 結果
2.1 基線資料
共納入48例患兒,其中男28例、女20例,平均年齡(9.3±4.5)歲。AVP組25例,Ross手術組23例。兩組患兒年齡、性別及術前紐約心臟協會(New York Heart Association,NYHA)心功能分級、既往手術史、術前TTE指標差異無統計學意義(P均>0.05)。AVP組患兒術前合并BAV的比例顯著低于Ross手術組(48.0% vs. 78.3%,P=0.031);且兩組術前主動脈瓣病變類型亦存在顯著差異,其中AVP組以主動脈瓣反流性病變為主[16/25(64.0%)],而Ross手術組則以狹窄性病變為主[11/23(47.8%)](P=0.037);見表1。
2.2 手術資料
AVP組的體外循環時間及主動脈阻斷時間均短于Ross手術組(P均<0.001)。AVP組最常用的成形策略為瓣葉削薄[15/25(60.0%)]及瓣葉延展[10/25(40.0%)]。術后共有22例(88.0%)患兒的即刻矯治效果評價為滿意,3例(12.0%)評價為次滿意的患兒均存在術后即刻輕-中度主動脈瓣反流,但前向血流均未見明顯加速。AVP組共有17例(68.0%)患兒接受了同期手術矯治,其中VSD修補及左心室流出道疏通最為常見且均為7例次。Ross手術組最常用的策略為根部置換[12/23(52.2%)]。右心室流出道最常用的重建材料為同種異體帶瓣管道,共10例(43.5%)患兒以同種異體肺動脈帶瓣管道進行重建,1例(4.3%)患兒以同種異體主動脈瓣管道進行重建。Ross術后所有患兒的即刻矯治效果評價均為滿意。Ross手術組共有8例(34.8%)患兒接受了同期手術矯治,其中3例(13.0%)患兒同期行Konno手術;見表2~3。
2.3 隨訪資料
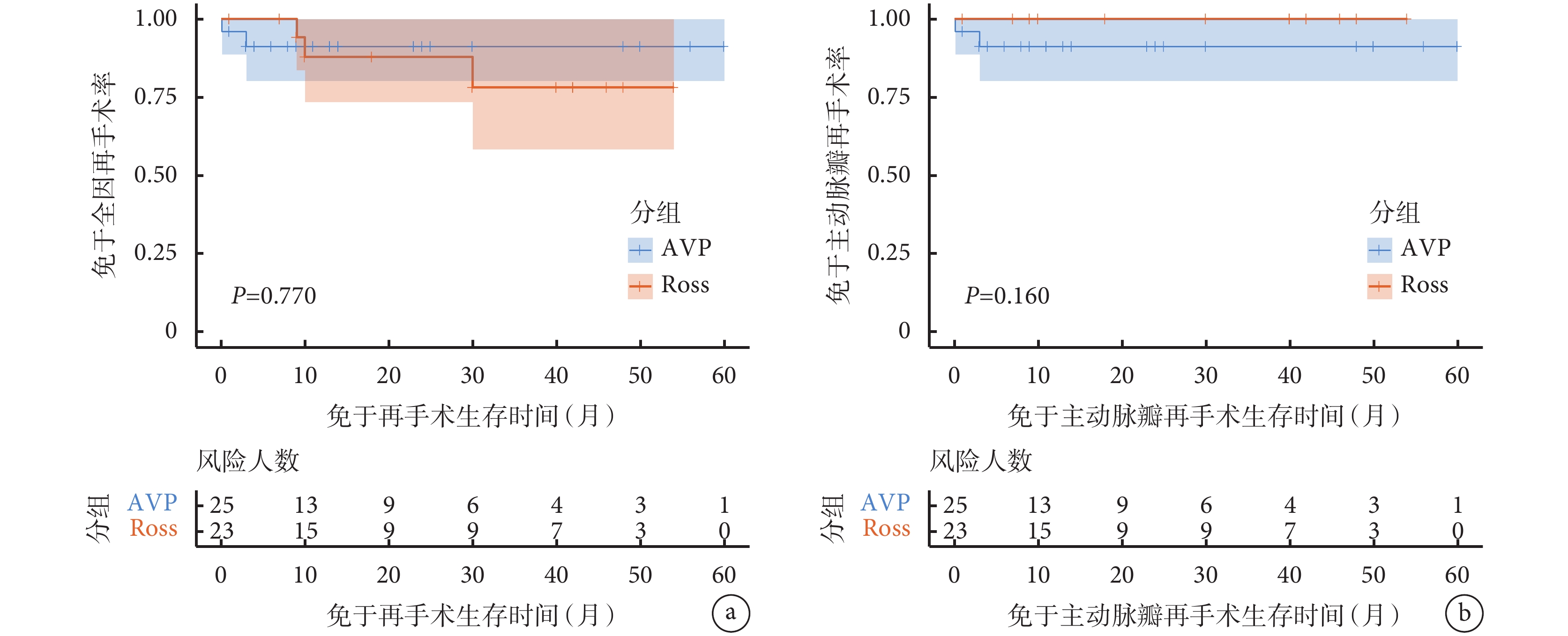
兩組患兒術后住院期間及出院后隨訪資料見表4。兩組患兒術后住ICU時間差異無統計學意義(P=0.676)。兩組術后均無需體外膜肺氧合輔助及永久起搏器植入,AVP組1例(4.0%)患兒因術后出血行再次開胸探查,術后無患兒發生住院期間死亡。全組中位隨訪時間為16.0(7.0,30.0)個月,兩組隨訪時間差異無統計學意義(P=0.469)。兩組患者的術后NYHA心功能分級均較術前顯著改善,且兩組間近似(P=0.095)。AVP組患兒術后中位主動脈瓣峰值流速為2.0(1.4,2.9)m/s,共有5例(20.0%)患兒術后主動脈瓣峰值流速>3.0 m/s;Ross手術組患兒術后中位主動脈瓣峰值流速為1.2(1.0,1.5)m/s(P<0.001),Ross手術組無患兒術后主動脈瓣峰值流速>3.0 m/s(P=0.073)。AVP組共有7例(28.0%)患兒術后復發中度及以上主動脈瓣反流,Ross手術組僅1例(4.3%)(P=0.127)。AVP組有2例(8.0%)患兒接受再次手術,分別于術后3 d及3個月分別行再次AVP及主動脈瓣置換;Ross手術組有3例(13.0%)患兒接受再次手術,分別于術后9個月、10個月及30個月行右心室流出道帶瓣管道置換。兩組患兒免于全因再手術及主動脈瓣再手術生存曲線見圖2。Log-rank檢驗結果提示兩組差異均無統計學意義(P=0.770,0.160)。
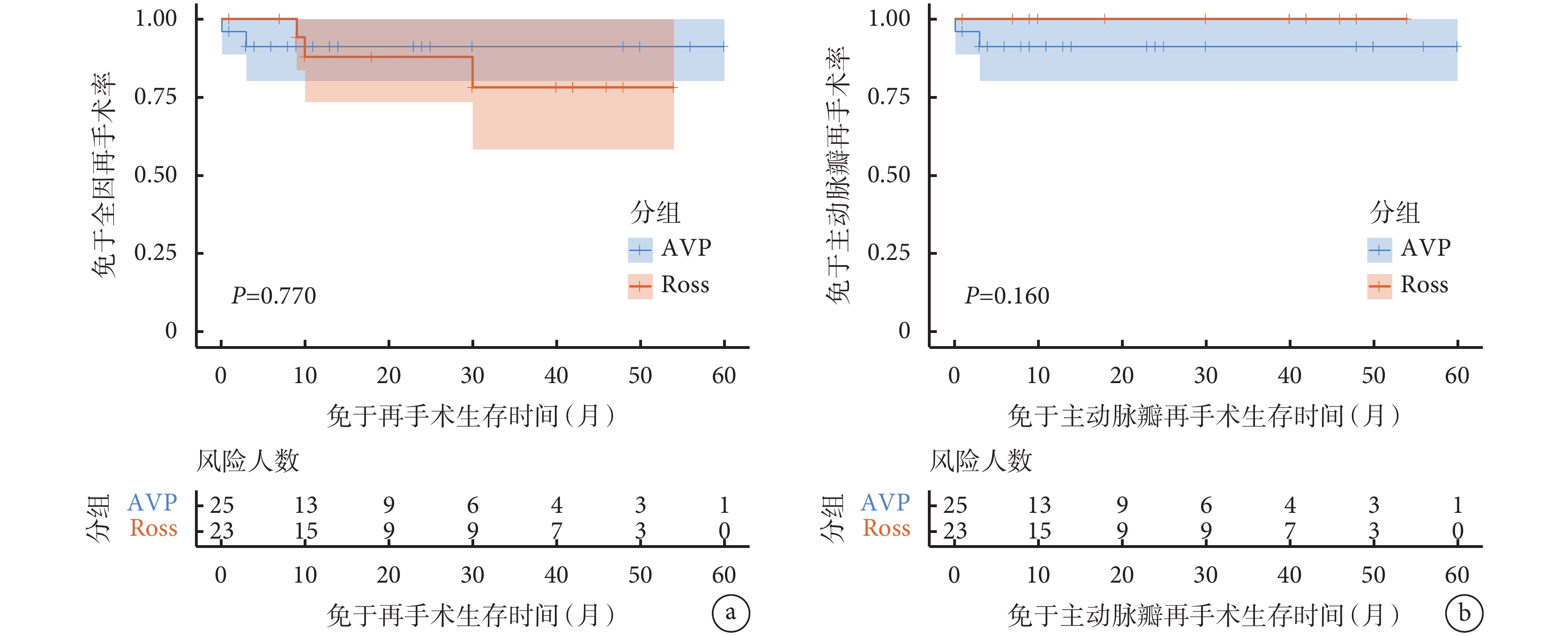 圖2
兩組免于再手術生存曲線
圖2
兩組免于再手術生存曲線
a:AVP組與Ross手術組免于全因再手術生存曲線;b:AVP組與Ross手術組免于主動脈瓣再手術生存曲線;AVP:主動脈瓣成形術
AVP組共有13例(52.0%)患兒主動脈瓣病變復發,而Ross手術組僅1例(4.3%)。兩組患兒免于主動脈瓣病變復發生存差異有統計學意義(log-rank檢驗P<0.001);見圖3。針對AVP組存在主動脈瓣病變復發的患兒,利用Cox回歸模型進行主動脈瓣病變復發的危險因素分析,納入的指標包括:年齡(是否>5歲)、性別、是否為BAV、術前主動脈瓣病變類型、是否具有既往心臟手術史、成形策略是否使用補片及術后即刻主動脈瓣功能狀況是否滿意,分析結果并未發現明確的主動脈瓣病變復發的危險因素;見表5。
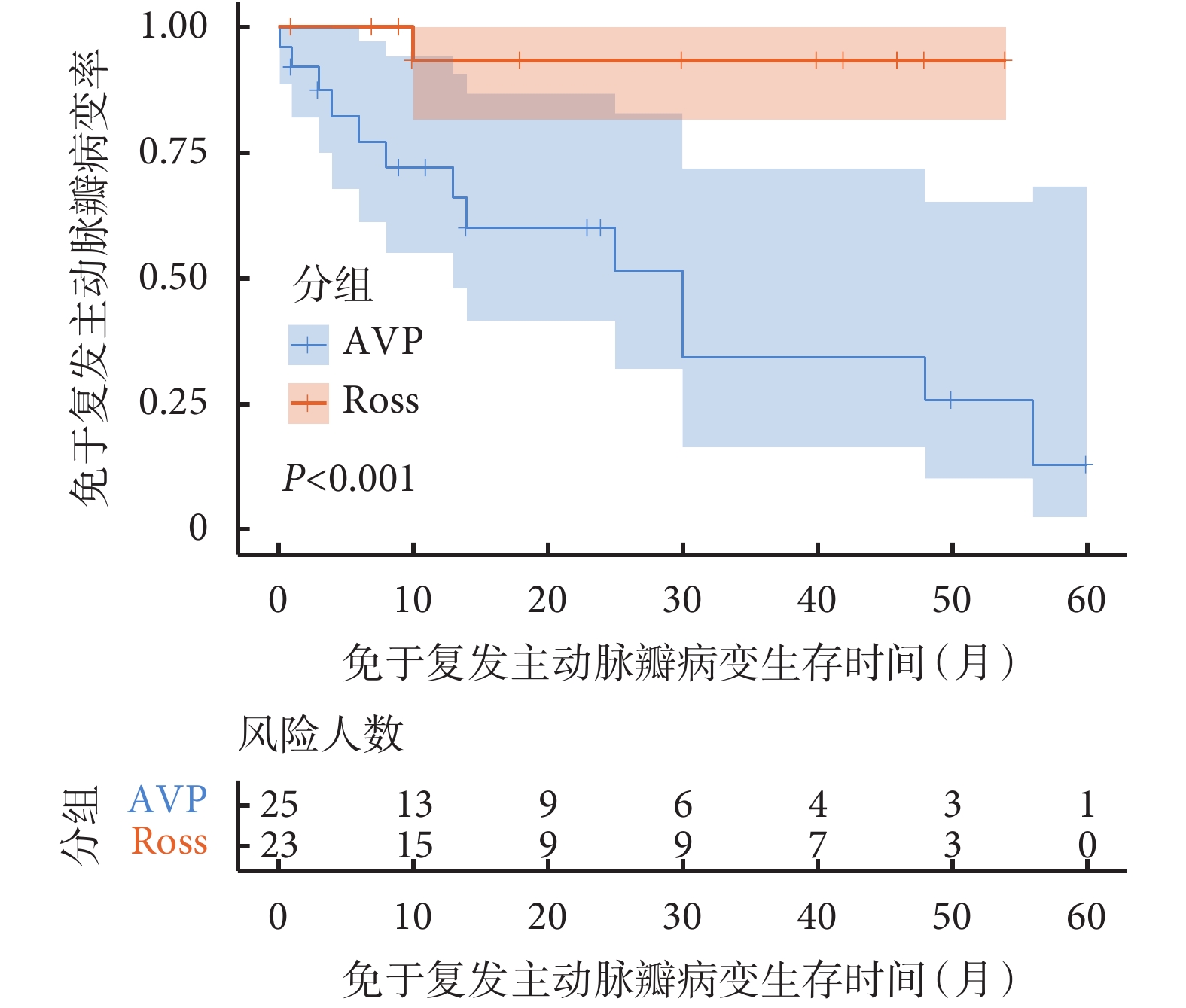 圖3
AVP組與Ross手術組免于主動脈瓣病變復發生存曲線
圖3
AVP組與Ross手術組免于主動脈瓣病變復發生存曲線
AVP:主動脈瓣成形術
3 討論
兒童重度主動脈瓣病變診治是心臟外科領域的一大挑戰,外科矯治的主要目的為改善患兒癥狀并盡可能避免或延緩人工瓣膜置換及再次手術;同時外科矯治需兼顧手術效果的持續性及術后主動脈瓣的生長能力,目前尚缺乏一致的外科矯治理念及普適的外科矯治策略[1]。主動脈瓣置換并非是患兒的優良選擇,機械瓣置換術后患兒需面臨長期抗凝、瓣膜功能障礙、PPM及再手術的風險,而生物瓣置換術后患兒則需面對瓣膜衰敗、PPM及多次再手術的問題[1-2, 13]。同種異體主動脈瓣置換目前在國內鮮有應用,但現有的小樣本臨床證據提示仍有40%~50%的患兒需在遠期接受主動脈瓣再次手術[14-16]。Ozaki手術選擇利用自體心包組織重建主動脈瓣,其已在成年患者中展現出了相對理想的遠期效果[3]。但Ozaki手術在兒童中的應用證據有限,雖術后短期內結局相對理想,但近-中期結果已展現出了令人憂慮的耐久性問題,有研究[4, 14]指出,3年內20%的患兒需接受再次手術。AVP及Ross手術是目前僅有的兩種能在主動脈瓣位保留瓣膜生長能力的手術方式,目前的臨床證據提示,兩種手術方式均在兒童患者中具有相對理想的術后效果,但兩種手術方式的直接效果比較及選擇優先性尚不明晰[1, 5-6]。
AVP在兒童中的矯治效果近來得到穩步提升,使其在主動脈瓣病變患兒中的應用愈發積極且廣泛[17]。在嬰幼兒患者中,相比于主動脈瓣球囊擴張而言,AVP在具有同等安全性的同時,術后遠期免于主動脈瓣再手術率更高[18]。AVP的成形理念及手術策略較為復雜且多變,其在BAV患兒中尤其如此[5, 7-8]。AVP的主要手術策略包括:瓣葉削薄、交界切開、交界懸吊/折疊、瓣葉延展及單瓣葉重建等。在納入的患者中,我們所采用的主要AVP策略包括瓣葉削薄[15/25(60.0%)]、瓣葉延展[10/25(40.0%)]及交界切開[5/25(20.0%)],這與Schlein等[5]所報道的以交界切開和瓣葉修補/延展為主要策略的AVP策略一致。在需使用補片的AVP中,我們選擇的補片材料包括了自體心包組織及牛心包組織;如選擇自體心包組織,我們通常將以0.6%的戊二醛溶液處理2~10 min,這與目前的報道一致[19]。但需要指出的是,有學者[8, 12]并不主張在AVP過程中激進地使用補片進行瓣葉重建,因為有研究指出補片的使用是影響AVP耐久度的重要危險因素。AVP組無患兒發生圍術期死亡,2例(8.0%)于隨訪期間行再手術,這與Schlein等[5]及Zhu等[20]所報道的結果近似。但AVP組共有13例(52.0%)患兒存在主動脈瓣病變復發,因此中期隨訪時間內潛在需要再手術的患兒可能較多。
既往研究[5, 8, 12, 20]指出,低齡(年齡<1歲)、主動脈瓣狹窄性病變、主動脈瓣單瓣化畸形、使用補片重建及“次滿意”的即刻術后效果等是AVP術后主動脈瓣病變復發及再手術的危險因素,其中以低齡及使用補片重建證據相對充分。但在本研究中,Cox回歸模型并未發現顯著的主動脈瓣病變復發的危險因素,其中低齡及使用補片重建的風險比(hazard ratio,HR)及95%CI分別為0.61(0.13,2.80)及0.96(0.14,6.72)。我們推測Cox回歸模型的陰性結果可能與較小的樣本量及復雜的混雜因素相關。
近年來,Ross手術在成年患者中優異的遠期結局使其迎來了復興,其在兒童甚至嬰幼兒中的應用亦愈發廣泛[21-23]。但需要指出的是,低齡仍是Ross手術圍術期死亡的重要危險因素,相比>1歲患兒,嬰幼兒Ross手術的圍術期死亡率明顯偏高(17% vs. 0%)[1, 23]。本研究所納入的Ross手術患兒的平均年齡為(10.1±3.9)歲,最小年齡為2歲。在手術策略方面,根部置換及冠脈下再植在兒童中的應用最為廣泛,這與我們的選擇一致,但具體策略的選擇與不同術者的習慣及偏好相關[23-24]。在自體肺動脈瓣的吻合方式方面,有術者選擇以連續縫合的方式進行吻合,另有術者選擇以類似瓣膜置換的間斷縫合方式進行吻合,關于兩種吻合方法優劣性及術后效果的探索尚匱乏;由于術者習慣及偏好的差異,本中心兩種吻合策略均有使用。在右心室流出道重建方面,同種異體帶瓣管道是國際上右心室流出道重建的最主要選擇[23-24],這亦與我們的策略一致;但因國內同種異體帶瓣管道的獲得較為困難,人工帶瓣管道等材料的選擇可能更多[25],本中心以Gore-Tex帶瓣管道作為人工管道的首選,針對少部分患者選擇以牛頸靜脈帶瓣管道進行重建。在隨訪期間,尚無患兒出現主動脈根部瘤樣擴張,無患兒的主動脈瓣峰值流速>3.0 m/s;中位主動脈瓣峰值流速為1.2(1.0,1.5)m/s,僅1例患兒復發中度主動脈瓣反流,這與Murin等[24]報道的結果一致。共3例(13.0%)患兒于隨訪期間行再次手術,這高于Murin等[24]、Ivanov等[6]所報道的結果。3例再手術均為右心室流出道帶瓣管道置換,再手術的原因均為帶瓣管道鈣化及瓣膜功能異常,其中2例為牛頸靜脈帶瓣管道(術后9個月及10個月再手術),1例為Gore-Tex帶瓣管道(術后30個月再手術)。我們注意到牛頸靜脈帶瓣管道的鈣化速度似乎較快,這與國內目前的經驗相似[25],出于對該種材料耐久性的顧慮,目前我們已不再選擇其作為右心室流出道的重建選擇。
兒童患者中AVP與Ross手術的效果優劣性及選擇優先性尚存爭議,目前相關的高質量臨床證據尚較為有限[1]。來自墨爾本皇家兒童醫院的研究[20]顯示,AVP術后患兒的遠期生存率更優(93.9% vs. 80.9%,P=0.04),但免于再手術率組間差異無統計學意義(45.7% vs. 48.5%,P=0.29),不過AVP組免于主動脈瓣再手術率較Ross手術組更低(45.7% vs. 70.7%,P<0.01)。上述研究結果提示,AVP或許應作為主動脈瓣重度病變患兒的初始手術方案(遠期生存更優),而Ross手術作為AVP術后主動脈瓣病變復發的再手術選擇。在需使用補片的復雜AVP中,有研究[26]提示,復雜AVP術后患兒遠期生存率與Ross手術組相當(94.1% vs. 91.0%,P=0.89),且遠期總體再手術率亦近似(50.1% vs. 69%,P=0.32)。該研究結果亦支持復雜AVP可作為主動脈瓣病變患兒的初始治療選擇,不必擔憂補片使用所帶來的劣性結局。本研究結果表明AVP及Ross手術在兒童中具有同等的安全性,兩組術后嚴重不良事件發生率差異無統計學意義;兩組均無患兒發生隨訪期間死亡,且近中期全因再手術率及主動脈瓣再手術率相似(8.0% vs. 13.0%,P=0.922;8.0% vs. 0.0%,P=0.266),這與上述研究[20, 26]的結果近似。但從主動脈瓣病變復發的角度分析,AVP術后主動脈瓣病變復發率顯著更高(52.0% vs. 4.3%,P<0.001),該差異提示所納入AVP組患兒的中期及遠期結局可能劣于Ross手術組患兒,這有待進一步觀察確認,且亦需在更大的樣本量上進行證實及危險因素分析。我們推測相對更不滿意的術后即刻主動脈瓣功能及瓣葉延展材料的固有缺陷可能是AVP組術后主動脈瓣病變復發比例更高的原因,但其有待進一步證實。
本研究存在局限:(1)本研究樣本量較小且隨訪時間較短,研究結論有待在更大樣本量及更長隨訪時間的研究中進一步明確;(2)本研究中納入患者的AVP及Ross手術的理念及策略具有一定的中心特色,可能無法代表整體的矯治理念及策略,因此研究結論的外推可能受限;(3)本研究中AVP組存在主動脈瓣病變復發的患者比例較高,但危險因素分析未見陽性結果,其有待在大樣本研究中進一步探索。
綜上,AVP及Ross手術在兒童中具有同等的圍術期安全性,術后隨訪期間生存率及總體再手術率近似。AVP組術后主動脈瓣病變復發率較Ross手術組更高,其具體原因仍有待進一步研究確認。我們目前支持將AVP及Ross手術作為主動脈瓣重度病變患兒的初始外科矯治方式的理念,但具體的策略選擇應依據患者的病情進行個體化制定。
利益沖突:無。
作者貢獻:謝林、吳鑄衡、劉靖宇及賃可負責研究的選題及設計;謝林、吳鑄衡及劉靖宇負責數據收集、統計分析,文章寫作及修改;賃可對文章、圖片及統計結果進行核對、審校和修訂。
兒童重度主動脈瓣病變是心臟外科診療領域的一大難題,目前尚缺乏統一、普適且證據充分的外科治療策略[1]。機械瓣膜置換術后患兒將面臨包括長期抗凝、假體-患者失匹配(prosthesis-patient mismatch,PPM)及遠期再手術等風險[2]。Ozaki手術雖在成人中展現出了理想的遠期效果,但該術式在兒童中的應用仍相對有限,且術后瓣膜的耐久性仍受到質疑[3-4]。主動脈瓣成形術(aortic valve plasty/repair,AVP)與自體肺動脈瓣移植術(Ross手術)可在主動脈瓣位保留具有生長能力的瓣膜,這對兒童患者甚為重要。現有臨床證據提示,AVP及Ross手術在兒童患者中均具有相對理想的矯治效果,但兩者的優劣性及選擇時機仍不明確[5-6]。本研究回顧性分析本中心兒童患者AVP與Ross手術的近中期結局,對比兩種術式的矯治效果差異。
1 資料與方法
1.1 臨床資料和分組
回顧性納入2019年1月—2023年9月于本中心行AVP或Ross手術的主動脈瓣重度病變患兒。患兒的主動脈瓣病變類型、程度及心臟合并畸形通過經胸超聲心動圖(transthoracic echocardiography,TTE)和心臟CT明確。納入標準:(1)于我院診斷為主動脈瓣重度狹窄或重度反流的未成年患者(年齡<18歲);(2)于我院行AVP或Ross手術,且術后于我院規律隨訪。根據不同手術方式,將患兒分為AVP組和Ross手術組。
1.2 手術方法
策略選擇:所有患兒均以正中開胸入路,經由主動脈及上下腔靜脈插管建立體外循環,并通過右上肺靜脈置入左心引流管,隨后通過主動脈根部或冠狀動脈(冠脈)開口直接灌注心臟停搏液停跳心臟。在切開主動脈后,主刀醫師將對主動脈瓣進行探查,并結合循證證據及個人判斷綜合評估主動脈瓣修復成功的可能性及修復后的預期耐久性,隨后在AVP及Ross手術間進行策略選擇。
AVP:需要特別指出的是,對于主動脈瓣二葉式畸形(bicuspid aortic valve,BAV)患者,我們的修復理念與既往文獻[7-8]報道一致。總體來說,在AVP術中,本中心采取的主要策略如下:(1)瓣葉削薄:針對瓣葉增厚、鈣化的部分,將剝離/剔除增生的纖維組織及鈣化斑塊,在削減瓣葉厚度的同時改善瓣葉的活動度;(2)交界切開:當瓣葉對合緣存在融合/粘連時,常選擇切開融合部分,以改善瓣葉活動度(圖1a~b);(3)交界懸吊:當瓣葉冗長并發生脫垂時(常見于BAV及室間隔缺損的患兒中),常選擇以6-0/7-0 Prolene縫線于瓣葉游離緣進行連續縫合,并將縫線懸吊固定于瓣葉游離緣對應的主動脈壁上(圖1c~d),此種策略可在對冗余瓣葉組織進行折疊的同時提升瓣葉對合高度,進而改善瓣葉脫垂;(4)瓣葉延展:當瓣葉對合高度不足時(或在BAV患兒中行融合嵴切開轉三葉化修復時),常選取合適大小的自體/牛心包補片縫合于瓣葉游離緣(圖1e~f),延展瓣葉組織,增加對合高度;(5)單瓣葉重建:當患兒存在局限于單瓣葉的病變但修復困難或預期修復后耐久性較差時,可選擇切除病變的瓣葉,隨后以戊二醛處理的自體心包進行單瓣葉重建。
 圖1
主動脈瓣成形策略
圖1
主動脈瓣成形策略
a:主動脈瓣二葉式畸形伴瓣葉交界區融合;b:交界融合切開;c:主動脈瓣二葉式畸形伴瓣葉冗長、脫垂;d:交界懸吊:以Prolene縫線于瓣葉游離緣行連續縫合,并將縫線懸吊固定于瓣葉游離緣對應的主動脈壁上,以此在折疊冗長瓣葉的同時提升對合高度;e:主動脈瓣二葉式畸形伴瓣葉短小、對合不良,取心包補片連續縫合于瓣葉游離緣,延展短小的瓣葉;f:主動脈瓣二葉式畸形轉三葉化修復中,切開融合嵴后,取合適大小“三角巾”形補片延展瓣葉對合緣
Ross手術:本中心所采用的Ross手術策略與既往文獻[9-11]報道的類似或一致。總體來說,主要策略如下:(1)根部置換策略:切除病變的主動脈瓣及原主動脈根部,同時獲取冠脈紐扣;隨后切取自體肺動脈帶瓣管道并以連續/間斷縫合的方式再植入主動脈瓣位,并將冠脈紐扣再植于新主動脈上;(2)冠脈下再植策略:切除病變的主動脈瓣;切取自體肺動脈帶瓣管道,連續縫合將自體肺動脈帶瓣管道近端再植進入原主動脈根部左心室流出道內;隨后修剪冠脈開口處對應的肺動脈壁組織,并以連續縫合的方式固定遠端;(3)外部加固策略:在根部置換策略的基礎上,為降低遠期新主動脈根部擴張的風險,常選取牛心包條/Gore-Tex補片作為加固材料,通過連續縫合使加固材料環抱于新主動脈根部外側。在右心室流出道重建方面,本中心共有3種材料選擇,即同種異體帶瓣管道、Gore-Tex帶瓣管道及牛頸靜脈帶瓣管道,其中以前兩者最為常用。
術后效果評價:在心臟復跳后,通過經食管超聲心動圖(transesophageal echocardiography,TEE)評估術后即刻的主動脈瓣功能,并依據TEE結果將術后效果分為“滿意”與“次滿意”兩類。“滿意”的術后效果定義為TEE測定的主動脈瓣峰值壓差<35 mm Hg(1 mm Hg=0.133 kPa),且反流程度為輕度及以下[12];反之則定義為“次滿意”效果。將“主動脈瓣病變復發”定義為:患兒術后隨訪期間復發中度及以上主動脈瓣反流,或術后出現主動脈瓣峰值流速>3.0 m/s,或患兒因主動脈瓣病變接受再次手術。
1.3 資料收集
患者的術前資料包括:TTE、心電圖及心臟CT檢查結果等。手術資料包括:手術時間、體外循環時間、主動脈阻斷時間、手術策略及術后即刻TEE檢查結果等;術后住院期間及隨訪期間的資料包括:住重癥監護室(intensive care unit,ICU)時間、死亡、再手術、心功能分級、心電圖及TTE檢查等。
1.4 統計學分析
統計學分析及統計圖繪制采用以SPSS 29.0及R語言(版本4.3.1)。選擇Q-Q圖及Shapiro-Wilk檢驗評價連續變量的正態性,若為正態分布,則以均數±標準差(x±s)描述,組間比較采用獨立樣本t檢驗;若為非正態分布,則以中位數(上下四分位數)[M(P25,P75)]描述,組間比較采用Wilcoxon秩和檢驗。分類變量以頻數及百分比(%)描述,組間比較采用χ2檢驗或Fisher確切概率法。采用Kaplan-Meier生存分析及log-rank檢驗比較兩組再手術及主動脈瓣病變復發的風險。以Cox回歸模型進行AVP組主動脈瓣病變復發的危險因素分析。雙側P≤0.05為差異有統計學意義。
1.5 倫理審查
本研究由四川大學華西醫院倫理委員會審批通過,審批號:2024年審(1172)號。
2 結果
2.1 基線資料
共納入48例患兒,其中男28例、女20例,平均年齡(9.3±4.5)歲。AVP組25例,Ross手術組23例。兩組患兒年齡、性別及術前紐約心臟協會(New York Heart Association,NYHA)心功能分級、既往手術史、術前TTE指標差異無統計學意義(P均>0.05)。AVP組患兒術前合并BAV的比例顯著低于Ross手術組(48.0% vs. 78.3%,P=0.031);且兩組術前主動脈瓣病變類型亦存在顯著差異,其中AVP組以主動脈瓣反流性病變為主[16/25(64.0%)],而Ross手術組則以狹窄性病變為主[11/23(47.8%)](P=0.037);見表1。
2.2 手術資料
AVP組的體外循環時間及主動脈阻斷時間均短于Ross手術組(P均<0.001)。AVP組最常用的成形策略為瓣葉削薄[15/25(60.0%)]及瓣葉延展[10/25(40.0%)]。術后共有22例(88.0%)患兒的即刻矯治效果評價為滿意,3例(12.0%)評價為次滿意的患兒均存在術后即刻輕-中度主動脈瓣反流,但前向血流均未見明顯加速。AVP組共有17例(68.0%)患兒接受了同期手術矯治,其中VSD修補及左心室流出道疏通最為常見且均為7例次。Ross手術組最常用的策略為根部置換[12/23(52.2%)]。右心室流出道最常用的重建材料為同種異體帶瓣管道,共10例(43.5%)患兒以同種異體肺動脈帶瓣管道進行重建,1例(4.3%)患兒以同種異體主動脈瓣管道進行重建。Ross術后所有患兒的即刻矯治效果評價均為滿意。Ross手術組共有8例(34.8%)患兒接受了同期手術矯治,其中3例(13.0%)患兒同期行Konno手術;見表2~3。
2.3 隨訪資料
兩組患兒術后住院期間及出院后隨訪資料見表4。兩組患兒術后住ICU時間差異無統計學意義(P=0.676)。兩組術后均無需體外膜肺氧合輔助及永久起搏器植入,AVP組1例(4.0%)患兒因術后出血行再次開胸探查,術后無患兒發生住院期間死亡。全組中位隨訪時間為16.0(7.0,30.0)個月,兩組隨訪時間差異無統計學意義(P=0.469)。兩組患者的術后NYHA心功能分級均較術前顯著改善,且兩組間近似(P=0.095)。AVP組患兒術后中位主動脈瓣峰值流速為2.0(1.4,2.9)m/s,共有5例(20.0%)患兒術后主動脈瓣峰值流速>3.0 m/s;Ross手術組患兒術后中位主動脈瓣峰值流速為1.2(1.0,1.5)m/s(P<0.001),Ross手術組無患兒術后主動脈瓣峰值流速>3.0 m/s(P=0.073)。AVP組共有7例(28.0%)患兒術后復發中度及以上主動脈瓣反流,Ross手術組僅1例(4.3%)(P=0.127)。AVP組有2例(8.0%)患兒接受再次手術,分別于術后3 d及3個月分別行再次AVP及主動脈瓣置換;Ross手術組有3例(13.0%)患兒接受再次手術,分別于術后9個月、10個月及30個月行右心室流出道帶瓣管道置換。兩組患兒免于全因再手術及主動脈瓣再手術生存曲線見圖2。Log-rank檢驗結果提示兩組差異均無統計學意義(P=0.770,0.160)。
 圖2
兩組免于再手術生存曲線
圖2
兩組免于再手術生存曲線
a:AVP組與Ross手術組免于全因再手術生存曲線;b:AVP組與Ross手術組免于主動脈瓣再手術生存曲線;AVP:主動脈瓣成形術
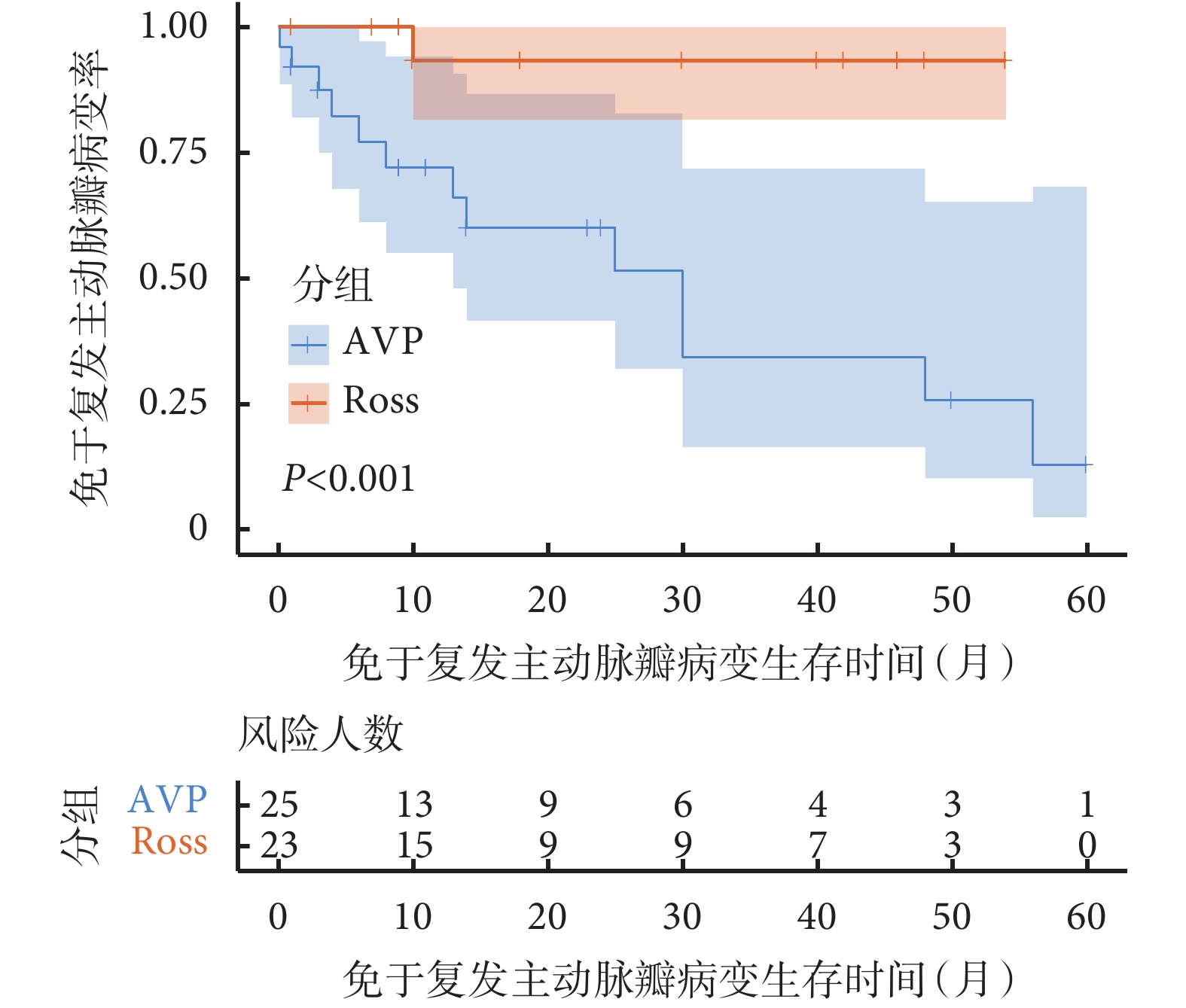
AVP組共有13例(52.0%)患兒主動脈瓣病變復發,而Ross手術組僅1例(4.3%)。兩組患兒免于主動脈瓣病變復發生存差異有統計學意義(log-rank檢驗P<0.001);見圖3。針對AVP組存在主動脈瓣病變復發的患兒,利用Cox回歸模型進行主動脈瓣病變復發的危險因素分析,納入的指標包括:年齡(是否>5歲)、性別、是否為BAV、術前主動脈瓣病變類型、是否具有既往心臟手術史、成形策略是否使用補片及術后即刻主動脈瓣功能狀況是否滿意,分析結果并未發現明確的主動脈瓣病變復發的危險因素;見表5。
 圖3
AVP組與Ross手術組免于主動脈瓣病變復發生存曲線
圖3
AVP組與Ross手術組免于主動脈瓣病變復發生存曲線
AVP:主動脈瓣成形術
3 討論
兒童重度主動脈瓣病變診治是心臟外科領域的一大挑戰,外科矯治的主要目的為改善患兒癥狀并盡可能避免或延緩人工瓣膜置換及再次手術;同時外科矯治需兼顧手術效果的持續性及術后主動脈瓣的生長能力,目前尚缺乏一致的外科矯治理念及普適的外科矯治策略[1]。主動脈瓣置換并非是患兒的優良選擇,機械瓣置換術后患兒需面臨長期抗凝、瓣膜功能障礙、PPM及再手術的風險,而生物瓣置換術后患兒則需面對瓣膜衰敗、PPM及多次再手術的問題[1-2, 13]。同種異體主動脈瓣置換目前在國內鮮有應用,但現有的小樣本臨床證據提示仍有40%~50%的患兒需在遠期接受主動脈瓣再次手術[14-16]。Ozaki手術選擇利用自體心包組織重建主動脈瓣,其已在成年患者中展現出了相對理想的遠期效果[3]。但Ozaki手術在兒童中的應用證據有限,雖術后短期內結局相對理想,但近-中期結果已展現出了令人憂慮的耐久性問題,有研究[4, 14]指出,3年內20%的患兒需接受再次手術。AVP及Ross手術是目前僅有的兩種能在主動脈瓣位保留瓣膜生長能力的手術方式,目前的臨床證據提示,兩種手術方式均在兒童患者中具有相對理想的術后效果,但兩種手術方式的直接效果比較及選擇優先性尚不明晰[1, 5-6]。
AVP在兒童中的矯治效果近來得到穩步提升,使其在主動脈瓣病變患兒中的應用愈發積極且廣泛[17]。在嬰幼兒患者中,相比于主動脈瓣球囊擴張而言,AVP在具有同等安全性的同時,術后遠期免于主動脈瓣再手術率更高[18]。AVP的成形理念及手術策略較為復雜且多變,其在BAV患兒中尤其如此[5, 7-8]。AVP的主要手術策略包括:瓣葉削薄、交界切開、交界懸吊/折疊、瓣葉延展及單瓣葉重建等。在納入的患者中,我們所采用的主要AVP策略包括瓣葉削薄[15/25(60.0%)]、瓣葉延展[10/25(40.0%)]及交界切開[5/25(20.0%)],這與Schlein等[5]所報道的以交界切開和瓣葉修補/延展為主要策略的AVP策略一致。在需使用補片的AVP中,我們選擇的補片材料包括了自體心包組織及牛心包組織;如選擇自體心包組織,我們通常將以0.6%的戊二醛溶液處理2~10 min,這與目前的報道一致[19]。但需要指出的是,有學者[8, 12]并不主張在AVP過程中激進地使用補片進行瓣葉重建,因為有研究指出補片的使用是影響AVP耐久度的重要危險因素。AVP組無患兒發生圍術期死亡,2例(8.0%)于隨訪期間行再手術,這與Schlein等[5]及Zhu等[20]所報道的結果近似。但AVP組共有13例(52.0%)患兒存在主動脈瓣病變復發,因此中期隨訪時間內潛在需要再手術的患兒可能較多。
既往研究[5, 8, 12, 20]指出,低齡(年齡<1歲)、主動脈瓣狹窄性病變、主動脈瓣單瓣化畸形、使用補片重建及“次滿意”的即刻術后效果等是AVP術后主動脈瓣病變復發及再手術的危險因素,其中以低齡及使用補片重建證據相對充分。但在本研究中,Cox回歸模型并未發現顯著的主動脈瓣病變復發的危險因素,其中低齡及使用補片重建的風險比(hazard ratio,HR)及95%CI分別為0.61(0.13,2.80)及0.96(0.14,6.72)。我們推測Cox回歸模型的陰性結果可能與較小的樣本量及復雜的混雜因素相關。
近年來,Ross手術在成年患者中優異的遠期結局使其迎來了復興,其在兒童甚至嬰幼兒中的應用亦愈發廣泛[21-23]。但需要指出的是,低齡仍是Ross手術圍術期死亡的重要危險因素,相比>1歲患兒,嬰幼兒Ross手術的圍術期死亡率明顯偏高(17% vs. 0%)[1, 23]。本研究所納入的Ross手術患兒的平均年齡為(10.1±3.9)歲,最小年齡為2歲。在手術策略方面,根部置換及冠脈下再植在兒童中的應用最為廣泛,這與我們的選擇一致,但具體策略的選擇與不同術者的習慣及偏好相關[23-24]。在自體肺動脈瓣的吻合方式方面,有術者選擇以連續縫合的方式進行吻合,另有術者選擇以類似瓣膜置換的間斷縫合方式進行吻合,關于兩種吻合方法優劣性及術后效果的探索尚匱乏;由于術者習慣及偏好的差異,本中心兩種吻合策略均有使用。在右心室流出道重建方面,同種異體帶瓣管道是國際上右心室流出道重建的最主要選擇[23-24],這亦與我們的策略一致;但因國內同種異體帶瓣管道的獲得較為困難,人工帶瓣管道等材料的選擇可能更多[25],本中心以Gore-Tex帶瓣管道作為人工管道的首選,針對少部分患者選擇以牛頸靜脈帶瓣管道進行重建。在隨訪期間,尚無患兒出現主動脈根部瘤樣擴張,無患兒的主動脈瓣峰值流速>3.0 m/s;中位主動脈瓣峰值流速為1.2(1.0,1.5)m/s,僅1例患兒復發中度主動脈瓣反流,這與Murin等[24]報道的結果一致。共3例(13.0%)患兒于隨訪期間行再次手術,這高于Murin等[24]、Ivanov等[6]所報道的結果。3例再手術均為右心室流出道帶瓣管道置換,再手術的原因均為帶瓣管道鈣化及瓣膜功能異常,其中2例為牛頸靜脈帶瓣管道(術后9個月及10個月再手術),1例為Gore-Tex帶瓣管道(術后30個月再手術)。我們注意到牛頸靜脈帶瓣管道的鈣化速度似乎較快,這與國內目前的經驗相似[25],出于對該種材料耐久性的顧慮,目前我們已不再選擇其作為右心室流出道的重建選擇。
兒童患者中AVP與Ross手術的效果優劣性及選擇優先性尚存爭議,目前相關的高質量臨床證據尚較為有限[1]。來自墨爾本皇家兒童醫院的研究[20]顯示,AVP術后患兒的遠期生存率更優(93.9% vs. 80.9%,P=0.04),但免于再手術率組間差異無統計學意義(45.7% vs. 48.5%,P=0.29),不過AVP組免于主動脈瓣再手術率較Ross手術組更低(45.7% vs. 70.7%,P<0.01)。上述研究結果提示,AVP或許應作為主動脈瓣重度病變患兒的初始手術方案(遠期生存更優),而Ross手術作為AVP術后主動脈瓣病變復發的再手術選擇。在需使用補片的復雜AVP中,有研究[26]提示,復雜AVP術后患兒遠期生存率與Ross手術組相當(94.1% vs. 91.0%,P=0.89),且遠期總體再手術率亦近似(50.1% vs. 69%,P=0.32)。該研究結果亦支持復雜AVP可作為主動脈瓣病變患兒的初始治療選擇,不必擔憂補片使用所帶來的劣性結局。本研究結果表明AVP及Ross手術在兒童中具有同等的安全性,兩組術后嚴重不良事件發生率差異無統計學意義;兩組均無患兒發生隨訪期間死亡,且近中期全因再手術率及主動脈瓣再手術率相似(8.0% vs. 13.0%,P=0.922;8.0% vs. 0.0%,P=0.266),這與上述研究[20, 26]的結果近似。但從主動脈瓣病變復發的角度分析,AVP術后主動脈瓣病變復發率顯著更高(52.0% vs. 4.3%,P<0.001),該差異提示所納入AVP組患兒的中期及遠期結局可能劣于Ross手術組患兒,這有待進一步觀察確認,且亦需在更大的樣本量上進行證實及危險因素分析。我們推測相對更不滿意的術后即刻主動脈瓣功能及瓣葉延展材料的固有缺陷可能是AVP組術后主動脈瓣病變復發比例更高的原因,但其有待進一步證實。
本研究存在局限:(1)本研究樣本量較小且隨訪時間較短,研究結論有待在更大樣本量及更長隨訪時間的研究中進一步明確;(2)本研究中納入患者的AVP及Ross手術的理念及策略具有一定的中心特色,可能無法代表整體的矯治理念及策略,因此研究結論的外推可能受限;(3)本研究中AVP組存在主動脈瓣病變復發的患者比例較高,但危險因素分析未見陽性結果,其有待在大樣本研究中進一步探索。
綜上,AVP及Ross手術在兒童中具有同等的圍術期安全性,術后隨訪期間生存率及總體再手術率近似。AVP組術后主動脈瓣病變復發率較Ross手術組更高,其具體原因仍有待進一步研究確認。我們目前支持將AVP及Ross手術作為主動脈瓣重度病變患兒的初始外科矯治方式的理念,但具體的策略選擇應依據患者的病情進行個體化制定。
利益沖突:無。
作者貢獻:謝林、吳鑄衡、劉靖宇及賃可負責研究的選題及設計;謝林、吳鑄衡及劉靖宇負責數據收集、統計分析,文章寫作及修改;賃可對文章、圖片及統計結果進行核對、審校和修訂。