縱隔腫瘤是縱隔內組織結構腫瘤性改變的統稱,是胸外科常見病,包括胸腺瘤、神經源性腫瘤、畸胎瘤等[1-2]。縱隔內器官和組織解剖結構復雜且空間狹小,其周圍鄰近心臟及大血管等重要臟器。臨床上,手術通常是縱隔腫瘤的首選治療方法,患者大多預后較好[3-4]。20世紀以來,電視胸腔鏡技術發展迅速,大量病例證明,與經典胸骨正中切口或前外側肋間切口開胸入路相比,微創電視輔助胸腔鏡手術(video-assisted thoracoscopic surgery,VATS)具有切口小、創傷小、并發癥少、術后恢復快等優點[5]。目前,微創VATS已取代傳統開胸手術,廣泛應用于臨床縱隔相關疾病的治療。然而,傳統的電視胸腔鏡存在一些不可避免的缺陷,如二維景深、小空間(特別是上縱隔和胸膜頂病變處理能力不足)、縫合打結等操作困難等[6]。針對VATS的缺陷,開發了機器人輔助胸腔鏡手術。該機器人系統的優點是可以提供高達10-15倍放大的高分辨率三維視場,從而實現對縱隔結構細節的更清晰觀察[7]。同時,機器人輔助胸外科手術(robot-assisted thoracic surgery,RATS)可解決VATS帶來的手部生理性震顫,避免因手術失誤造成副損傷和意外傷害[8]。
多個研究[9-10]已經揭示了VATS或RATS治療縱隔腫瘤的可行性和安全性。但是這些研究都屬于小樣本量的單中心回顧性研究。在縱隔腫瘤的治療中,RATS能否達到與VATS相同甚至更好的手術效果尚不清楚。因此,本研究結合最新國內外文獻,進行全面的Meta分析,以期為臨床實踐提供更高水平的循證醫學證據。
1 資料與方法
1.1 納入與排除標準
1.1.1 納入標準
(1)研究類型:回顧性隊列研究或隨機對照試驗;(2)研究對象:診斷為縱隔腫瘤且符合手術指征的患者;(3)干預措施:RATS或VATS縱隔腫瘤手術;(4)結局指標:腫瘤大小、手術時間、術中出血量、中轉開胸率、術后引流時間、術后總并發癥發生率、術后住院時間等。
1.1.2 排除標準
(1)數據不完整或無法提供有用數據的研究;(2)非臨床比較性研究,如綜述、病例報告或單干預措施的研究;(3)重復發表或納入病例較少(≤10例)的研究。
1.2 檢索策略
對PubMed、EMbase、The Cochrane Library、Web of Science、萬方、CNKI、CBM、VIP數據庫進行系統、全面的文獻檢索,檢索時間為建庫至2024年3月31日。檢索比較RATS和VATS治療縱隔腫瘤臨床療效的相關文獻。中文檢索詞為:機器人輔助胸外科手術、機器人、機器人輔助、達芬奇、視頻輔助胸外科手術、視頻輔助、縱隔腫瘤、胸腺瘤、畸胎瘤、神經源性腫瘤。英文檢索詞為:robot-assisted thoracic surgery、robotic、robot-assisted、da Vinci、video-assisted thoracic surgery、video-assisted、mediastinal tumors、mediastinal neoplasms、mediastinum cancers、mediastinal cancer。以PubMed數據庫為例,檢索式如下:(("mediastinal tumors"[All Fields] OR "mediastinal neoplasms" [MeSH Terms] OR "mediastinum cancers"[All Fields] OR "mediastinal cancer"[All Fields])) AND ("robot-assisted thoracic surgery"[MeSH Terms] OR "robot-assisted"[All Fields] OR "da Vinci"[All Fields])) AND ("video-assisted thoracic surgery"[MeSH Terms] OR "video-assisted"[All Fields]))。
1.3 數據資料提取及質量評價方法
文獻檢索由兩名研究者獨立完成,并通過閱讀檢索文獻的標題和摘要來評估是否初步納入研究。在初步檢索完成后,閱讀檢索文獻的全文,以決定是否將其納入研究。對于有疑問或不同意見的研究,通過團隊討論來解決。研究提取內容包括:(1)作者、年份、樣本量、性別、年齡、干預措施、研究類型;(2)相結局指標:腫瘤大小、手術時間、術中出血量、中轉開胸率、術后總并發癥、術后引流時間、術后住院時間、住院費用。
采用紐卡斯爾-渥太華量表(Newcastle-Ottawa Scale,NOS)對納入研究進行質量評價,NOS包括3個項目:隊列的選擇、研究組間可比性和結果評估[11]。高質量研究定義為質量評分≥7分的研究。任何分歧均通過團隊討論解決。
1.4 統計學分析
使用 Review Manager 5.4軟件分別計算二分類變量資料和連續性變量資料的相對比值比(odds ratio,OR)和均數差(mean difference,MD)以及95%CI。研究間的異質性用Q檢驗和I2檢驗,若I2<50%,P>0.1,各研究間異質性不顯著,采用固定效應模型;若I2≥50%,P≤0.1,各研究間異質性顯著,采用隨機效應模型。通過敏感性分析檢驗Meta分析結果的穩定性,采用漏斗圖分析潛在的發表偏倚。
2 結果
2.1 文獻檢索結果
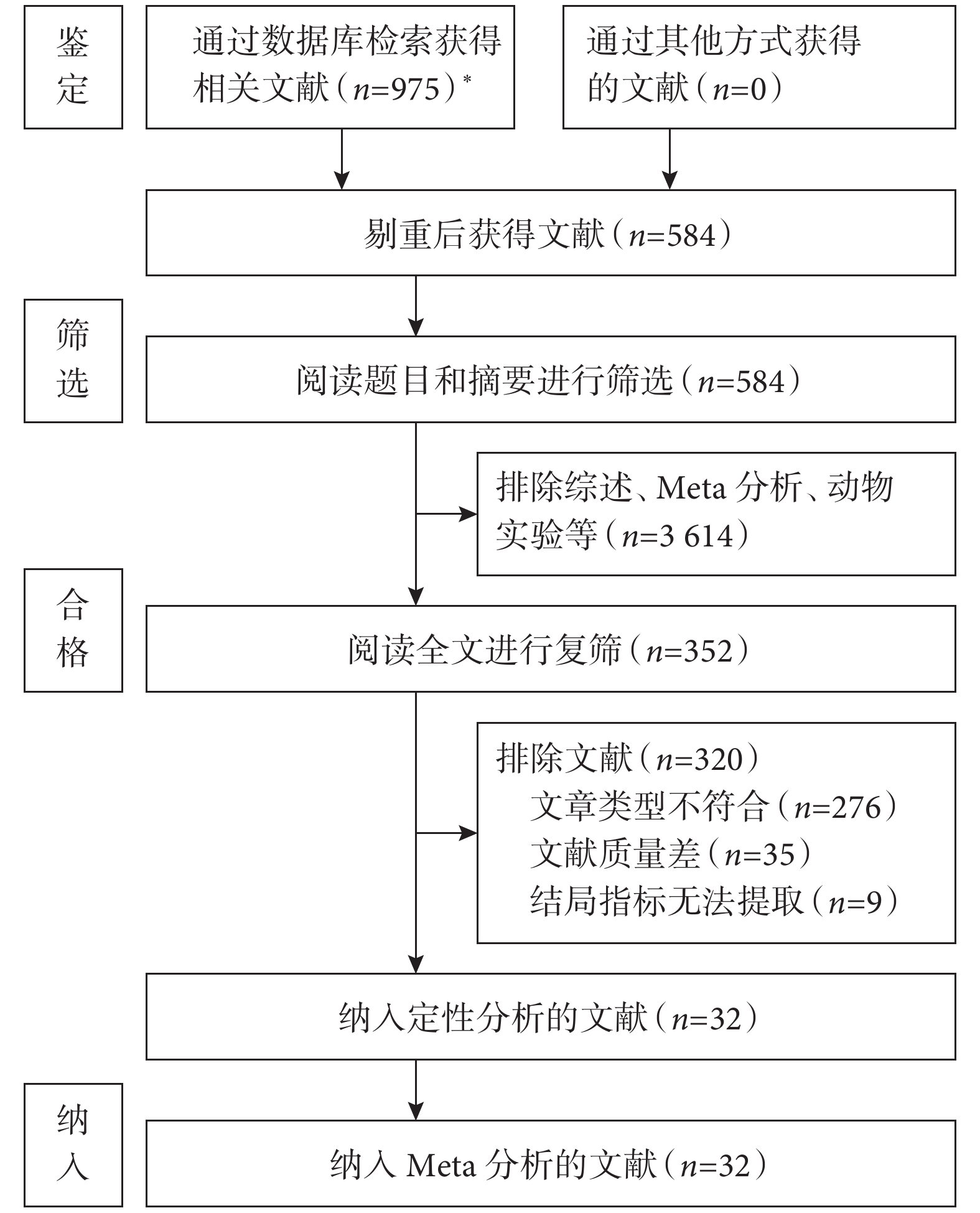
初步檢索共獲得文獻975篇,剔重后剩余584篇。通過閱讀題目和摘要排除232篇,進一步閱讀全文排除文獻320篇,最終納入32篇文獻[12-43]。文獻篩選流程見圖1。
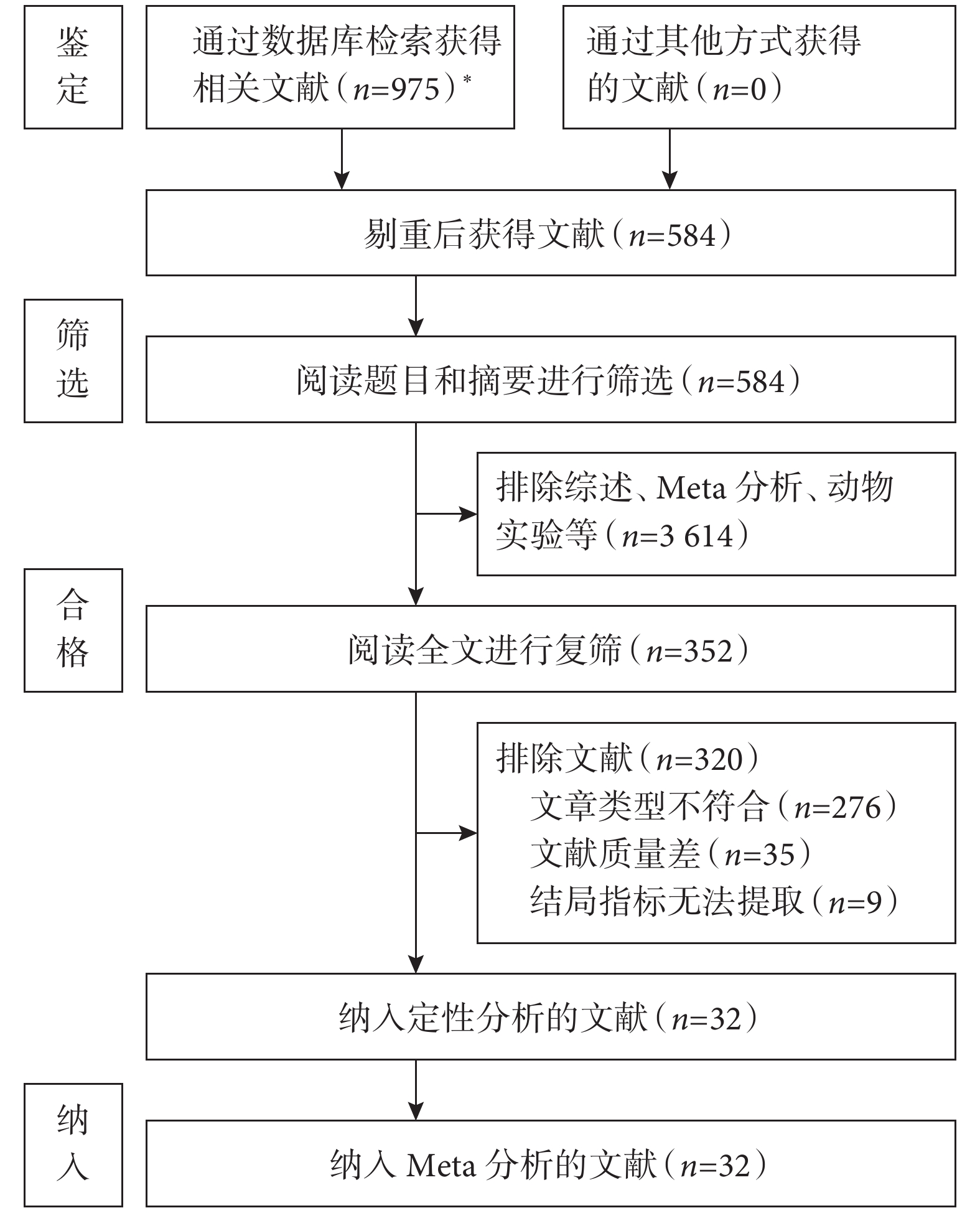 圖1
文獻篩選流程
圖1
文獻篩選流程
*:PubMed(
2.2 文獻基本特征
納入32篇文獻[12-43],共
2.3 Meta分析結果
2.3.1 腫瘤大小
納入22篇文獻[12-15,17,20-21,23,27-30,32-41],共
2.3.2 手術時間
納入28篇文獻[12-18,20-23,25-26,28-32,34-43],共
2.3.3 術中出血量
納入25篇文獻[12-15,17,21-23,25,28-43],共
2.3.4 中轉開胸率
納入10篇文獻[12,15,17,19,22,26,30,35,38,40],共
2.3.5 術后總并發癥
納入24篇文獻[12-13,15-18,20-22,25,28-30,32-35,37-43],共
2.3.6 術后引流時間
納入24篇文獻[12-15,17,18,20-23,28,30-35,37-43],共
2.3.7 術后住院時間
納入30篇文獻[12-24,27-43],共
2.3.8 住院費用
納入9篇文獻[16-17,21,30-31,34,38–40],共
2.4 亞組分析
為尋找研究間的異質性來源,根據各研究納入患者的國家將各指標分為中國組和其他國家組后進行亞組分析。結果顯示,在中國組中,各項指標與總體相比異質性無明顯變化,P值無顯著改變;在其他國家組中,術中出血量、術后并發癥、術后引流時間,住院費用的P值和總體相比有顯著變化,均表現為無統計學差異;見表3。
2.5 敏感性分析
分別采用固定和隨機效應模型分析中轉開胸率、術后總并發癥,結果無明顯差異。而對于腫瘤大小、手術時間、術中出血量、術后引流時間、術后住院時間、住院費用等指標,原始研究間異質性較大,對于這些指標進行敏感性分析,逐步排除一些研究直至研究間異質性為I2=0%,再分別使用隨機和固定效應模型驗證結果,結果無明顯變化,表明Meta分析結果穩定;見表4。
2.6 發表偏倚分析
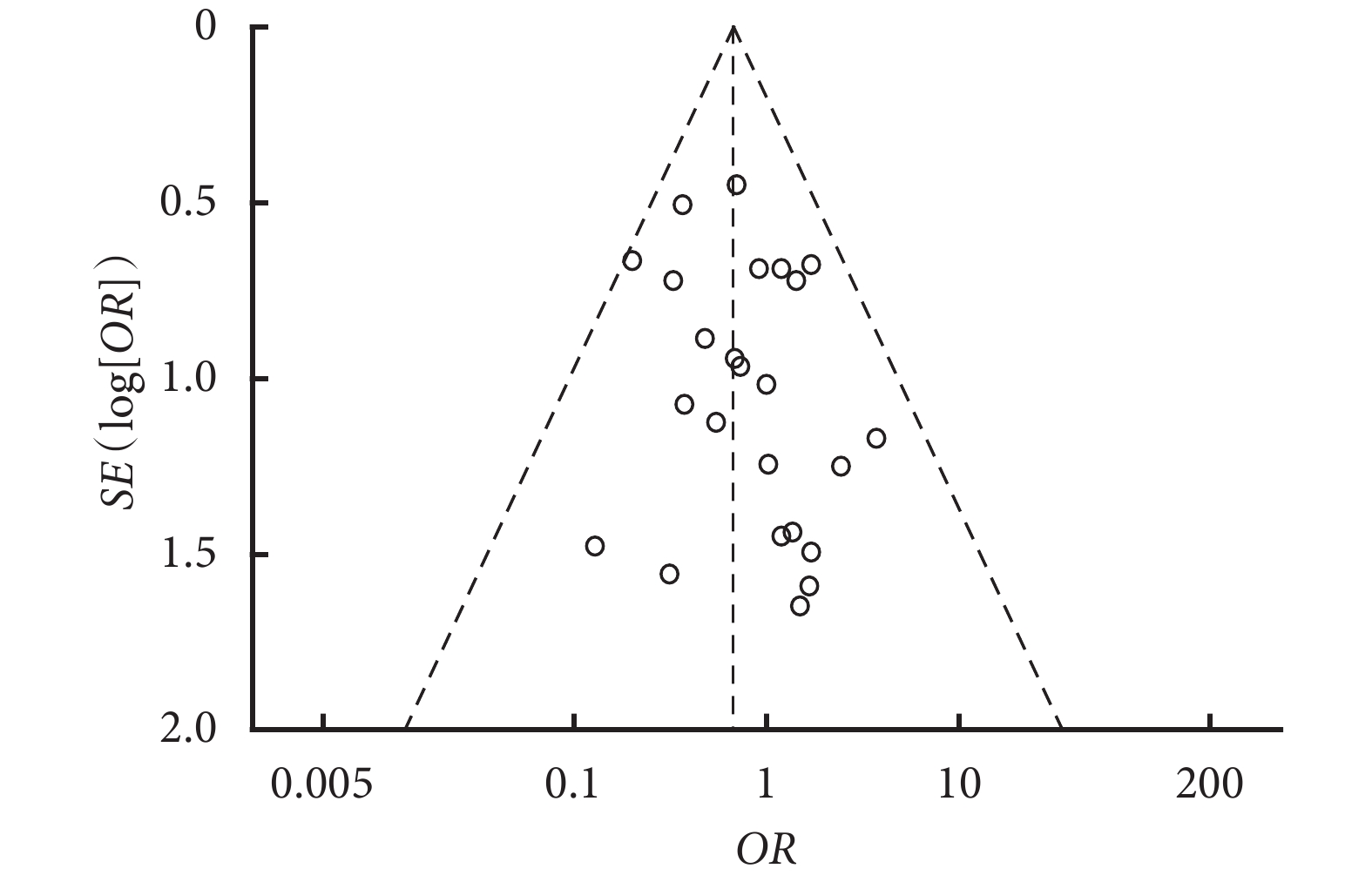
通過對各結局指標繪制漏斗圖,發現所有研究均均勻分布在漏斗圖的兩側,說明本研究的發表偏倚較小。以術后總并發癥發生率為例繪制的漏斗圖見圖2。
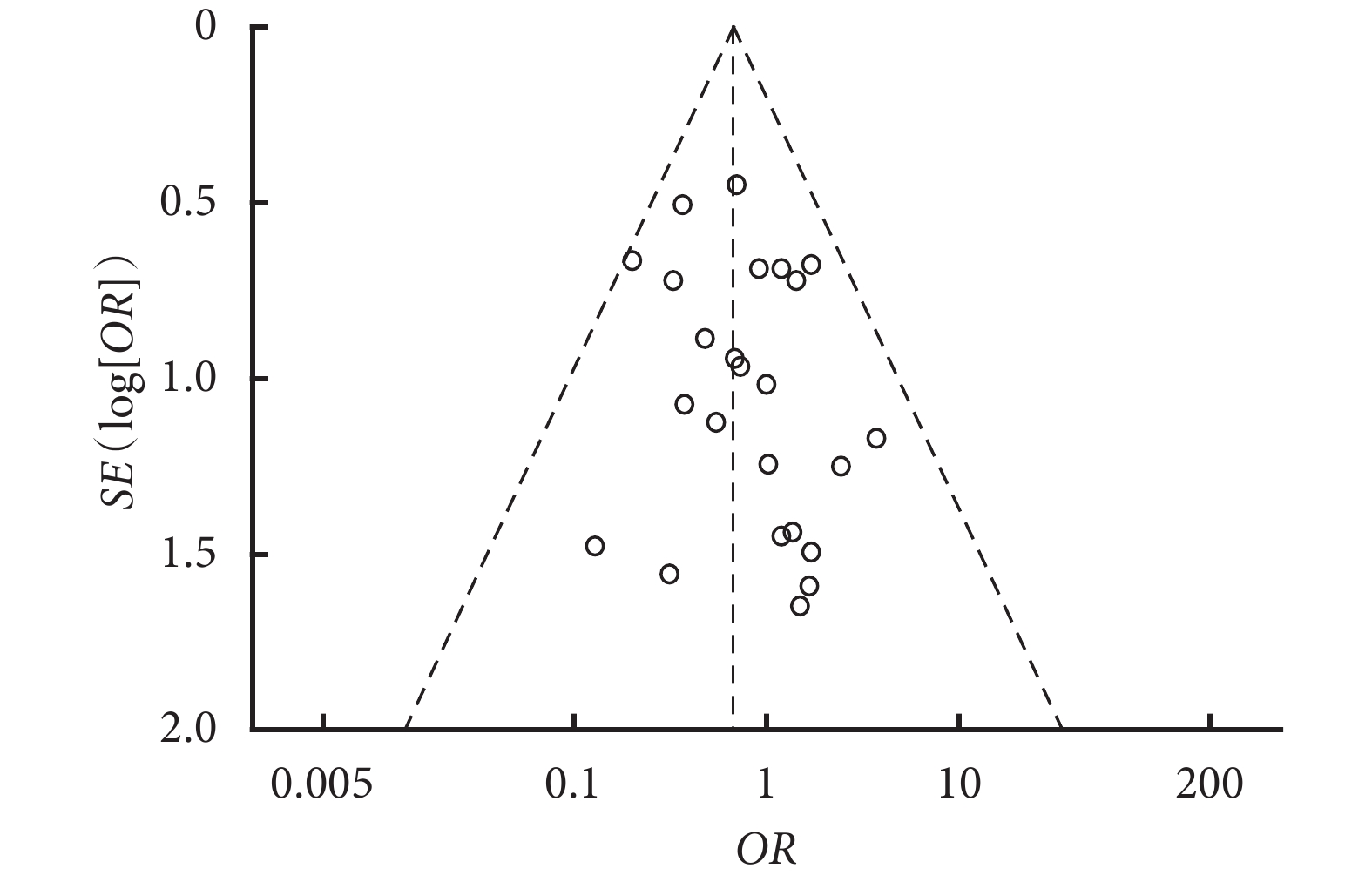 圖2
術后總并發癥發生率漏斗圖
圖2
術后總并發癥發生率漏斗圖
3 討論
縱隔的解剖結構較復雜且空間狹小,縱隔腫瘤組織來源多樣,鄰近心臟、大血管等重要臟器[44]。自2001年Yoshino等[45]報道世界上首例機器人縱隔腫瘤切除術以來,RATS已在一些大型醫療中心用于治療縱隔腫瘤。目前,微創手術發展迅速,RATS縱隔腫瘤切除術和VATS縱隔腫瘤切除術越來越多地被胸外科醫生選擇。然而,RATS在縱隔腫瘤切除方面是否優于VATS仍然存在爭議。因此,我們進行Meta分析,以比較和討論RATS和VATS治療縱隔腫瘤的有效性和安全性。
本Meta分析結果顯示,RATS組與VATS組患者的腫瘤大小差異不顯著,表明腫瘤的大小不會影響縱隔腫瘤切除術式的選擇。同樣,兩組患者在手術時間上的總體比較也無顯著差異。最初的一些研究[16]表明,RATS的手術時間通常相對較長,導致這種差異的原因可能是一些醫療中心開展機器人手術較晚,且受縱隔復雜解剖結構的影響,RATS在縱隔腫瘤的手術經驗不足,一些外科醫生的RATS學習曲線正處于緩慢的上升階段。然而,隨著近年來胸外科醫生縱隔手術經驗的積累和RATS手術操作熟練程度的提升,RATS的手術時間顯著縮短。
對比術中出血量,我們發現RATS組術中出血量明顯少于VATS組。這可能是因為RATS可以在手術中提供三維放大視圖,更靈活的操作,消除手部震顫,從而準確暴露切除靶點周圍復雜的解剖結構[2]。這有助于醫生在手術過程中精確地實施手術,更好地控制小血管出血。
在中轉開胸率方面,RATS組比VATS組更有優勢。中轉開胸手術多是由于RATS或VATS術中發現較復雜的情況,如腫瘤位置、大小等與預期不符或腫瘤已侵入到周圍組織血管以及發生胸膜粘連,需要中轉開胸以更好地處理腫瘤。RATS組中轉開胸率低于VATS組可能得益于RATS手術的高三維視野,可全面觀察腫瘤情況并實施更精細的手術操作,從而減少中轉開胸的可能性[46]。然而,需要注意的是,雖然RATS組中轉開胸率低于VATS組,但RATS轉開胸不如VATS方便。
術后并發癥是評價術后短期療效的重要指標。本研究結果顯示,RATS組術后并發癥總體發生率低于VATS組。主要原因如下:(1)與VATS相比,RATS術后恢復更快,并發癥風險明顯降低。(2)RATS提高了術者手術的舒適度,有助于在堅持安全、無腫瘤、微創的基礎上,提高腫瘤的全切率、前縱隔脂肪組織切除的徹底性等,從而降低術后并發癥發生率。在臨床實踐中,我們也發現RATS在解剖前縱隔脂肪和脂肪組織方面更有優勢。RATS可提供更完整、精確的腫瘤解剖,從而更好地保護縱隔腫瘤膜的完整性。
術后引流時間方面,Meta分析結果顯示,RATS組短于VATS組。我們認為這可能是RATS在手術精準度上比VATS更具優勢。RATS為手術過程提供更精確的三維視野,可準確評估腫瘤大小,切除腫瘤和組織更完整,減少了小血管的損傷且止血比較徹底,從而減少周圍組織的刺激因素,使術后引流量顯著減少。同時,在前縱隔腫瘤手術中,縱隔周圍區域的脂肪組織也隨腫瘤完全切除,減少了術后炎癥反應,術后引流量即相對減少。上述因素均使RATS組術后引流量減少,從而縮短術后引流時間。
對于術后住院時間,Meta分析結果表明,RATS組患者的術后住院時間比VATS組患者短。我們考慮這是因為RATS比VATS更具微創性,術后給患者帶來的創傷相對較小,因此患者術后疼痛較輕,恢復更快,在一定程度上縮短了術后住院時間,這也符合快速康復的理念[47]。
關于術后住院費用,Meta分析結果顯示,RATS組的術后住院費用普遍較高。我們分析其主要原因是RATS手術設備和技術較新,相比傳統腔鏡較復雜,手術時間相對較長,這在一定程度上增加了術后住院費用。
亞組分析結果顯示,中國組的研究是總體研究異質性的主要來源;其他國家在一些指標的統計學差異可能是國內外RATS開展時間和發展水平差異導致的。手術時間、術中出血量等原始研究間異質性較大,可能與腫瘤類型有關,納入的文獻中包括前縱隔腫瘤、中縱隔腫瘤和后縱隔腫瘤,不同部位的縱膈腫瘤手術難度和手術入路可能不同,導致手術時間不同。同時,不同醫院的手術水平存在差異導致手術時間與術中出血量也存在差異,并且患者年齡和性別對術中出血量也有影響。
本Meta分析的局限性:(1)醫院成本存在顯著異質性,這可能是由于不同醫療中心的RATS收費標準不同所致;(2)納入的研究都是回顧性臨床研究,選擇偏倚在所難免,需要大樣本的隨機對照試驗進行驗證;(3)目前缺乏兩類手術的長期隨訪數據,我們希望在未來進一步完善這一數據;(4)本研究沒有對縱隔腫瘤的位置進行更詳細的比較,可能導致結果存在一定偏倚。
綜上所述,通過對納入文獻的Meta分析,我們發現RATS縱膈腫瘤切除術在術中出血量、中轉開胸率、術后總并發癥發生率、術后引流時間、術后住院時間等方面均優于VATS縱膈腫瘤切除術。其次,RATS縱隔腫瘤切除增加了醫療費用。然而,目前缺乏對術后患者的長期隨訪研究。我們期待在未來有更多大樣本、高質量的隨機對照研究進一步驗證本研究結果。
利益沖突:無。
作者貢獻:曹煒、李浩篪負責論文設計,開展研究,數據處理與分析,論文撰寫與修改;楊凱、王淇負責論文審核和修改;左莊負責實施研究;曹煒負責數據整理與分析;茍云久負責論文設計。
縱隔腫瘤是縱隔內組織結構腫瘤性改變的統稱,是胸外科常見病,包括胸腺瘤、神經源性腫瘤、畸胎瘤等[1-2]。縱隔內器官和組織解剖結構復雜且空間狹小,其周圍鄰近心臟及大血管等重要臟器。臨床上,手術通常是縱隔腫瘤的首選治療方法,患者大多預后較好[3-4]。20世紀以來,電視胸腔鏡技術發展迅速,大量病例證明,與經典胸骨正中切口或前外側肋間切口開胸入路相比,微創電視輔助胸腔鏡手術(video-assisted thoracoscopic surgery,VATS)具有切口小、創傷小、并發癥少、術后恢復快等優點[5]。目前,微創VATS已取代傳統開胸手術,廣泛應用于臨床縱隔相關疾病的治療。然而,傳統的電視胸腔鏡存在一些不可避免的缺陷,如二維景深、小空間(特別是上縱隔和胸膜頂病變處理能力不足)、縫合打結等操作困難等[6]。針對VATS的缺陷,開發了機器人輔助胸腔鏡手術。該機器人系統的優點是可以提供高達10-15倍放大的高分辨率三維視場,從而實現對縱隔結構細節的更清晰觀察[7]。同時,機器人輔助胸外科手術(robot-assisted thoracic surgery,RATS)可解決VATS帶來的手部生理性震顫,避免因手術失誤造成副損傷和意外傷害[8]。
多個研究[9-10]已經揭示了VATS或RATS治療縱隔腫瘤的可行性和安全性。但是這些研究都屬于小樣本量的單中心回顧性研究。在縱隔腫瘤的治療中,RATS能否達到與VATS相同甚至更好的手術效果尚不清楚。因此,本研究結合最新國內外文獻,進行全面的Meta分析,以期為臨床實踐提供更高水平的循證醫學證據。
1 資料與方法
1.1 納入與排除標準
1.1.1 納入標準
(1)研究類型:回顧性隊列研究或隨機對照試驗;(2)研究對象:診斷為縱隔腫瘤且符合手術指征的患者;(3)干預措施:RATS或VATS縱隔腫瘤手術;(4)結局指標:腫瘤大小、手術時間、術中出血量、中轉開胸率、術后引流時間、術后總并發癥發生率、術后住院時間等。
1.1.2 排除標準
(1)數據不完整或無法提供有用數據的研究;(2)非臨床比較性研究,如綜述、病例報告或單干預措施的研究;(3)重復發表或納入病例較少(≤10例)的研究。
1.2 檢索策略
對PubMed、EMbase、The Cochrane Library、Web of Science、萬方、CNKI、CBM、VIP數據庫進行系統、全面的文獻檢索,檢索時間為建庫至2024年3月31日。檢索比較RATS和VATS治療縱隔腫瘤臨床療效的相關文獻。中文檢索詞為:機器人輔助胸外科手術、機器人、機器人輔助、達芬奇、視頻輔助胸外科手術、視頻輔助、縱隔腫瘤、胸腺瘤、畸胎瘤、神經源性腫瘤。英文檢索詞為:robot-assisted thoracic surgery、robotic、robot-assisted、da Vinci、video-assisted thoracic surgery、video-assisted、mediastinal tumors、mediastinal neoplasms、mediastinum cancers、mediastinal cancer。以PubMed數據庫為例,檢索式如下:(("mediastinal tumors"[All Fields] OR "mediastinal neoplasms" [MeSH Terms] OR "mediastinum cancers"[All Fields] OR "mediastinal cancer"[All Fields])) AND ("robot-assisted thoracic surgery"[MeSH Terms] OR "robot-assisted"[All Fields] OR "da Vinci"[All Fields])) AND ("video-assisted thoracic surgery"[MeSH Terms] OR "video-assisted"[All Fields]))。
1.3 數據資料提取及質量評價方法
文獻檢索由兩名研究者獨立完成,并通過閱讀檢索文獻的標題和摘要來評估是否初步納入研究。在初步檢索完成后,閱讀檢索文獻的全文,以決定是否將其納入研究。對于有疑問或不同意見的研究,通過團隊討論來解決。研究提取內容包括:(1)作者、年份、樣本量、性別、年齡、干預措施、研究類型;(2)相結局指標:腫瘤大小、手術時間、術中出血量、中轉開胸率、術后總并發癥、術后引流時間、術后住院時間、住院費用。
采用紐卡斯爾-渥太華量表(Newcastle-Ottawa Scale,NOS)對納入研究進行質量評價,NOS包括3個項目:隊列的選擇、研究組間可比性和結果評估[11]。高質量研究定義為質量評分≥7分的研究。任何分歧均通過團隊討論解決。
1.4 統計學分析
使用 Review Manager 5.4軟件分別計算二分類變量資料和連續性變量資料的相對比值比(odds ratio,OR)和均數差(mean difference,MD)以及95%CI。研究間的異質性用Q檢驗和I2檢驗,若I2<50%,P>0.1,各研究間異質性不顯著,采用固定效應模型;若I2≥50%,P≤0.1,各研究間異質性顯著,采用隨機效應模型。通過敏感性分析檢驗Meta分析結果的穩定性,采用漏斗圖分析潛在的發表偏倚。
2 結果
2.1 文獻檢索結果
初步檢索共獲得文獻975篇,剔重后剩余584篇。通過閱讀題目和摘要排除232篇,進一步閱讀全文排除文獻320篇,最終納入32篇文獻[12-43]。文獻篩選流程見圖1。
 圖1
文獻篩選流程
圖1
文獻篩選流程
*:PubMed(
2.2 文獻基本特征
納入32篇文獻[12-43],共
2.3 Meta分析結果
2.3.1 腫瘤大小
納入22篇文獻[12-15,17,20-21,23,27-30,32-41],共
2.3.2 手術時間
納入28篇文獻[12-18,20-23,25-26,28-32,34-43],共
2.3.3 術中出血量
納入25篇文獻[12-15,17,21-23,25,28-43],共
2.3.4 中轉開胸率
納入10篇文獻[12,15,17,19,22,26,30,35,38,40],共
2.3.5 術后總并發癥
納入24篇文獻[12-13,15-18,20-22,25,28-30,32-35,37-43],共
2.3.6 術后引流時間
納入24篇文獻[12-15,17,18,20-23,28,30-35,37-43],共
2.3.7 術后住院時間
納入30篇文獻[12-24,27-43],共
2.3.8 住院費用
納入9篇文獻[16-17,21,30-31,34,38–40],共
2.4 亞組分析
為尋找研究間的異質性來源,根據各研究納入患者的國家將各指標分為中國組和其他國家組后進行亞組分析。結果顯示,在中國組中,各項指標與總體相比異質性無明顯變化,P值無顯著改變;在其他國家組中,術中出血量、術后并發癥、術后引流時間,住院費用的P值和總體相比有顯著變化,均表現為無統計學差異;見表3。
2.5 敏感性分析
分別采用固定和隨機效應模型分析中轉開胸率、術后總并發癥,結果無明顯差異。而對于腫瘤大小、手術時間、術中出血量、術后引流時間、術后住院時間、住院費用等指標,原始研究間異質性較大,對于這些指標進行敏感性分析,逐步排除一些研究直至研究間異質性為I2=0%,再分別使用隨機和固定效應模型驗證結果,結果無明顯變化,表明Meta分析結果穩定;見表4。
2.6 發表偏倚分析
通過對各結局指標繪制漏斗圖,發現所有研究均均勻分布在漏斗圖的兩側,說明本研究的發表偏倚較小。以術后總并發癥發生率為例繪制的漏斗圖見圖2。
 圖2
術后總并發癥發生率漏斗圖
圖2
術后總并發癥發生率漏斗圖
3 討論
縱隔的解剖結構較復雜且空間狹小,縱隔腫瘤組織來源多樣,鄰近心臟、大血管等重要臟器[44]。自2001年Yoshino等[45]報道世界上首例機器人縱隔腫瘤切除術以來,RATS已在一些大型醫療中心用于治療縱隔腫瘤。目前,微創手術發展迅速,RATS縱隔腫瘤切除術和VATS縱隔腫瘤切除術越來越多地被胸外科醫生選擇。然而,RATS在縱隔腫瘤切除方面是否優于VATS仍然存在爭議。因此,我們進行Meta分析,以比較和討論RATS和VATS治療縱隔腫瘤的有效性和安全性。
本Meta分析結果顯示,RATS組與VATS組患者的腫瘤大小差異不顯著,表明腫瘤的大小不會影響縱隔腫瘤切除術式的選擇。同樣,兩組患者在手術時間上的總體比較也無顯著差異。最初的一些研究[16]表明,RATS的手術時間通常相對較長,導致這種差異的原因可能是一些醫療中心開展機器人手術較晚,且受縱隔復雜解剖結構的影響,RATS在縱隔腫瘤的手術經驗不足,一些外科醫生的RATS學習曲線正處于緩慢的上升階段。然而,隨著近年來胸外科醫生縱隔手術經驗的積累和RATS手術操作熟練程度的提升,RATS的手術時間顯著縮短。
對比術中出血量,我們發現RATS組術中出血量明顯少于VATS組。這可能是因為RATS可以在手術中提供三維放大視圖,更靈活的操作,消除手部震顫,從而準確暴露切除靶點周圍復雜的解剖結構[2]。這有助于醫生在手術過程中精確地實施手術,更好地控制小血管出血。
在中轉開胸率方面,RATS組比VATS組更有優勢。中轉開胸手術多是由于RATS或VATS術中發現較復雜的情況,如腫瘤位置、大小等與預期不符或腫瘤已侵入到周圍組織血管以及發生胸膜粘連,需要中轉開胸以更好地處理腫瘤。RATS組中轉開胸率低于VATS組可能得益于RATS手術的高三維視野,可全面觀察腫瘤情況并實施更精細的手術操作,從而減少中轉開胸的可能性[46]。然而,需要注意的是,雖然RATS組中轉開胸率低于VATS組,但RATS轉開胸不如VATS方便。
術后并發癥是評價術后短期療效的重要指標。本研究結果顯示,RATS組術后并發癥總體發生率低于VATS組。主要原因如下:(1)與VATS相比,RATS術后恢復更快,并發癥風險明顯降低。(2)RATS提高了術者手術的舒適度,有助于在堅持安全、無腫瘤、微創的基礎上,提高腫瘤的全切率、前縱隔脂肪組織切除的徹底性等,從而降低術后并發癥發生率。在臨床實踐中,我們也發現RATS在解剖前縱隔脂肪和脂肪組織方面更有優勢。RATS可提供更完整、精確的腫瘤解剖,從而更好地保護縱隔腫瘤膜的完整性。
術后引流時間方面,Meta分析結果顯示,RATS組短于VATS組。我們認為這可能是RATS在手術精準度上比VATS更具優勢。RATS為手術過程提供更精確的三維視野,可準確評估腫瘤大小,切除腫瘤和組織更完整,減少了小血管的損傷且止血比較徹底,從而減少周圍組織的刺激因素,使術后引流量顯著減少。同時,在前縱隔腫瘤手術中,縱隔周圍區域的脂肪組織也隨腫瘤完全切除,減少了術后炎癥反應,術后引流量即相對減少。上述因素均使RATS組術后引流量減少,從而縮短術后引流時間。
對于術后住院時間,Meta分析結果表明,RATS組患者的術后住院時間比VATS組患者短。我們考慮這是因為RATS比VATS更具微創性,術后給患者帶來的創傷相對較小,因此患者術后疼痛較輕,恢復更快,在一定程度上縮短了術后住院時間,這也符合快速康復的理念[47]。
關于術后住院費用,Meta分析結果顯示,RATS組的術后住院費用普遍較高。我們分析其主要原因是RATS手術設備和技術較新,相比傳統腔鏡較復雜,手術時間相對較長,這在一定程度上增加了術后住院費用。
亞組分析結果顯示,中國組的研究是總體研究異質性的主要來源;其他國家在一些指標的統計學差異可能是國內外RATS開展時間和發展水平差異導致的。手術時間、術中出血量等原始研究間異質性較大,可能與腫瘤類型有關,納入的文獻中包括前縱隔腫瘤、中縱隔腫瘤和后縱隔腫瘤,不同部位的縱膈腫瘤手術難度和手術入路可能不同,導致手術時間不同。同時,不同醫院的手術水平存在差異導致手術時間與術中出血量也存在差異,并且患者年齡和性別對術中出血量也有影響。
本Meta分析的局限性:(1)醫院成本存在顯著異質性,這可能是由于不同醫療中心的RATS收費標準不同所致;(2)納入的研究都是回顧性臨床研究,選擇偏倚在所難免,需要大樣本的隨機對照試驗進行驗證;(3)目前缺乏兩類手術的長期隨訪數據,我們希望在未來進一步完善這一數據;(4)本研究沒有對縱隔腫瘤的位置進行更詳細的比較,可能導致結果存在一定偏倚。
綜上所述,通過對納入文獻的Meta分析,我們發現RATS縱膈腫瘤切除術在術中出血量、中轉開胸率、術后總并發癥發生率、術后引流時間、術后住院時間等方面均優于VATS縱膈腫瘤切除術。其次,RATS縱隔腫瘤切除增加了醫療費用。然而,目前缺乏對術后患者的長期隨訪研究。我們期待在未來有更多大樣本、高質量的隨機對照研究進一步驗證本研究結果。
利益沖突:無。
作者貢獻:曹煒、李浩篪負責論文設計,開展研究,數據處理與分析,論文撰寫與修改;楊凱、王淇負責論文審核和修改;左莊負責實施研究;曹煒負責數據整理與分析;茍云久負責論文設計。