肺癌是我國發病率和死亡率排名第1的惡性腫瘤[1],其中非小細胞肺癌(non-small cell lung cancer,NSCLC)占比84%[2]。手術是早期肺癌的主要治療手段。肺手術切除范圍包括肺葉切除、肺段切除、楔形切除等。自1995年以來,肺葉切除術一直被視為早期NSCLC的標準治療方案。大型多中心隨機對照試驗(JCOG0802/WJOG4607L)[3-4]表明,肺段切除術相比肺葉切除術在5年生存率方面具有很大潛力,因而最新的NCCN指南[5]強烈推薦將其作為周圍性T1a-bN0M0NSCLC的替代方法。隨著低劑量螺旋CT肺癌篩查的普及和人們體檢意識的提高,越來越多的老年肺癌患者被及早發現。同時,外科治療模式的不斷優化也使高齡患者接受手術治療的限制逐漸減少[6-7]。然而,相比于年輕患者,老年肺癌患者具有其特殊性:合并癥較多、身體機能差、手術風險及術后并發癥發生率也更高[8-9];同時,該類患者預期壽命有限,因此在選擇手術切除范圍時存在較大爭議,尚需進一步研究[10]。本研究擬回顧性納入美國監測、流行病學和最終結果(Surveillance,Epidemiology,and End Results,SEER)數據庫中行肺葉切除術或肺段切除術的老年Ⅰ期NSCLC患者,比較兩組遠期生存情況,以期為老年Ⅰ期NSCLC患者的手術方式選擇提供理論依據。
1 資料與方法
1.1 臨床資料和分組
研究納入SEER數據庫中2010—2020年術后病理確診的NSCLC患者。納入標準:(1)NSCLC患者(肺鱗癌:
1.2 資料收集
收集患者的基線資料和生存資料。基線資料包括:(1)人口學資料:年齡、性別、人種;(2)病灶特點:病灶大小和位置、組織學亞型、分化程度、胸膜侵襲、分期;(3)手術信息:切除范圍。生存資料(研究結局指標)包括:總生存(overall survival,OS)和肺癌特異性生存(lung cancer specific survival,LCSS)。
1.3 統計學分析
所有統計學分析均采用R 4.3.3的“CBCgrps”“survival”“survminer”和“MatchIt”等包完成[12]。符合正態分布的計量資料以均數±標準差(x±s)描述,組間比較采用Student’s t檢驗;不符合正態分布的以中位數(上下四分位數)[M(P25,P75)]描述,組間比較采用Wilcoxon秩和檢驗。計數資料以頻數(百分比)描述,組間比較采用四格表χ2檢驗。采用單因素及多因素Cox比例風險回歸分析影響兩組患者預后的風險因素。單因素Cox回歸中,P<0.1的變量納入多因素Cox回歸分析。采用風險比(hazard ratio,HR)及其95%可信區間(confidence interval,CI)描述單因素和多因素分析結果。基于年齡、性別、種族、組織病理學亞型、病灶位置、病灶所在肺葉、病灶大小、分化程度、胸膜侵犯程度、輔助放療,對肺葉切除組患者和肺段切除組患者以2∶1進行傾向性評分匹配(propensity score matching,PSM)。采用Kaplan-Meier法繪制匹配后的生存曲線,利用log-rank檢驗比較兩組患者的生存差異,并進一步在不同患者亞組中比較肺段和肺葉切除對患者預后的影響。檢驗水準α=0.05。
1.4 倫理審查
本研究數據來源于SEER數據庫中的匿名和去識別數據。研究已獲得眉山市人民醫院醫學倫理審查委員會批準(2024-81)。
2 結果
2.1 患者基線特征
納入
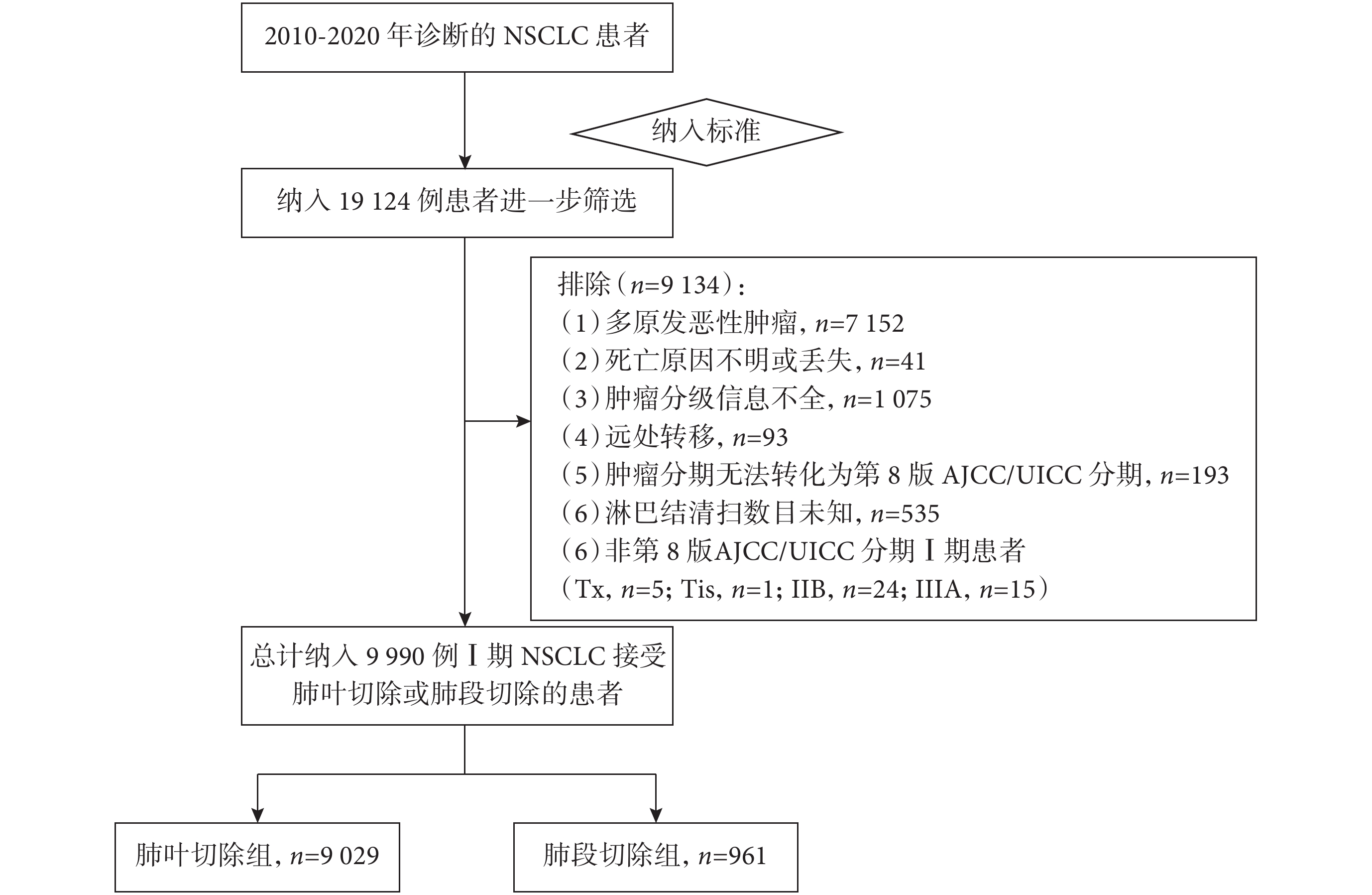
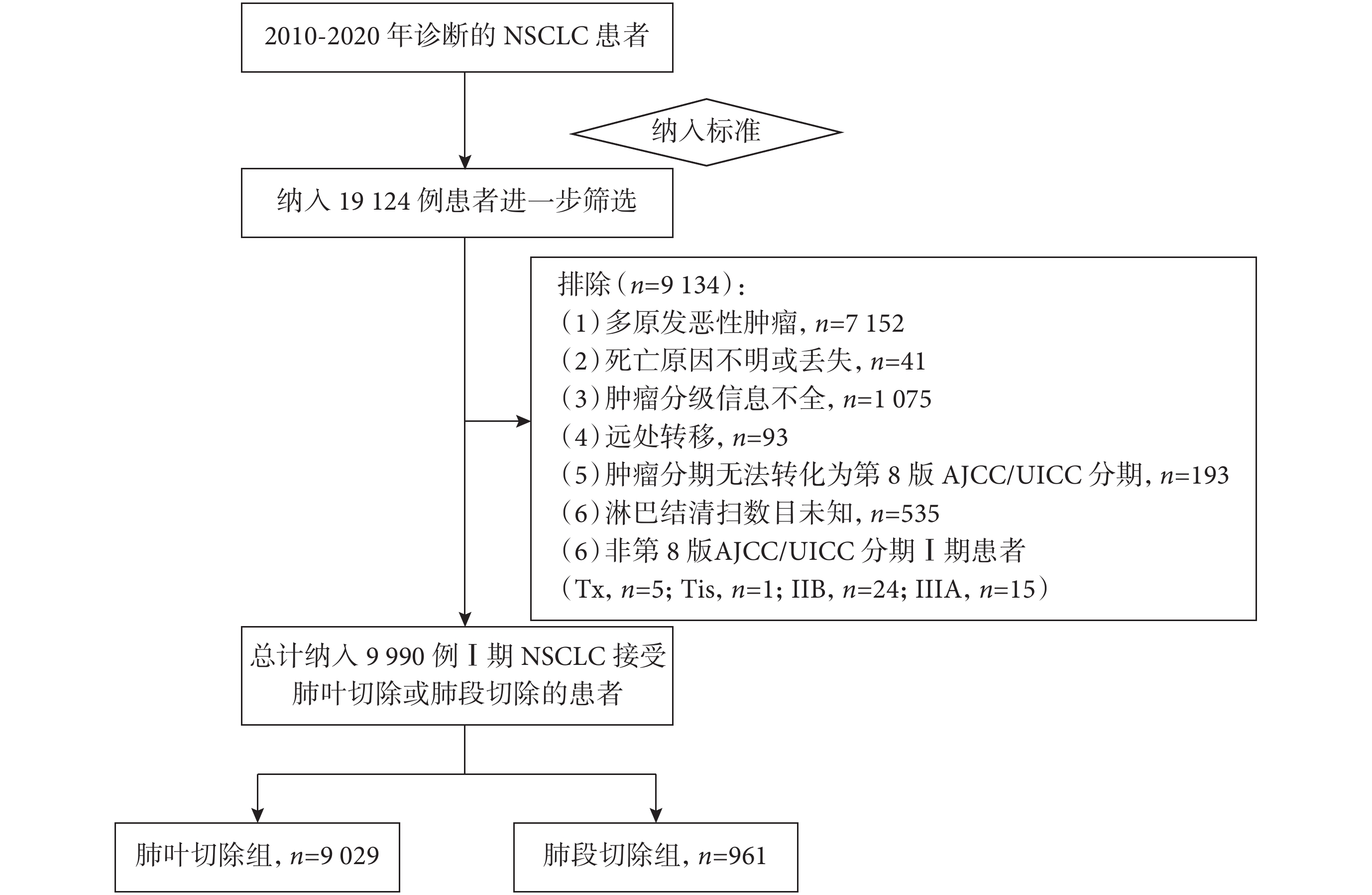 圖1
患者篩選流程圖
圖1
患者篩選流程圖
2.2 總生存的危險因素
以OS為結局,進行單因素Cox回歸分析,發現年齡、性別、種族、組織病理學亞型、腫瘤大小、分化程度、胸膜侵犯程度、腫瘤分期、手術方式、淋巴結清掃數目以及是否接受輔助放療對患者預后有顯著影響(P<0.01)。進一步多因素Cox回歸分析顯示,年齡>70歲、男性、白種人、腫瘤病理亞型為非腺癌的NSCLC(尤其是鱗癌)、腫瘤直徑>2 cm、分化程度低、接受肺段切除術、淋巴結清掃數目過少、接受過輔助放療是患者預后不良的高危因素(P<0.01);見表2。
2.3 亞組分析
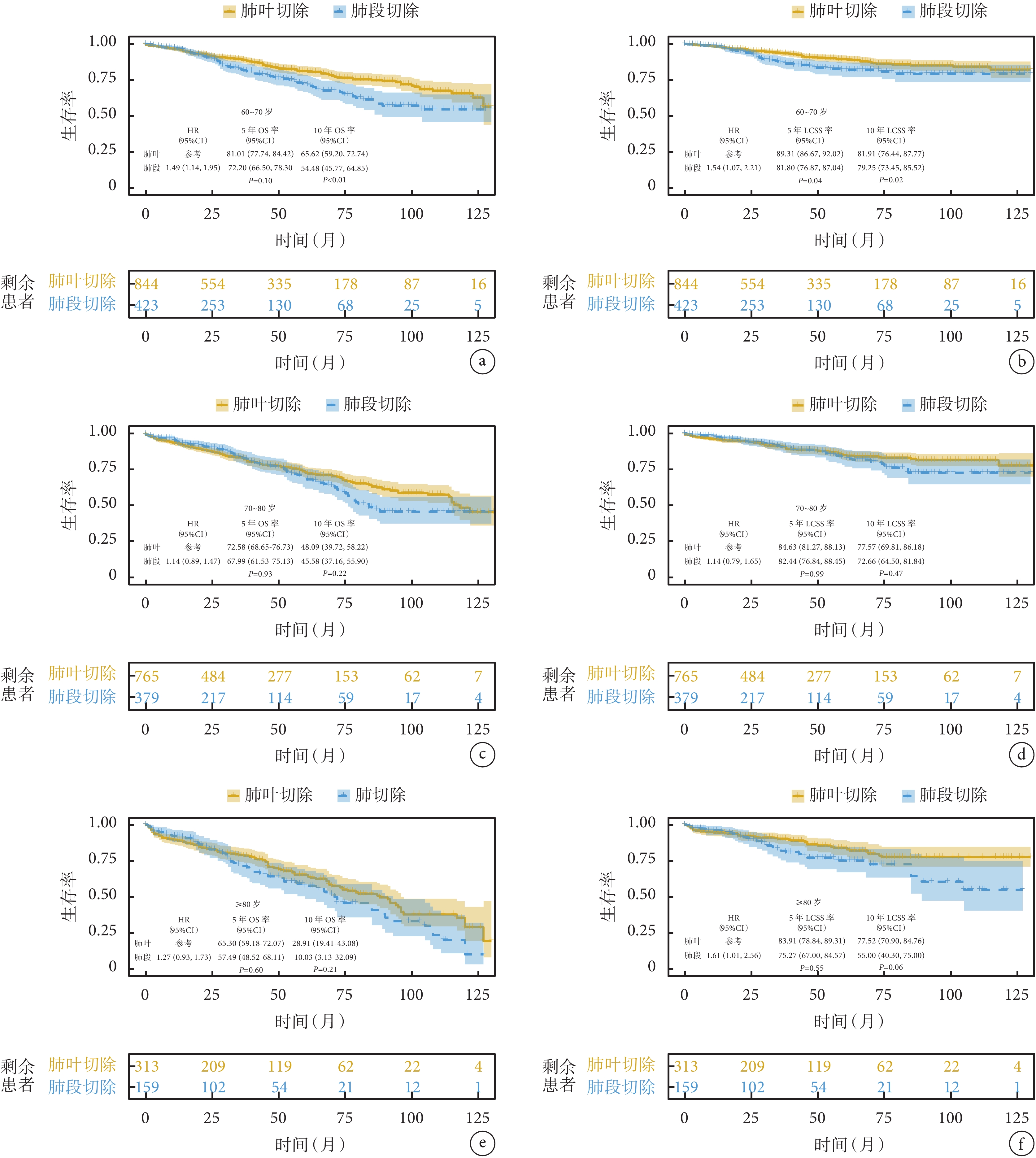
對不同年齡段患者進行生存分析發現,60~70歲Ⅰ期NSCLC患者,接受肺葉切除后的10年OS率(P<0.01)和LCSS率(P=0.02)均顯著高于肺段切除患者。而對于>70歲患者,兩組手術方式的5年OS率(P=0.81)及10年OS率(P=0.06)差異無統計學意義;見圖3。
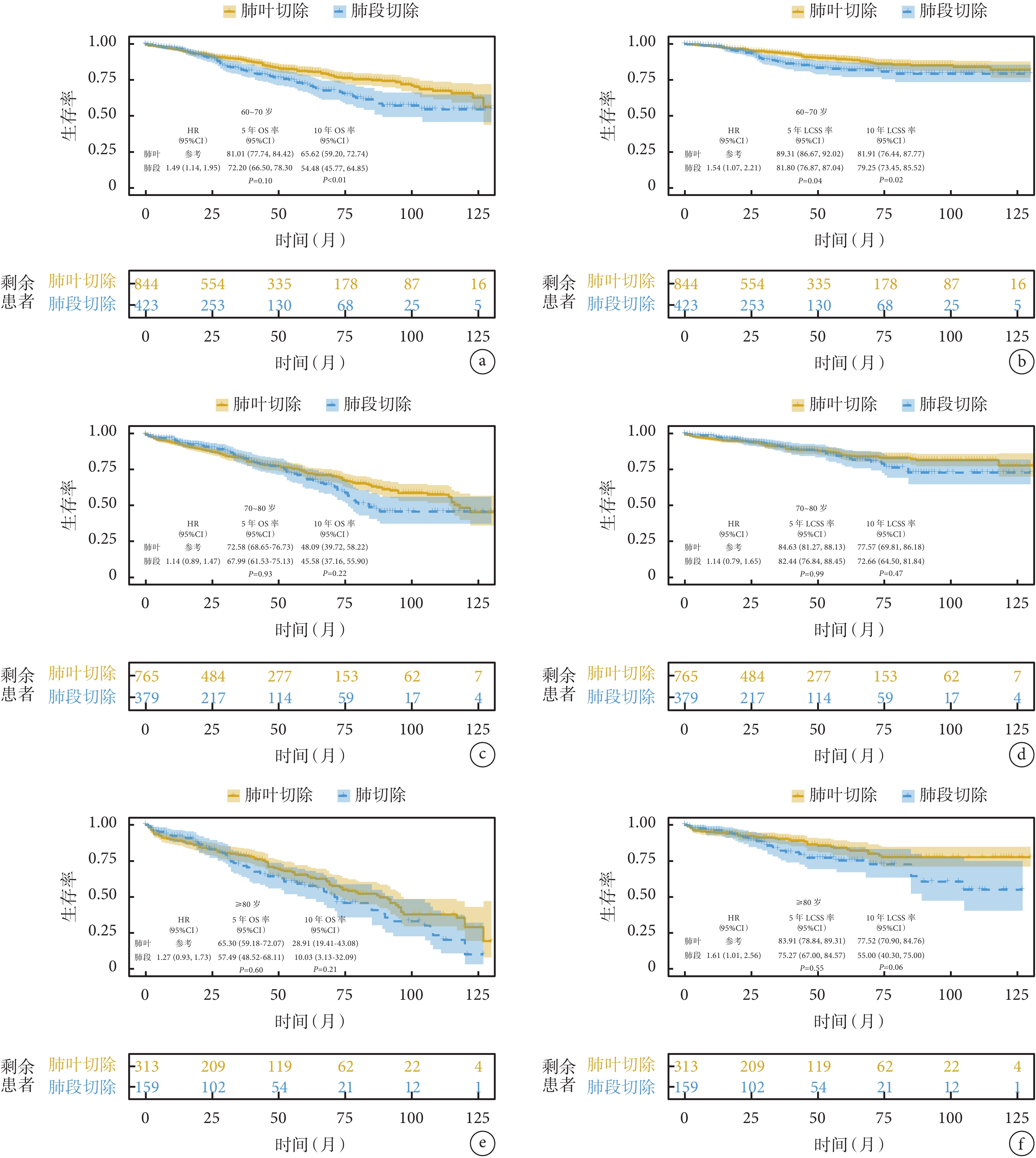 圖3
傾向性評分匹配后不同年齡段患者生存比較
圖3
傾向性評分匹配后不同年齡段患者生存比較
a~b:分別為60~70歲患者OS和LCSS比較;c~d:分別為70~80歲患者OS和LCSS比較;e~f:分別為≥80歲患者OS和LCSS比較;OS:總生存;LCSS:肺癌特異性生存
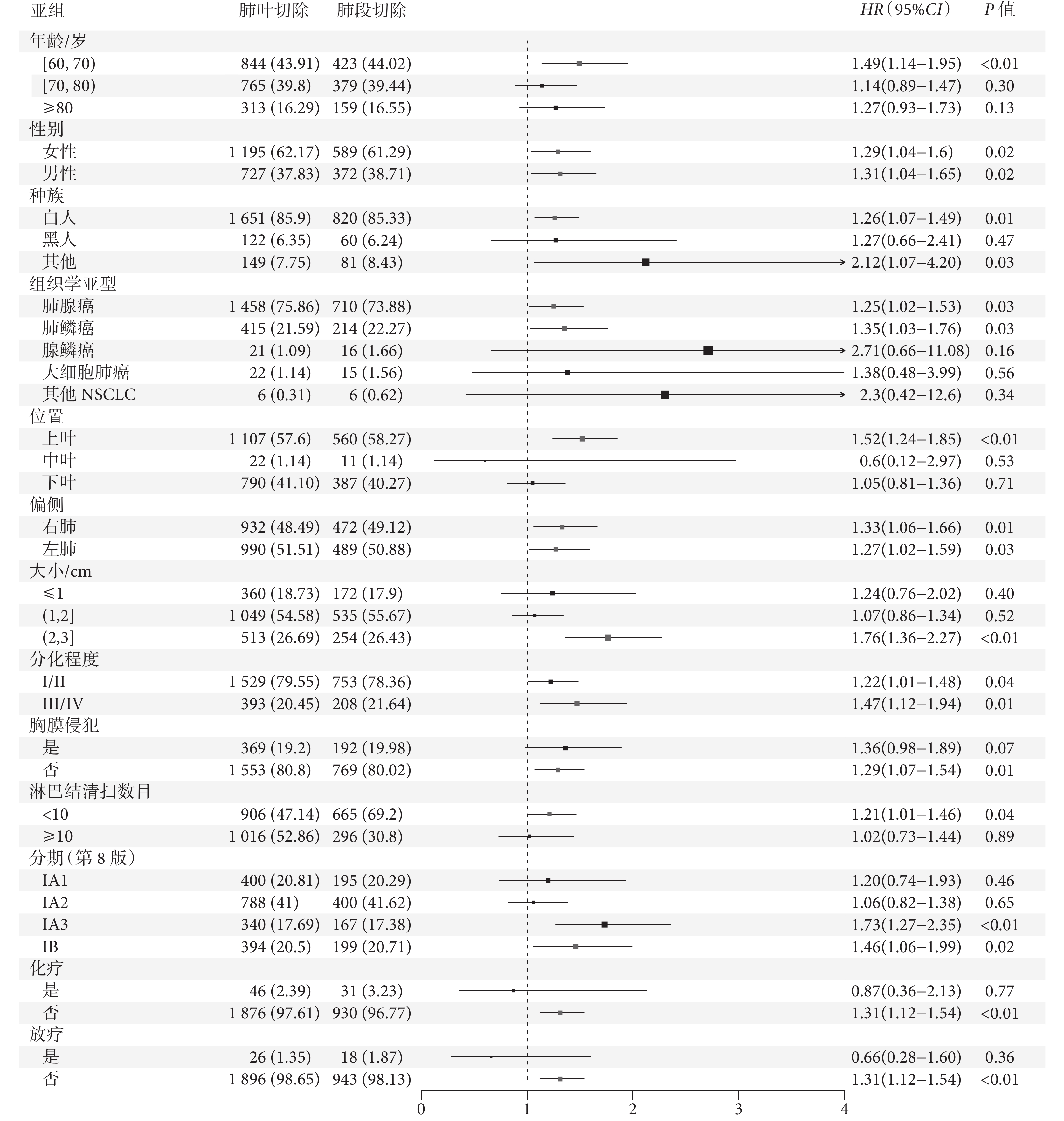
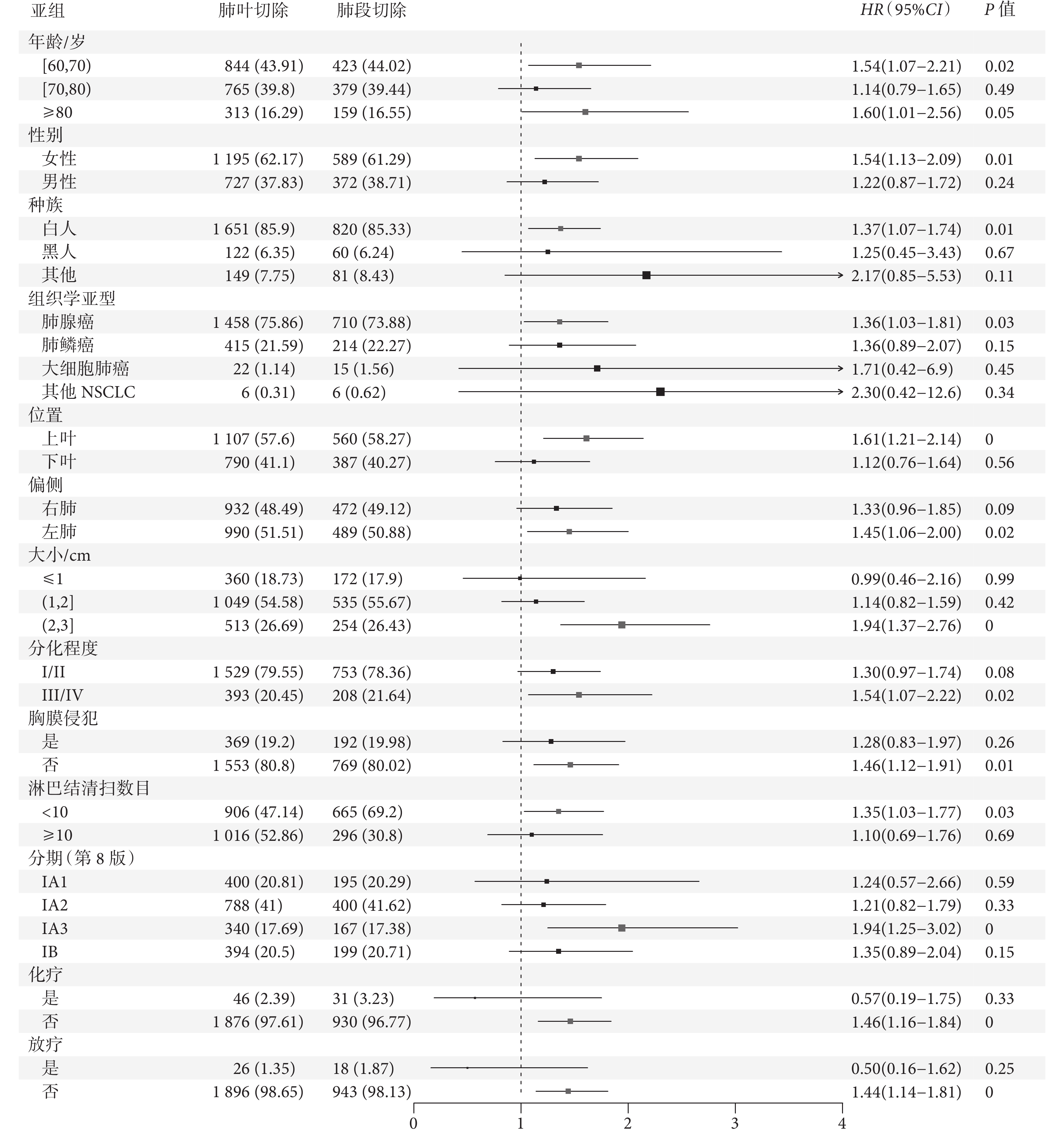
進一步亞組分析顯示,對于年齡60~70歲、女性、白種人、腫瘤組織學亞型為肺腺癌、位于左肺及上葉、直徑>2 cm、分化程度較高、淋巴結清掃個數<10枚、術后不行化療/放療患者,肺葉切除術的OS及LCSS獲益均高于肺段切除術。而對于年齡70~80歲、黑種人、腫瘤位于下葉、直徑≤2 cm(ⅠA1~ⅠA2期),淋巴結清掃個數≥10枚,術后行化療/放療患者,肺段切除與肺葉切除對生存無顯著影響;見圖4~5。
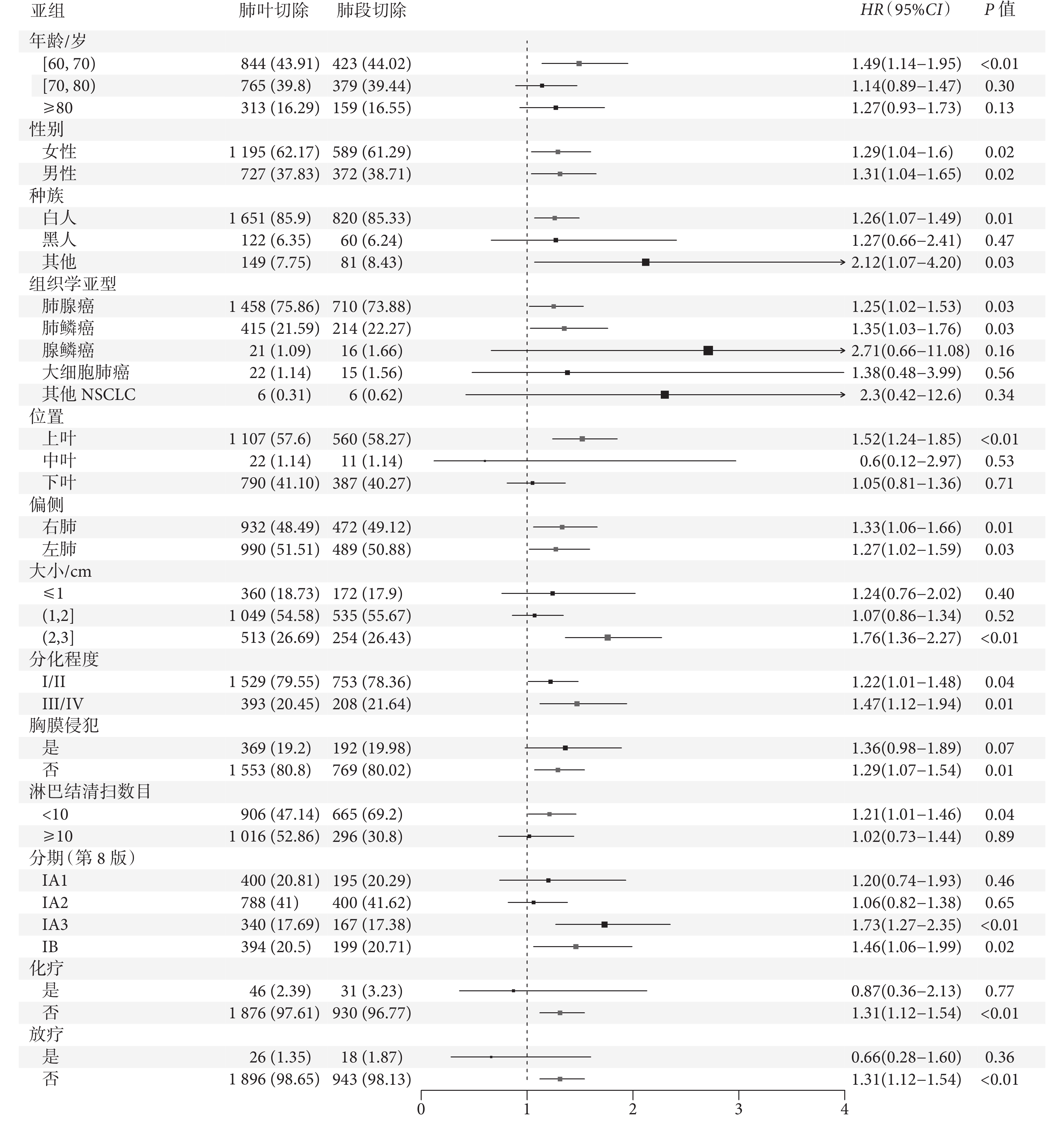 圖4
總生存的亞組分析森林圖
圖4
總生存的亞組分析森林圖
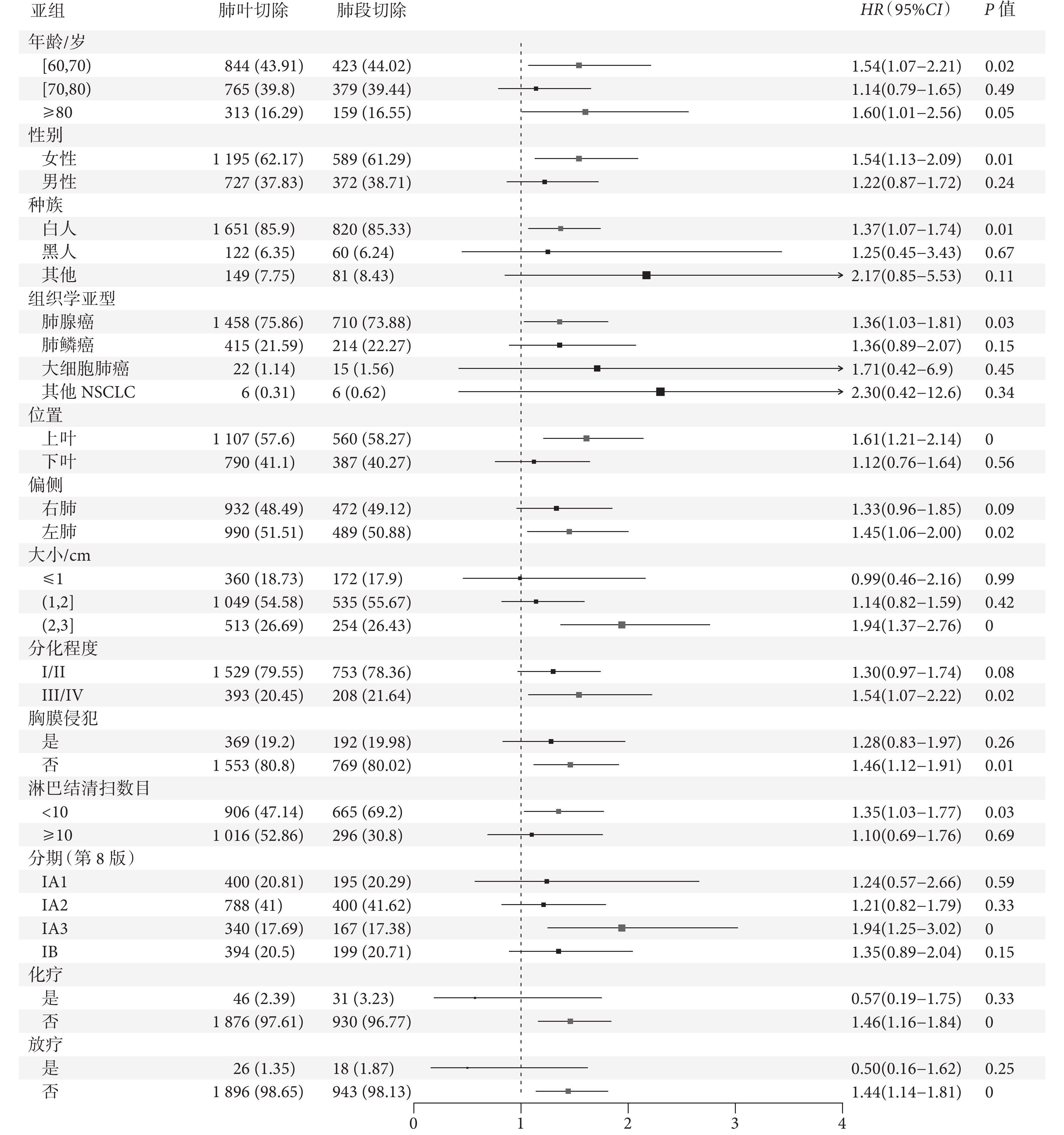 圖5
肺癌特異性生存的亞組分析森林圖
圖5
肺癌特異性生存的亞組分析森林圖
3 討論
本研究基于SEER數據庫2010—2020年肺癌患者數據,通過PSM,探究了老年Ⅰ期NSCLC患者接受肺葉切除和肺段切除術的預后差異。總體分析結果提示,與肺段切除相比,肺葉切除能夠帶來更高的10年OS率和LCSS率。但進一步亞組分析發現,肺葉切除的優勢僅局限于60~70歲老年Ⅰ期NSCLC患者,對于>70歲患者,肺葉切除患者的生存率雖仍略高于肺段切除組,但差異無統計學意義。此外,在患者腫瘤直徑≤2 cm、分期較早(ⅠA1~ⅠA2期)、術中確保淋巴結清掃質量、術后行輔助放/化療等特定情況下,肺段切除也能帶來與肺葉切相似的遠期預后。
老年Ⅰ期NSCLC患者手術方式選擇問題一直備受國內外關注。對于肺葉和肺段對圍術期結局的比較,一項基于10家中國三甲醫院數據的回顧性研究[13]結果顯示,>65歲的老年Ⅰ期NSCLC患者中,亞肺葉切除術更常用于年齡大、合并癥多、腫瘤較小、位于左側、組織學亞型為腺癌的患者;肺段切除患者術中失血量更少,手術時間、術后置管時間及住院時間明顯縮短,且短期生存與肺葉切除術無顯著差異。但本研究中,肺段組患者淋巴結切除個數顯著少于肺葉組,肺段切除對N分期、局部復發和長期預后的影響尚不明確。另一項來自瑞士的單中心回顧性研究[14]顯示,對于直徑<2 cm的實性NSCLC,腔鏡下肺段切除與肺葉切除患者的短期內局部復發情況相似[中位隨訪時間:23(6~38.5)個月]。而針對長期預后的比較,一項基于SEER數據庫的回顧性研究[15]發現,肺葉切除相比亞肺葉切除并不會為>70歲、ⅠA期、腫瘤直徑≤3 cm的老年NSCLC患者帶來更多的遠期生存(LCSS)獲益。而日本的大型多中心隨機對照試驗(JCOG0802/WJOG4607L)[3]公布的結果則顯示,對于腫瘤大小≤2 cm、純實性的周圍型早期肺癌,肺段切除術相比肺葉切除術在提高5年OS率方面更有優勢,尤其是針對>70歲患者[肺葉切除:77.1%,95%CI(68.2,83.8)],肺段切除:85.6%,95%CI(77.5,90.9),P<0.01]。然而,兩組患者的總體局部復發率雖無顯著差異,但對于<70歲女性患者,肺段切除患者5年內疾病復發風險顯著高于肺葉切除患者[HR=4.10,95%CI(1.36,12.38),P<0.01]。值得注意的是,JCOG0802/WJOG4607L研究中,>70歲且腫瘤大小≤2 cm、接受肺段切除患者的5年OS率顯著高于我們基于北美SEER數據庫分析得出的結果[69.60%,95%CI(63.50,76.40)]。而我們對>70歲且腫瘤大小≤2 cm人群的比較結果顯示,肺段切除患者的5年OS率不差于肺葉切除[72.74%,95%CI(68.85,76.85),P=0.37]。這可能與人種、不同地區手術方式及圍術期管理等差異有關[16]。
綜合以上研究結果,我們認為:相比于肺段切除術,肺葉切除術能夠更全面地清除腫瘤病灶,并且清掃的淋巴結數目相對更多,可確保更為精確的肺癌病理分期及治療方案選擇[17],有效降低疾病復發風險,為大部分患者帶來更優的OS。然而,對于部分年齡較大的患者(如>70歲),其身體狀況較差,術后康復能力較弱,加之預期壽命有限,即使采用肺葉切除術,長期預后及生活質量也不一定優于其他手術方式。此外,對于腫瘤直徑較小(≤2 cm)和分期較早(ⅠA1~ⅠA2期)的患者,由于腫瘤本身的惡性程度較低,尤其是腺癌早期病變及含有GGO成分的肺結節[18-19],即使采用肺段切除術,遠期預后也不會顯著差于肺葉切除術。除以上結論外,盡管目前的循證證據[20]及本研究結果均不支持Ⅰ期NSCLC患者在接受標準手術切除方案(肺葉切除術)后行輔助化療,本研究結果提示,肺段切除術后行放/化療可能改善長期預后。但這一結論還需進一步通過大樣本研究證實。
本研究存在一些不足。首先,本研究是一項回顧性研究,不可避免存在選擇偏倚,但本研究使用了PSM方法,盡量減小了基線差異對結果造成的偏倚。其次,本研究從人口學特征、病灶特點和手術信息等方面研究了不同肺手術切除范圍的預后差異,但受限于SEER數據庫本身的信息完整度,仍有一些指標未納入分析,如合并癥、肺功能、腫瘤實性成分占比、手術方式(腔鏡或者開胸,聯合切除)、淋巴結清掃站數等。另外,SEER數據庫為北美腫瘤登記數據庫,患者中白種人占比顯著高于其他人種,因此考慮人種、手術方式及手術開展中心的差異,應謹慎對待本研究結論,其對中國臨床的適用性待進一步驗證。最后,在生存數據方面,詳細的復發、轉移數據不全,這也限制了對結果的深入分析。期待未來多中心、大樣本研究結果(如STEPS研究[21]等)為中國Ⅰ期NSCLC老年患者的術式選擇提供更高質量的臨床指導。
綜上,本研究基于SEER數據庫的分析結果提示,對于老年Ⅰ期NSCLC患者,肺葉切除對改善OS和LCSS更具優勢。但對年齡>70歲、腫瘤直徑≤2 cm、分期為ⅠA1~ⅠA2期等特定類型患者,在確保淋巴結清掃質量和精確病理分期的基礎上,肺段切術是可行的。因此,在決定老年Ⅰ期NSCLC患者手術切除范圍時,應綜合考慮個體差異、腫瘤特征和圍術期治療方案。
利益沖突:無。
作者貢獻:崔輝主導研究實施,負責選題與設計,崔輝、石勇、余永康負責數據搜集和整理;崔輝、胡祥負責數據分析;全體作者參與論文撰寫和修改。
肺癌是我國發病率和死亡率排名第1的惡性腫瘤[1],其中非小細胞肺癌(non-small cell lung cancer,NSCLC)占比84%[2]。手術是早期肺癌的主要治療手段。肺手術切除范圍包括肺葉切除、肺段切除、楔形切除等。自1995年以來,肺葉切除術一直被視為早期NSCLC的標準治療方案。大型多中心隨機對照試驗(JCOG0802/WJOG4607L)[3-4]表明,肺段切除術相比肺葉切除術在5年生存率方面具有很大潛力,因而最新的NCCN指南[5]強烈推薦將其作為周圍性T1a-bN0M0NSCLC的替代方法。隨著低劑量螺旋CT肺癌篩查的普及和人們體檢意識的提高,越來越多的老年肺癌患者被及早發現。同時,外科治療模式的不斷優化也使高齡患者接受手術治療的限制逐漸減少[6-7]。然而,相比于年輕患者,老年肺癌患者具有其特殊性:合并癥較多、身體機能差、手術風險及術后并發癥發生率也更高[8-9];同時,該類患者預期壽命有限,因此在選擇手術切除范圍時存在較大爭議,尚需進一步研究[10]。本研究擬回顧性納入美國監測、流行病學和最終結果(Surveillance,Epidemiology,and End Results,SEER)數據庫中行肺葉切除術或肺段切除術的老年Ⅰ期NSCLC患者,比較兩組遠期生存情況,以期為老年Ⅰ期NSCLC患者的手術方式選擇提供理論依據。
1 資料與方法
1.1 臨床資料和分組
研究納入SEER數據庫中2010—2020年術后病理確診的NSCLC患者。納入標準:(1)NSCLC患者(肺鱗癌:
1.2 資料收集
收集患者的基線資料和生存資料。基線資料包括:(1)人口學資料:年齡、性別、人種;(2)病灶特點:病灶大小和位置、組織學亞型、分化程度、胸膜侵襲、分期;(3)手術信息:切除范圍。生存資料(研究結局指標)包括:總生存(overall survival,OS)和肺癌特異性生存(lung cancer specific survival,LCSS)。
1.3 統計學分析
所有統計學分析均采用R 4.3.3的“CBCgrps”“survival”“survminer”和“MatchIt”等包完成[12]。符合正態分布的計量資料以均數±標準差(x±s)描述,組間比較采用Student’s t檢驗;不符合正態分布的以中位數(上下四分位數)[M(P25,P75)]描述,組間比較采用Wilcoxon秩和檢驗。計數資料以頻數(百分比)描述,組間比較采用四格表χ2檢驗。采用單因素及多因素Cox比例風險回歸分析影響兩組患者預后的風險因素。單因素Cox回歸中,P<0.1的變量納入多因素Cox回歸分析。采用風險比(hazard ratio,HR)及其95%可信區間(confidence interval,CI)描述單因素和多因素分析結果。基于年齡、性別、種族、組織病理學亞型、病灶位置、病灶所在肺葉、病灶大小、分化程度、胸膜侵犯程度、輔助放療,對肺葉切除組患者和肺段切除組患者以2∶1進行傾向性評分匹配(propensity score matching,PSM)。采用Kaplan-Meier法繪制匹配后的生存曲線,利用log-rank檢驗比較兩組患者的生存差異,并進一步在不同患者亞組中比較肺段和肺葉切除對患者預后的影響。檢驗水準α=0.05。
1.4 倫理審查
本研究數據來源于SEER數據庫中的匿名和去識別數據。研究已獲得眉山市人民醫院醫學倫理審查委員會批準(2024-81)。
2 結果
2.1 患者基線特征
納入
 圖1
患者篩選流程圖
圖1
患者篩選流程圖
2.2 總生存的危險因素
以OS為結局,進行單因素Cox回歸分析,發現年齡、性別、種族、組織病理學亞型、腫瘤大小、分化程度、胸膜侵犯程度、腫瘤分期、手術方式、淋巴結清掃數目以及是否接受輔助放療對患者預后有顯著影響(P<0.01)。進一步多因素Cox回歸分析顯示,年齡>70歲、男性、白種人、腫瘤病理亞型為非腺癌的NSCLC(尤其是鱗癌)、腫瘤直徑>2 cm、分化程度低、接受肺段切除術、淋巴結清掃數目過少、接受過輔助放療是患者預后不良的高危因素(P<0.01);見表2。
2.3 亞組分析
對不同年齡段患者進行生存分析發現,60~70歲Ⅰ期NSCLC患者,接受肺葉切除后的10年OS率(P<0.01)和LCSS率(P=0.02)均顯著高于肺段切除患者。而對于>70歲患者,兩組手術方式的5年OS率(P=0.81)及10年OS率(P=0.06)差異無統計學意義;見圖3。
 圖3
傾向性評分匹配后不同年齡段患者生存比較
圖3
傾向性評分匹配后不同年齡段患者生存比較
a~b:分別為60~70歲患者OS和LCSS比較;c~d:分別為70~80歲患者OS和LCSS比較;e~f:分別為≥80歲患者OS和LCSS比較;OS:總生存;LCSS:肺癌特異性生存
進一步亞組分析顯示,對于年齡60~70歲、女性、白種人、腫瘤組織學亞型為肺腺癌、位于左肺及上葉、直徑>2 cm、分化程度較高、淋巴結清掃個數<10枚、術后不行化療/放療患者,肺葉切除術的OS及LCSS獲益均高于肺段切除術。而對于年齡70~80歲、黑種人、腫瘤位于下葉、直徑≤2 cm(ⅠA1~ⅠA2期),淋巴結清掃個數≥10枚,術后行化療/放療患者,肺段切除與肺葉切除對生存無顯著影響;見圖4~5。
 圖4
總生存的亞組分析森林圖
圖4
總生存的亞組分析森林圖
 圖5
肺癌特異性生存的亞組分析森林圖
圖5
肺癌特異性生存的亞組分析森林圖
3 討論
本研究基于SEER數據庫2010—2020年肺癌患者數據,通過PSM,探究了老年Ⅰ期NSCLC患者接受肺葉切除和肺段切除術的預后差異。總體分析結果提示,與肺段切除相比,肺葉切除能夠帶來更高的10年OS率和LCSS率。但進一步亞組分析發現,肺葉切除的優勢僅局限于60~70歲老年Ⅰ期NSCLC患者,對于>70歲患者,肺葉切除患者的生存率雖仍略高于肺段切除組,但差異無統計學意義。此外,在患者腫瘤直徑≤2 cm、分期較早(ⅠA1~ⅠA2期)、術中確保淋巴結清掃質量、術后行輔助放/化療等特定情況下,肺段切除也能帶來與肺葉切相似的遠期預后。
老年Ⅰ期NSCLC患者手術方式選擇問題一直備受國內外關注。對于肺葉和肺段對圍術期結局的比較,一項基于10家中國三甲醫院數據的回顧性研究[13]結果顯示,>65歲的老年Ⅰ期NSCLC患者中,亞肺葉切除術更常用于年齡大、合并癥多、腫瘤較小、位于左側、組織學亞型為腺癌的患者;肺段切除患者術中失血量更少,手術時間、術后置管時間及住院時間明顯縮短,且短期生存與肺葉切除術無顯著差異。但本研究中,肺段組患者淋巴結切除個數顯著少于肺葉組,肺段切除對N分期、局部復發和長期預后的影響尚不明確。另一項來自瑞士的單中心回顧性研究[14]顯示,對于直徑<2 cm的實性NSCLC,腔鏡下肺段切除與肺葉切除患者的短期內局部復發情況相似[中位隨訪時間:23(6~38.5)個月]。而針對長期預后的比較,一項基于SEER數據庫的回顧性研究[15]發現,肺葉切除相比亞肺葉切除并不會為>70歲、ⅠA期、腫瘤直徑≤3 cm的老年NSCLC患者帶來更多的遠期生存(LCSS)獲益。而日本的大型多中心隨機對照試驗(JCOG0802/WJOG4607L)[3]公布的結果則顯示,對于腫瘤大小≤2 cm、純實性的周圍型早期肺癌,肺段切除術相比肺葉切除術在提高5年OS率方面更有優勢,尤其是針對>70歲患者[肺葉切除:77.1%,95%CI(68.2,83.8)],肺段切除:85.6%,95%CI(77.5,90.9),P<0.01]。然而,兩組患者的總體局部復發率雖無顯著差異,但對于<70歲女性患者,肺段切除患者5年內疾病復發風險顯著高于肺葉切除患者[HR=4.10,95%CI(1.36,12.38),P<0.01]。值得注意的是,JCOG0802/WJOG4607L研究中,>70歲且腫瘤大小≤2 cm、接受肺段切除患者的5年OS率顯著高于我們基于北美SEER數據庫分析得出的結果[69.60%,95%CI(63.50,76.40)]。而我們對>70歲且腫瘤大小≤2 cm人群的比較結果顯示,肺段切除患者的5年OS率不差于肺葉切除[72.74%,95%CI(68.85,76.85),P=0.37]。這可能與人種、不同地區手術方式及圍術期管理等差異有關[16]。
綜合以上研究結果,我們認為:相比于肺段切除術,肺葉切除術能夠更全面地清除腫瘤病灶,并且清掃的淋巴結數目相對更多,可確保更為精確的肺癌病理分期及治療方案選擇[17],有效降低疾病復發風險,為大部分患者帶來更優的OS。然而,對于部分年齡較大的患者(如>70歲),其身體狀況較差,術后康復能力較弱,加之預期壽命有限,即使采用肺葉切除術,長期預后及生活質量也不一定優于其他手術方式。此外,對于腫瘤直徑較小(≤2 cm)和分期較早(ⅠA1~ⅠA2期)的患者,由于腫瘤本身的惡性程度較低,尤其是腺癌早期病變及含有GGO成分的肺結節[18-19],即使采用肺段切除術,遠期預后也不會顯著差于肺葉切除術。除以上結論外,盡管目前的循證證據[20]及本研究結果均不支持Ⅰ期NSCLC患者在接受標準手術切除方案(肺葉切除術)后行輔助化療,本研究結果提示,肺段切除術后行放/化療可能改善長期預后。但這一結論還需進一步通過大樣本研究證實。
本研究存在一些不足。首先,本研究是一項回顧性研究,不可避免存在選擇偏倚,但本研究使用了PSM方法,盡量減小了基線差異對結果造成的偏倚。其次,本研究從人口學特征、病灶特點和手術信息等方面研究了不同肺手術切除范圍的預后差異,但受限于SEER數據庫本身的信息完整度,仍有一些指標未納入分析,如合并癥、肺功能、腫瘤實性成分占比、手術方式(腔鏡或者開胸,聯合切除)、淋巴結清掃站數等。另外,SEER數據庫為北美腫瘤登記數據庫,患者中白種人占比顯著高于其他人種,因此考慮人種、手術方式及手術開展中心的差異,應謹慎對待本研究結論,其對中國臨床的適用性待進一步驗證。最后,在生存數據方面,詳細的復發、轉移數據不全,這也限制了對結果的深入分析。期待未來多中心、大樣本研究結果(如STEPS研究[21]等)為中國Ⅰ期NSCLC老年患者的術式選擇提供更高質量的臨床指導。
綜上,本研究基于SEER數據庫的分析結果提示,對于老年Ⅰ期NSCLC患者,肺葉切除對改善OS和LCSS更具優勢。但對年齡>70歲、腫瘤直徑≤2 cm、分期為ⅠA1~ⅠA2期等特定類型患者,在確保淋巴結清掃質量和精確病理分期的基礎上,肺段切術是可行的。因此,在決定老年Ⅰ期NSCLC患者手術切除范圍時,應綜合考慮個體差異、腫瘤特征和圍術期治療方案。
利益沖突:無。
作者貢獻:崔輝主導研究實施,負責選題與設計,崔輝、石勇、余永康負責數據搜集和整理;崔輝、胡祥負責數據分析;全體作者參與論文撰寫和修改。