慢性咳嗽作為一種肺癌術后常見的保護性反應,不但延長了患者住院時間,也加劇呼吸功能障礙,嚴重影響患者的康復進程和生活質量[1]。根據Sun 等[2]的研究,506例肺癌手術患者中,咳嗽的發病率達到25.69%,且麻醉持續時間與胃食管反流被認為是咳嗽的潛在風險因素。多項研究[3-4]表明,慢性咳嗽與氣道炎癥、神經系統激活以及氣道結構重塑相關,持續刺激可能導致氣道功能惡化,促進慢性炎癥,并觸發免疫系統反應,釋放炎癥介質,進一步損傷氣道。慢性咳嗽的診斷通常依據臨床表現、實驗室檢測和肺功能評估,而其治療主要依賴藥物治療、行為調整及環境控制,由于病情的復雜性和治療反應的個體差異,患者長期預后常常不佳,不僅加重醫療負擔,也降低患者生活質量[5-6]。美國胸科學會對慢性咳嗽進行詳細分類,雖能有效揭示不同病因,但在預測長期效果方面尚有不足,因而準確地預測慢性咳嗽的長期預后顯得格外重要[7]。血液生物標志物因其檢測便捷、快速而成為預后評估的重要工具,Periostin 在呼吸系統疾病中通常與細胞外基質的重塑相關,可影響氣道的敏感性和反應性,在咳嗽的觸發中扮演重要角色[8];白介素-33(interleukin-33,IL-33)作為一種促炎細胞因子,能激活免疫細胞并誘發多種細胞因子的釋放,加劇氣道的炎癥反應,增加咳嗽反射的敏感性,但二者在預測慢性咳嗽的研究較少[9]。冠狀動脈旁路移植術(coronary artery bypass grafting,CABG)合并肺癌患者具有獨特的特點,區別于單純肺癌患者,存在心臟病史,使得其手術復雜性增加,術后并發癥風險更高,慢性咳嗽在這一人群中尤為常見,不僅影響術后心肺功能的恢復,還加重患者整體康復難度,因而本文探討Periostin、IL-33與CABG合并肺癌患者胸腔鏡肺葉切除術后慢性咳嗽的相關性,以期為慢性咳嗽的臨床預測和治療提供新的參考。
1 資料與方法
1.1 臨床資料
本文為前瞻性研究,在我院2022年1月—2024年1月期間,共計收治134例肺癌合并冠心病患者。
納入標準:(1)年齡≥18歲且已接受CABG;(2)患者術前凝血功能正常、肝功能穩定、營養狀況優良,可承受兩次手術操作;(3)根據胸部CT結果,腫瘤適合進行肺葉切除術,無遠處轉移跡象,腫瘤單一,直徑<4 cm,在手術過程中無需轉為開胸手術,術后病理確診為肺癌;(4)心肺功能穩定,足以耐受胸腔鏡肺葉切除術及其恢復期;(5)患者已書面同意參與本研究,并愿意遵循研究協議進行后續的隨訪工作。
排除標準:(1)存在慢性阻塞性肺疾病或其他嚴重影響呼吸功能的慢性疾病;(2)存在其他癌癥的并發癥或同時接受其他重大手術的患者;(3)有長期或大劑量使用免疫抑制劑或皮質類固醇的歷史;(4)存在嚴重精神病或行為障礙,可能無法遵守醫療指導或研究程序的患者;(5)無法進行標準化的生物標志物采集或數據記錄不完整的患者。
1.2 治療方法
所有患者均成功接受CABG術并進行胸腔鏡肺葉切除術。術前評估:包括病史詢問、體征檢查、肺功能和心電圖測試,以及胸部CT確認腫瘤位置、大小和是否轉移。多學科會診由腫瘤科、胸外科和麻醉科共同評估患者手術適應性。術中:在全身麻醉下進行生命體征監控,通過側胸部切口植入胸腔鏡,探查并分離肺組織,切除肺葉后止血和檢查氣體泄漏,安置引流管以排出術后積液和氣體,縫合傷口。術后護理:包括疼痛管理、早期呼吸康復、引流管監測和拔除,以及術后活動促進。定期隨訪安排胸部X光和肺功能評估,以監測恢復及復發情況。
1.3 基線資料收集
收集CABG合并肺癌患者的初始資料:(1)基本信息:年齡,性別,體重指數,生活習慣(吸煙史:記錄患者是否吸煙,吸煙年數及每日吸煙量;飲酒史:記錄患者是否飲酒,飲酒頻率及種類),高血壓,糖尿病。(2)臨床癥狀:術前咳嗽。(3)手術情況:手術范圍,病理類型,NM分期,淋巴結清除數,氣管插管時間,腫瘤位置。(4)術后情況:術后是否胃酸反流。
1.4 血清Periostin和IL-33
采集患者晨起時自肘部靜脈取血5 mL,靜置0.5 h后,使用Allegra型號離心機(Beckman Coulter)以4 000轉/min(離心半徑為15 cm)離心10 min,用于分離血清。利用酶聯免疫吸附試驗進行血清中Periostin和IL-33的水平檢測,Multiskan FC型號酶標儀由美國賽默飛世爾科技公司提供。
1.5 術后慢性咳嗽
術后慢性咳嗽為持續≥8周的干咳,胸部X線復查未發現明顯問題,此癥狀需藥物介入治療。采用VAS量表來測量患者咳嗽的存在及其嚴重程度,評分范圍為0~10分。當VAS評分≥4分,表明咳嗽影響患者的睡眠質量,這些病例通常需要藥物干預。術前1 d,評定患者是否有咳嗽癥狀。術后3個月內,通過門診或電話跟蹤咳嗽情況,若VAS評分≥4分,診斷為術后慢性咳嗽[10]。
1.6 統計學學分析
采用SPSS 25.0軟件進行統計分析。正態分布的計量資料以均數±標準差(x±s)描述,組間比較采用獨立樣本t檢驗。不同時間點的數據經重復測量ANOVA進行比較。計數資料以百分比(%)描述,組間比較采用四格表χ2檢驗。相關性通過Pearson方法分析。Logistic回歸分析術后慢性咳嗽的影響因素。使用ROC曲線評價Periostin和IL-33在預測慢性咳嗽方面的效能。雙側P≤0.05為差異有統計學意義。
1.7 倫理審查
本研究已通過天津市胸科醫院醫學倫理委員會批準,倫理號:2024YS-058-01。
2 結果
2.1 兩組患者Periostin和IL-33比較
慢性咳嗽組中外周血Periostin和IL-33水平在各時間點(第7天和14天)均顯著高于非慢性咳嗽組,并且在組間和時間點之間存在顯著的交互作用(均P<0.001);見表1。
2.2 相關性分析
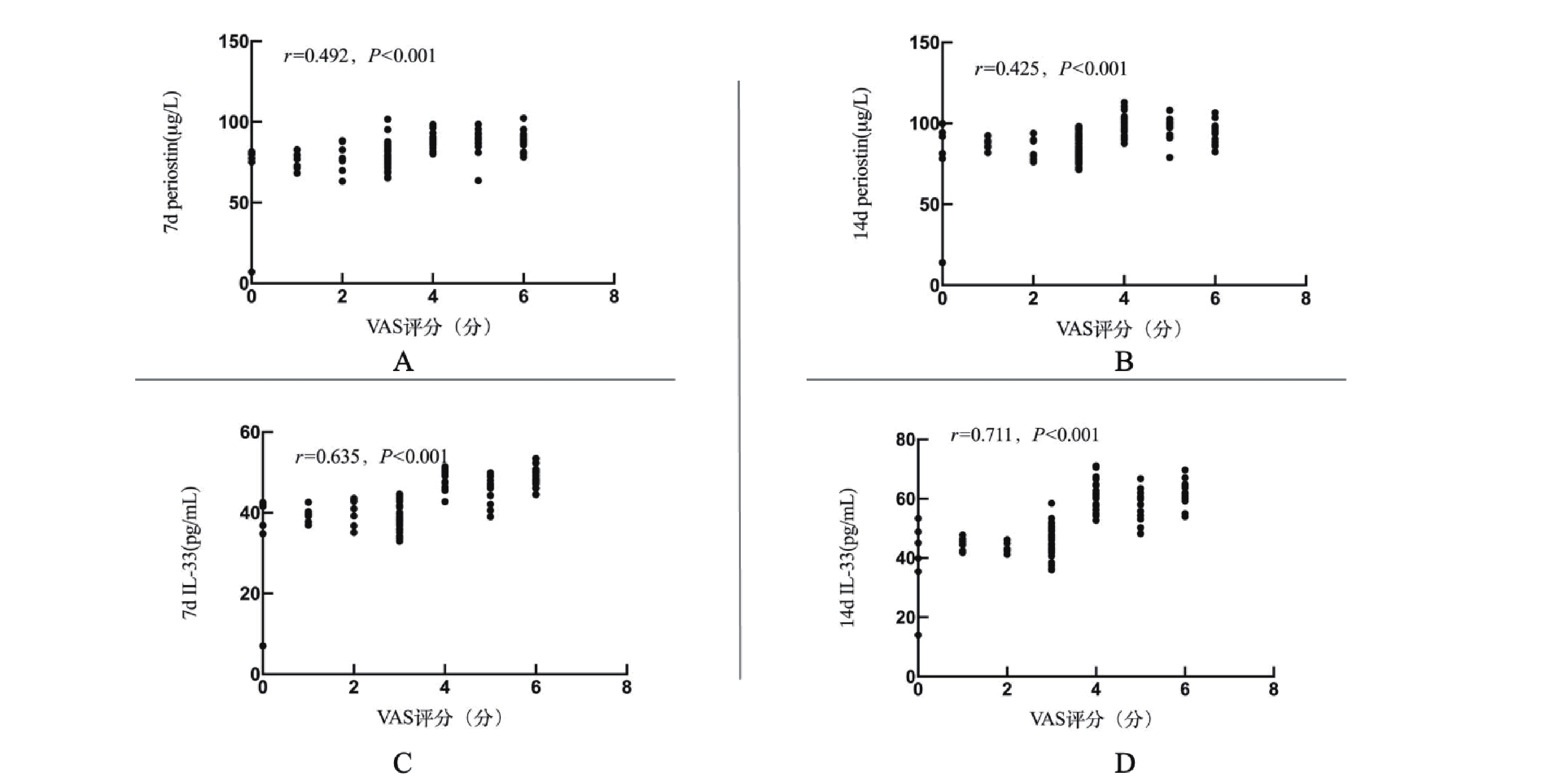
肺癌患者咳嗽程度評分為(3.44±1.60)分,咳嗽程度評分與7 d Periostin和14 d Periostin、7 d IL-33和14 d IL-33呈正相關(P<0.05);而與1 d Periostin和1 d IL-33無關(P>0.05);見圖1。
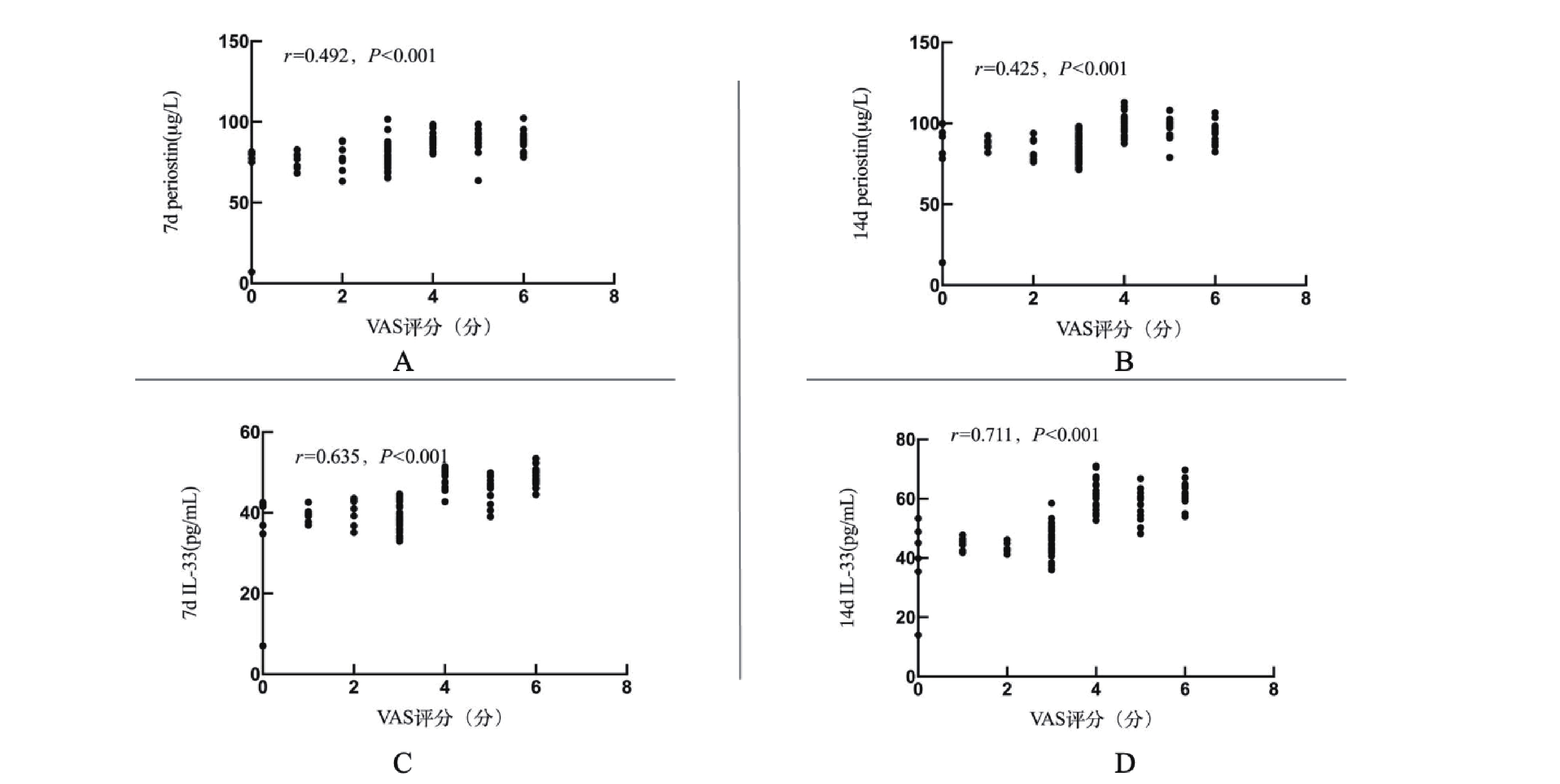 圖1
外周血Periostin和IL-33與咳嗽嚴重程度評分相關性
圖1
外周血Periostin和IL-33與咳嗽嚴重程度評分相關性
a~b:肺癌患者咳嗽程度評分與7 d、14 d Periostin相關性;c~d:肺癌患者咳嗽程度評分與7 d、14 d IL-33相關性
2.3 兩組臨床資料對比
慢性咳嗽組和非慢性咳嗽組患者在基本信息、生活習慣、健康狀況、臨床癥狀、手術詳情及術后情況等基線資料均無顯著差異(P>0.05);見表2。
2.4 肺癌患者慢性咳嗽多因素logistic回歸分析
利用logistic回歸方法,篩選出在統計上具有顯著性的變量作為獨立因子,以慢性咳嗽為因應變量進行分析。將“是否發生慢性咳嗽”設為變量“Y”,賦值為“否”=0,“是”=1;將7 d Periostin、14 d Periostin、7 d IL-33、14 d IL-33分別設為變量“X1”“X2”“X3”“X4”,為連續變量。結果表明,各變量間不存在共線性問題。在術后7 d和14 d的Periostin以及IL-33水平均是CABG合并肺癌患者在肺葉切除術后發生慢性咳嗽的響因素;見表3。
2.5 外周血Periostin和IL-33對肺癌患者術后慢性咳嗽診斷效能
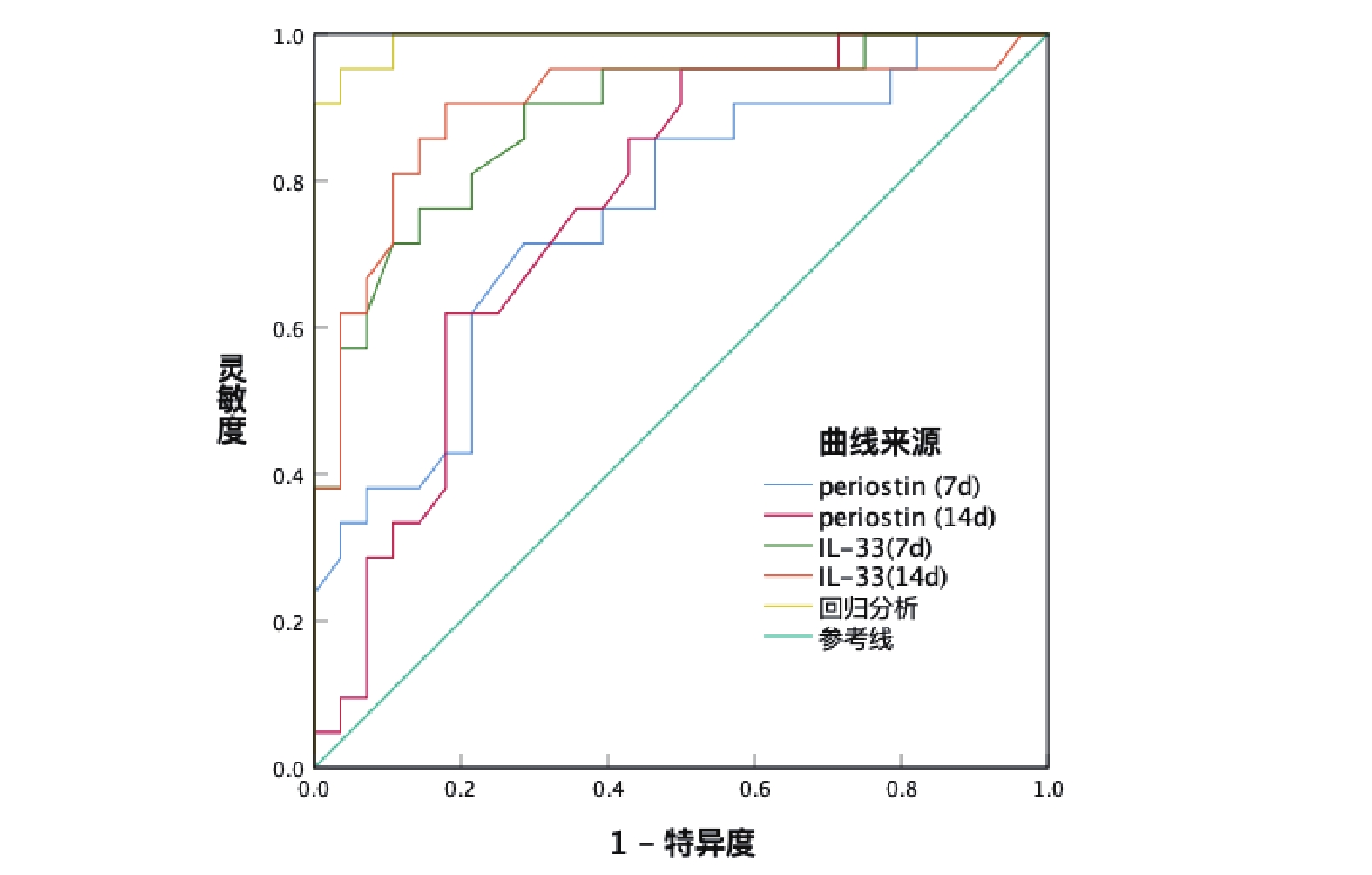
采用術后不同時間點外周血中Periostin和IL-33水平作為評估指標,以慢性咳嗽的發生作為狀態變量,并據此繪制ROC曲線。對于第7 d Periostin的分析顯示,其臨界值為79.20 μg/L,對應的靈敏度和特異度分別達到69.05%與71.67%,AUC為0.756[95%CI 0.616,0.893]。至于第14 d的Periostin,臨界值調整為88.81 μg/L,靈敏度提升至71.43%,特異度為76.67%,AUC評分為0.762[95%CI(0.633,0.898)]。第7 d IL-33的臨界值設為45.03 pg/mL,其靈敏度與特異度均為83.33%,AUC值高達0.884[95%CI(0.789,0.980)]。第14 d IL-33的臨界值設為56.01 pg/mL,靈敏度為85.71%,特異度為80.00%,AUC值為0.899[95%CI(0.799,0.999)]。進一步回歸分析表明,靈敏度為95.24%,特異度為95.00%,AUC異常高達0.993[95%CI(0.979,1.000)];見圖2。
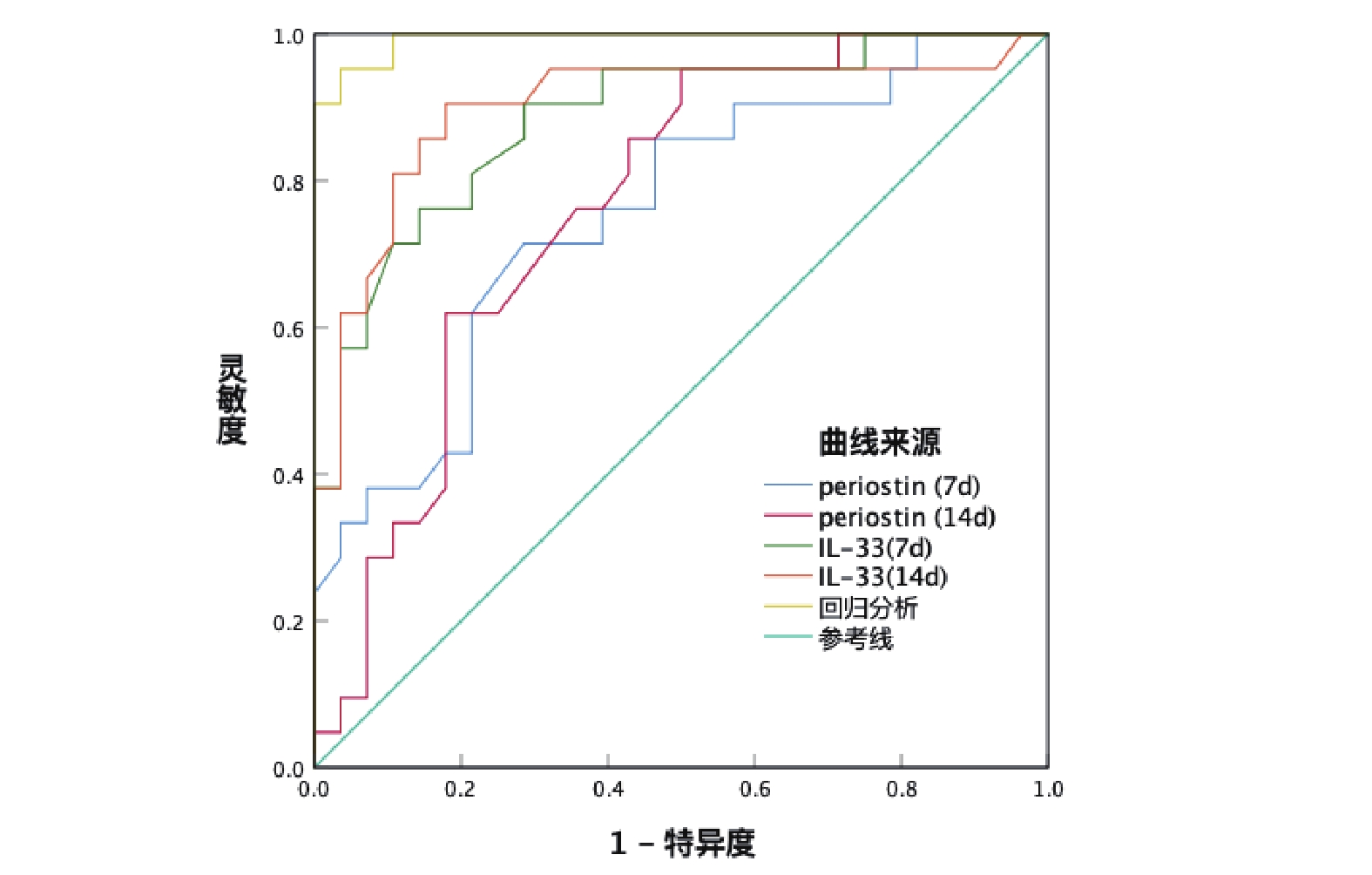 圖2
血清Periostin和IL-33對肺癌胸腔鏡肺葉切除術患者預后診斷效能
圖2
血清Periostin和IL-33對肺癌胸腔鏡肺葉切除術患者預后診斷效能
3 討論
在CABG和肺葉切除手術之后,慢性咳嗽經常出現,咳嗽誘發手術切口疼痛,不僅會延遲患者的康復,同時也會降低患者生活質量,與手術后肺部及氣道的生理變化相關,若慢性咳嗽持續存在,可引發更嚴重的呼吸功能衰退[11-12]。雖然已有眾多研究探討術后咳嗽的生理基礎,但臨床上仍缺少有效治療此癥狀的策略,目前的治療方法,包括藥物和呼吸康復,并不能徹底解決問題,因此針對手術后慢性咳嗽的預防及及早干預尤為關鍵。在細胞和分子水平上的機制探究,有助于發展更有效的治療方案,提升患者康復質量[13-14]。越來越多的研究[15]開始關注于諸如炎癥介質和細胞因子等生物標志物,這些標志物的變化與術后咳嗽的持續性和嚴重性密切相關,為早期診斷和個性化治療提供潛在靶向分子。
Periostin與慢性咳嗽的關系體現在其在氣道炎癥和氣道重塑的過程中發揮關鍵作用,增強Th2型免疫反應并激活嗜酸細胞和肥大細胞,直接參與炎癥介質的釋放,促進哮喘和其他氣道炎癥性疾病中的炎癥反應,導致慢性咳嗽的持續或加重[16]。IL-33是重要的促炎因子,與慢性咳嗽的發展密切相關,尤其在氣道上皮細胞受損時通過激活Th2型免疫反應釋放IL-5、IL-13等炎癥介質,激活嗜酸細胞和其他免疫細胞,維持慢性且持續的炎癥狀態[17]。本研究觀察到慢性咳嗽患者在癥狀發作后初期Periostin和IL-33水平顯著提高,并通過調節肺部炎癥和纖維化發揮作用,與疾病嚴重程度密切相關,提示阻斷Periostin和IL-33的信號通路可作為減輕慢性炎癥和組織纖維化的潛在治療策略,Periostin 在氣道重塑過程中也發揮著關鍵作用,可促進膠原蛋白的合成和沉積,加劇氣道壁的厚度和剛性,增加氣道反應性,且其水平升高常見于慢性咳嗽患者的血液和呼吸道分泌物中,使其成為潛在的生物標志物[18]。IL-33同樣參與氣道重塑,促使平滑肌增厚和細胞外基質的增加,導致氣道機械性質的改變,增強刺激反應性,加劇咳嗽的敏感性和頻率[19]。進一步通過單因素和多因素logistic回歸分析,發現Periostin和IL-33在不同時間點是慢性咳嗽預后不良的關鍵預測指標,揭示二者作為疾病監測和治療靶點的潛力,為未來的臨床藥物研發究提供重要的方向。
綜上所述,在CABG手術并發肺癌的患者中,通過胸腔鏡進行肺葉切除術后,Periostin和IL-33在不同時間點的表達水平顯著上升,且這種上升與患者咳嗽的嚴重程度有明顯的相關性。然而,本研究仍存在一些局限性,例如淋巴結清掃的站數可能影響術后咳嗽的發生率,但該因素在本研究未見顯著差異,未來的多中心、大樣本量研究將有助于驗證這些生物標志物在臨床中的預測價值。
利益沖突:無
作者貢獻:齊玉娟負責整項研究的設計、實施、進行及論文撰寫;白耀邦、焦妍負責收集患者血清,檢測相關因子;朱曉龍對患者進行隨訪并進行隨訪數據整理;付博負責數據分析及圖表整理;吳振華負責本研究進行及論文修改。
慢性咳嗽作為一種肺癌術后常見的保護性反應,不但延長了患者住院時間,也加劇呼吸功能障礙,嚴重影響患者的康復進程和生活質量[1]。根據Sun 等[2]的研究,506例肺癌手術患者中,咳嗽的發病率達到25.69%,且麻醉持續時間與胃食管反流被認為是咳嗽的潛在風險因素。多項研究[3-4]表明,慢性咳嗽與氣道炎癥、神經系統激活以及氣道結構重塑相關,持續刺激可能導致氣道功能惡化,促進慢性炎癥,并觸發免疫系統反應,釋放炎癥介質,進一步損傷氣道。慢性咳嗽的診斷通常依據臨床表現、實驗室檢測和肺功能評估,而其治療主要依賴藥物治療、行為調整及環境控制,由于病情的復雜性和治療反應的個體差異,患者長期預后常常不佳,不僅加重醫療負擔,也降低患者生活質量[5-6]。美國胸科學會對慢性咳嗽進行詳細分類,雖能有效揭示不同病因,但在預測長期效果方面尚有不足,因而準確地預測慢性咳嗽的長期預后顯得格外重要[7]。血液生物標志物因其檢測便捷、快速而成為預后評估的重要工具,Periostin 在呼吸系統疾病中通常與細胞外基質的重塑相關,可影響氣道的敏感性和反應性,在咳嗽的觸發中扮演重要角色[8];白介素-33(interleukin-33,IL-33)作為一種促炎細胞因子,能激活免疫細胞并誘發多種細胞因子的釋放,加劇氣道的炎癥反應,增加咳嗽反射的敏感性,但二者在預測慢性咳嗽的研究較少[9]。冠狀動脈旁路移植術(coronary artery bypass grafting,CABG)合并肺癌患者具有獨特的特點,區別于單純肺癌患者,存在心臟病史,使得其手術復雜性增加,術后并發癥風險更高,慢性咳嗽在這一人群中尤為常見,不僅影響術后心肺功能的恢復,還加重患者整體康復難度,因而本文探討Periostin、IL-33與CABG合并肺癌患者胸腔鏡肺葉切除術后慢性咳嗽的相關性,以期為慢性咳嗽的臨床預測和治療提供新的參考。
1 資料與方法
1.1 臨床資料
本文為前瞻性研究,在我院2022年1月—2024年1月期間,共計收治134例肺癌合并冠心病患者。
納入標準:(1)年齡≥18歲且已接受CABG;(2)患者術前凝血功能正常、肝功能穩定、營養狀況優良,可承受兩次手術操作;(3)根據胸部CT結果,腫瘤適合進行肺葉切除術,無遠處轉移跡象,腫瘤單一,直徑<4 cm,在手術過程中無需轉為開胸手術,術后病理確診為肺癌;(4)心肺功能穩定,足以耐受胸腔鏡肺葉切除術及其恢復期;(5)患者已書面同意參與本研究,并愿意遵循研究協議進行后續的隨訪工作。
排除標準:(1)存在慢性阻塞性肺疾病或其他嚴重影響呼吸功能的慢性疾病;(2)存在其他癌癥的并發癥或同時接受其他重大手術的患者;(3)有長期或大劑量使用免疫抑制劑或皮質類固醇的歷史;(4)存在嚴重精神病或行為障礙,可能無法遵守醫療指導或研究程序的患者;(5)無法進行標準化的生物標志物采集或數據記錄不完整的患者。
1.2 治療方法
所有患者均成功接受CABG術并進行胸腔鏡肺葉切除術。術前評估:包括病史詢問、體征檢查、肺功能和心電圖測試,以及胸部CT確認腫瘤位置、大小和是否轉移。多學科會診由腫瘤科、胸外科和麻醉科共同評估患者手術適應性。術中:在全身麻醉下進行生命體征監控,通過側胸部切口植入胸腔鏡,探查并分離肺組織,切除肺葉后止血和檢查氣體泄漏,安置引流管以排出術后積液和氣體,縫合傷口。術后護理:包括疼痛管理、早期呼吸康復、引流管監測和拔除,以及術后活動促進。定期隨訪安排胸部X光和肺功能評估,以監測恢復及復發情況。
1.3 基線資料收集
收集CABG合并肺癌患者的初始資料:(1)基本信息:年齡,性別,體重指數,生活習慣(吸煙史:記錄患者是否吸煙,吸煙年數及每日吸煙量;飲酒史:記錄患者是否飲酒,飲酒頻率及種類),高血壓,糖尿病。(2)臨床癥狀:術前咳嗽。(3)手術情況:手術范圍,病理類型,NM分期,淋巴結清除數,氣管插管時間,腫瘤位置。(4)術后情況:術后是否胃酸反流。
1.4 血清Periostin和IL-33
采集患者晨起時自肘部靜脈取血5 mL,靜置0.5 h后,使用Allegra型號離心機(Beckman Coulter)以4 000轉/min(離心半徑為15 cm)離心10 min,用于分離血清。利用酶聯免疫吸附試驗進行血清中Periostin和IL-33的水平檢測,Multiskan FC型號酶標儀由美國賽默飛世爾科技公司提供。
1.5 術后慢性咳嗽
術后慢性咳嗽為持續≥8周的干咳,胸部X線復查未發現明顯問題,此癥狀需藥物介入治療。采用VAS量表來測量患者咳嗽的存在及其嚴重程度,評分范圍為0~10分。當VAS評分≥4分,表明咳嗽影響患者的睡眠質量,這些病例通常需要藥物干預。術前1 d,評定患者是否有咳嗽癥狀。術后3個月內,通過門診或電話跟蹤咳嗽情況,若VAS評分≥4分,診斷為術后慢性咳嗽[10]。
1.6 統計學學分析
采用SPSS 25.0軟件進行統計分析。正態分布的計量資料以均數±標準差(x±s)描述,組間比較采用獨立樣本t檢驗。不同時間點的數據經重復測量ANOVA進行比較。計數資料以百分比(%)描述,組間比較采用四格表χ2檢驗。相關性通過Pearson方法分析。Logistic回歸分析術后慢性咳嗽的影響因素。使用ROC曲線評價Periostin和IL-33在預測慢性咳嗽方面的效能。雙側P≤0.05為差異有統計學意義。
1.7 倫理審查
本研究已通過天津市胸科醫院醫學倫理委員會批準,倫理號:2024YS-058-01。
2 結果
2.1 兩組患者Periostin和IL-33比較
慢性咳嗽組中外周血Periostin和IL-33水平在各時間點(第7天和14天)均顯著高于非慢性咳嗽組,并且在組間和時間點之間存在顯著的交互作用(均P<0.001);見表1。
2.2 相關性分析
肺癌患者咳嗽程度評分為(3.44±1.60)分,咳嗽程度評分與7 d Periostin和14 d Periostin、7 d IL-33和14 d IL-33呈正相關(P<0.05);而與1 d Periostin和1 d IL-33無關(P>0.05);見圖1。
 圖1
外周血Periostin和IL-33與咳嗽嚴重程度評分相關性
圖1
外周血Periostin和IL-33與咳嗽嚴重程度評分相關性
a~b:肺癌患者咳嗽程度評分與7 d、14 d Periostin相關性;c~d:肺癌患者咳嗽程度評分與7 d、14 d IL-33相關性
2.3 兩組臨床資料對比
慢性咳嗽組和非慢性咳嗽組患者在基本信息、生活習慣、健康狀況、臨床癥狀、手術詳情及術后情況等基線資料均無顯著差異(P>0.05);見表2。
2.4 肺癌患者慢性咳嗽多因素logistic回歸分析
利用logistic回歸方法,篩選出在統計上具有顯著性的變量作為獨立因子,以慢性咳嗽為因應變量進行分析。將“是否發生慢性咳嗽”設為變量“Y”,賦值為“否”=0,“是”=1;將7 d Periostin、14 d Periostin、7 d IL-33、14 d IL-33分別設為變量“X1”“X2”“X3”“X4”,為連續變量。結果表明,各變量間不存在共線性問題。在術后7 d和14 d的Periostin以及IL-33水平均是CABG合并肺癌患者在肺葉切除術后發生慢性咳嗽的響因素;見表3。
2.5 外周血Periostin和IL-33對肺癌患者術后慢性咳嗽診斷效能
采用術后不同時間點外周血中Periostin和IL-33水平作為評估指標,以慢性咳嗽的發生作為狀態變量,并據此繪制ROC曲線。對于第7 d Periostin的分析顯示,其臨界值為79.20 μg/L,對應的靈敏度和特異度分別達到69.05%與71.67%,AUC為0.756[95%CI 0.616,0.893]。至于第14 d的Periostin,臨界值調整為88.81 μg/L,靈敏度提升至71.43%,特異度為76.67%,AUC評分為0.762[95%CI(0.633,0.898)]。第7 d IL-33的臨界值設為45.03 pg/mL,其靈敏度與特異度均為83.33%,AUC值高達0.884[95%CI(0.789,0.980)]。第14 d IL-33的臨界值設為56.01 pg/mL,靈敏度為85.71%,特異度為80.00%,AUC值為0.899[95%CI(0.799,0.999)]。進一步回歸分析表明,靈敏度為95.24%,特異度為95.00%,AUC異常高達0.993[95%CI(0.979,1.000)];見圖2。
 圖2
血清Periostin和IL-33對肺癌胸腔鏡肺葉切除術患者預后診斷效能
圖2
血清Periostin和IL-33對肺癌胸腔鏡肺葉切除術患者預后診斷效能
3 討論
在CABG和肺葉切除手術之后,慢性咳嗽經常出現,咳嗽誘發手術切口疼痛,不僅會延遲患者的康復,同時也會降低患者生活質量,與手術后肺部及氣道的生理變化相關,若慢性咳嗽持續存在,可引發更嚴重的呼吸功能衰退[11-12]。雖然已有眾多研究探討術后咳嗽的生理基礎,但臨床上仍缺少有效治療此癥狀的策略,目前的治療方法,包括藥物和呼吸康復,并不能徹底解決問題,因此針對手術后慢性咳嗽的預防及及早干預尤為關鍵。在細胞和分子水平上的機制探究,有助于發展更有效的治療方案,提升患者康復質量[13-14]。越來越多的研究[15]開始關注于諸如炎癥介質和細胞因子等生物標志物,這些標志物的變化與術后咳嗽的持續性和嚴重性密切相關,為早期診斷和個性化治療提供潛在靶向分子。
Periostin與慢性咳嗽的關系體現在其在氣道炎癥和氣道重塑的過程中發揮關鍵作用,增強Th2型免疫反應并激活嗜酸細胞和肥大細胞,直接參與炎癥介質的釋放,促進哮喘和其他氣道炎癥性疾病中的炎癥反應,導致慢性咳嗽的持續或加重[16]。IL-33是重要的促炎因子,與慢性咳嗽的發展密切相關,尤其在氣道上皮細胞受損時通過激活Th2型免疫反應釋放IL-5、IL-13等炎癥介質,激活嗜酸細胞和其他免疫細胞,維持慢性且持續的炎癥狀態[17]。本研究觀察到慢性咳嗽患者在癥狀發作后初期Periostin和IL-33水平顯著提高,并通過調節肺部炎癥和纖維化發揮作用,與疾病嚴重程度密切相關,提示阻斷Periostin和IL-33的信號通路可作為減輕慢性炎癥和組織纖維化的潛在治療策略,Periostin 在氣道重塑過程中也發揮著關鍵作用,可促進膠原蛋白的合成和沉積,加劇氣道壁的厚度和剛性,增加氣道反應性,且其水平升高常見于慢性咳嗽患者的血液和呼吸道分泌物中,使其成為潛在的生物標志物[18]。IL-33同樣參與氣道重塑,促使平滑肌增厚和細胞外基質的增加,導致氣道機械性質的改變,增強刺激反應性,加劇咳嗽的敏感性和頻率[19]。進一步通過單因素和多因素logistic回歸分析,發現Periostin和IL-33在不同時間點是慢性咳嗽預后不良的關鍵預測指標,揭示二者作為疾病監測和治療靶點的潛力,為未來的臨床藥物研發究提供重要的方向。
綜上所述,在CABG手術并發肺癌的患者中,通過胸腔鏡進行肺葉切除術后,Periostin和IL-33在不同時間點的表達水平顯著上升,且這種上升與患者咳嗽的嚴重程度有明顯的相關性。然而,本研究仍存在一些局限性,例如淋巴結清掃的站數可能影響術后咳嗽的發生率,但該因素在本研究未見顯著差異,未來的多中心、大樣本量研究將有助于驗證這些生物標志物在臨床中的預測價值。
利益沖突:無
作者貢獻:齊玉娟負責整項研究的設計、實施、進行及論文撰寫;白耀邦、焦妍負責收集患者血清,檢測相關因子;朱曉龍對患者進行隨訪并進行隨訪數據整理;付博負責數據分析及圖表整理;吳振華負責本研究進行及論文修改。