2022年中國的結直腸癌新發病例為517 106萬[1]。姚宏偉等[2]納入73個中心的結直腸癌病例83 063例分析結果顯示,結腸癌占比略低于直腸癌(42.4%比57.6%)。對于結腸癌患者,有53.5%接受腹腔鏡下完整結腸系膜切除,它具有較低的局部復發率以及較高的生存率[3]。腹腔鏡下右半結腸切除術經歷了多種入路方式[4],從傳統開腹手術時的外側入路到腹腔鏡下以腸系膜上血管為導向的中間入路,再到后來的從盲腸部位開始的尾側入路,甚或選擇切開胃結腸韌帶開始的頭側入路等,各入路方式優缺點各異,如外側入路不符合腫瘤根治的“No Touch”原則,中間入路技術操作復雜,尾側入路同樣面臨“No Touch”原則和技術困難問題。本研究團隊受腹腔鏡下胰十二指腸切除術式切開屈氏韌帶解剖胰頭和十二指腸的啟發,首次嘗試了行腹腔鏡下右半結腸切除術時從切開屈氏韌帶開始作為右半結腸切除的手術入路,現報道1例右半結腸癌患者采用該手術入路的治療過程及結果并總結經驗。
1 臨床資料
1.1 病例介紹
患者,男,67歲,以“右上腹間斷性脹痛不適2個月余”為主訴入院。患者于2個月余前無明顯誘因出現右上腹部疼痛不適,呈間斷性發作,進食后感癥狀明顯,無明顯惡心及嘔吐,無便血以及腹瀉病情。于青島大學附屬醫院外科門診就診,在門診以“升結腸癌”收住入青島大學附屬醫院胃腸外科。
1.2 專科查體
患者一般情況良好,腹平,無胃腸型及蠕動波,腹壁靜脈無迂曲;腹軟,肝脾肋緣下未及,膽囊未及,墨菲征(–),麥氏點無壓痛,右側上腹深壓痛,無反跳痛,未及任何質硬包塊;肝區以及雙側腎區無叩擊痛,移動性濁音(–);腸鳴音正常,4~5次/min;腹部血管雜音(–)。
1.3 實驗室檢查
入院后查血常規、肝功能、腎功能、血脂、電解質、凝血功能4項均在正常范圍內。腫瘤標志物甲胎蛋白、癌胚抗原、血清CA19-9、血清CA-50及糖類抗原72-4水平均正常;C-反應蛋白、白細胞介素6及降鈣素原水平均在正常范圍內。
1.4 入院前后輔助檢查
正常心電圖,心臟彩超射血分數值64%,正常肺功能。胸部CT平掃未見異常,腹部強化CT檢查見升結腸中上段局部腸壁不均勻增厚伴腸腔狹窄,臨床考慮升結腸癌并周圍淋巴結腫大(圖1a)。行結腸鏡檢查病理提示為低分化腺癌。
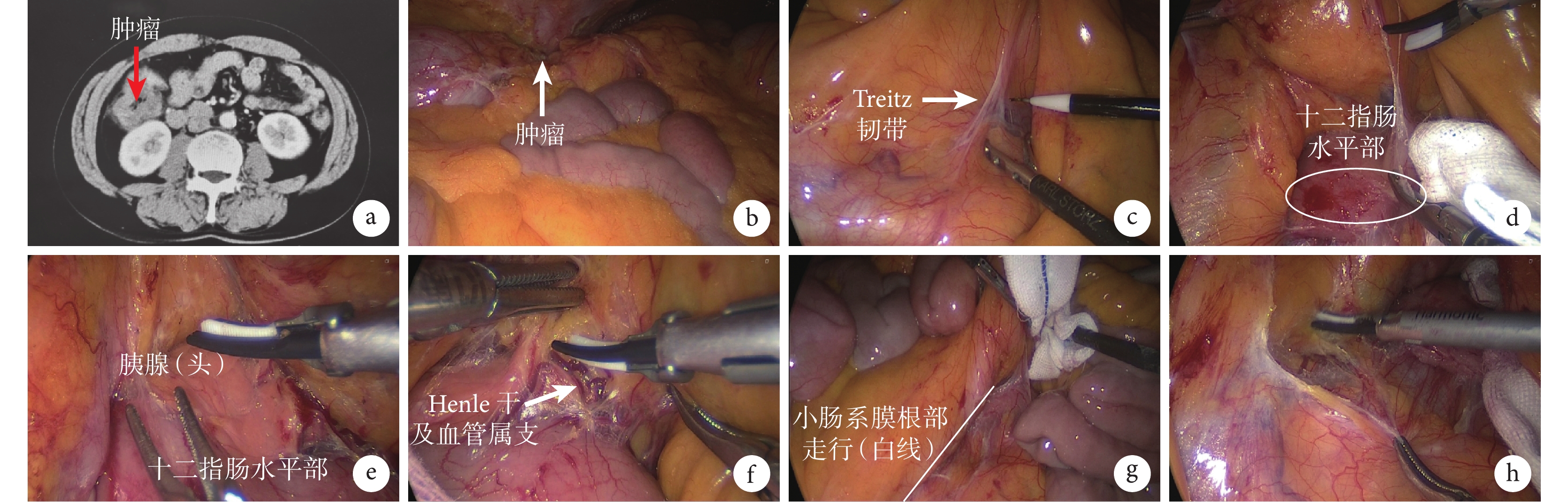 圖1
經屈氏韌帶入路切開路徑圖
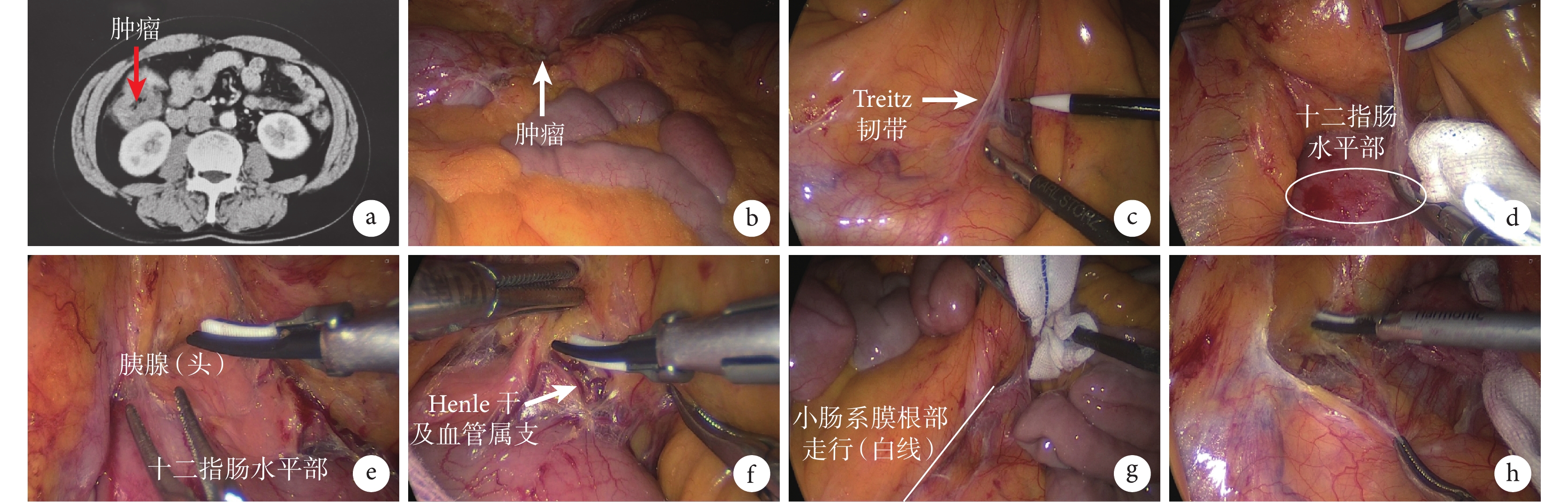
圖1
經屈氏韌帶入路切開路徑圖
a:CT下定位腫瘤;b:腹腔鏡下探查腫瘤;c:顯露屈氏韌帶;d:切開屈氏韌帶進入十二指腸水平部;e:進入胰腺前Toldt間隙;f:顯露 Henle干及各屬支;g:沿小腸系膜根部拓展間隙;h:擴大拓展胰頭十二指腸前間隙
1.5 術前評估
1.5.1 一般情況
患者身高169 cm,體質量67 kg,BMI 23.5 kg/m2。健康狀況良好,營養狀況良好。
1.5.2 麻醉評估
根據美國麻醉師協會評分系統評為Ⅰ級,無明顯麻醉禁忌證,可以耐受麻醉。
1.5.3 術前討論
患者升結腸惡性腫瘤病理診斷明確,未見有遠處轉移征象,具有明確手術指征且具備根治性切除術條件,可以實施腹腔鏡下右半結腸切除術;術前和患者家屬詳細溝通病情術前談話,簽署手術知情同意書,落實手術知情簽字制度。
1.6 手術步驟
① 體位:麻醉成功后,取患者平臥分腿位。② Trocar布置:術者站位于患者左側,助手站位于患者右側,扶鏡手立于患者兩腿之間。于臍下緣5 cm處穿刺Veress針建立氣腹,維持腹腔壓力12~14 mmHg(1 mmH=0.133 kPa),穿刺置入10 mm Trocar作為觀察孔,左上腹鎖骨中線穿刺10 mm Trocar作為術者主操作孔,左下腹反麥氏點穿刺5 mm Trocar為術者副操作孔,右下腹麥氏點位置5 mm Trocar作為助手主操作孔,右中腹鎖骨中線穿刺5 mm Trocar作助手副操作孔。③ 腹腔探查:常規探查腹腔內無腹水,肝臟表面光滑無結節,腹膜腔無轉移結節,盆腔無種植結節,腫瘤位于升結腸遠端近肝曲位置(圖1b),呈腫塊型生長,大小約5 cm×5 cm,侵及漿膜,術中確定可以行腹腔鏡下右半結腸切除術。④ 屈氏韌帶入路:改患者頭低足高15°,將橫結腸推向頭側,小腸推向右上腹,顯露屈氏韌帶,助手左手鉗向上張緊屈氏韌帶(圖1c),右手鉗沿著小腸系膜根部走形展拉,切開屈氏韌帶進入十二指腸水平部表面(圖1d),沿十二指腸水平部向患者右側游離進入胰腺前筋膜疏松的Toldt間隙內(圖1e),注意胰腺勾突的保護。⑤ Toldt間隙拓展:沿胰腺勾突前筋膜疏松的Toldt間隙向上拓展與橫結腸系膜后葉之間的間隙,清楚顯露 Henle干及各屬支(圖1f),塞紗布條作導引。沿小腸系膜根部向下向外側拓展,顯露腸系膜上血管(圖1g),并順勢進入升結腸后間隙。再次沿胰腺勾突以及十二指腸水平部平面間隙向患者右側拓展(圖1h),于十二指腸降段借勢下坡順勢拓展開腎前間隙并與已經拓展開的升結腸后間隙匯合,至此完成升結腸后間隙以及胰十二指腸前間隙的游離。⑥ 處理血管以及淋巴結清掃:助手張緊小腸系膜,術者沿腸系膜上靜脈以“揭房頂”方式分別處理回結腸血管,右結腸血管,結腸中動脈右支,副右結腸靜脈,血管根部分別Hemlock雙重結扎并完成淋巴結清掃。胃網膜弓下切開胃結腸韌帶,向患者右側解剖游離下結腸肝曲,至此完成右半結腸的間隙游離。⑦ 右上腹經腹直肌小切口加切口保護套,取出右半結腸,裁剪大網膜并分別裸化小腸以及橫結腸系膜,切除右半結腸行回腸與橫結腸側側吻合重建消化道,關閉共同開口,可吸收縫線漿肌層包埋縫合吻合口,徹底沖洗腹腔并止血,于右上腹放置腹腔引流管1枚,關閉腹腔結束手術。
1.7 術后匯總
該手術自屈氏韌帶入路開始至整個右半結腸間隙解剖完成包括淋巴結清掃用時約55 min,整個手術歷時約90 min(包括術中電勾損傷1處十二指腸漿膜層行腹腔鏡下縫合的時間),術中出血量為20 mL,術中補液量1 000 mL。結合科室加速康復外科舉措[5],患者返回病房清醒后進行簡單的床上活動手腳,術后第1天下床洗漱并自行活動,術后第2天患者排氣,患者恢復流質飲食,第4天恢復半流質軟食,排氣排便正常。患者術后狀況恢復順利,白細胞、血紅蛋白、C-反應蛋白均未見異常,術后每日引流液顏色正常且量均少于50 mL,無肺部感染、切口感染、腹腔出血、腹腔膿腫、吻合口出血、腸粘連等并發癥發生,于術后第6天順利出院。術后病理診斷:潰瘍型低分化腺癌,腫瘤大小5.5 cm×5.5 cm,侵及漿膜層;回腸切緣、結腸切緣、系膜切緣及大網膜均陰性;區域淋巴結:腸周(0/24),系膜區(0/7),中央區(0/7)。闌尾陰性。病理分期為pT3N0M0。
2 討論
1991年Jacobs等[6]首次報道了腹腔鏡下結腸癌切除術。對于腹腔鏡右半結腸切除術,入路選擇很重要。隨著膜解剖理念的更新以及解剖思路的改變,腹腔鏡下右半結腸切除術經歷了多種入路方式[4],經歷了三十余年的演變,一直不斷在發展和創新[7],從傳統開腹手術時的外側入路到腹腔鏡下廣泛開展的以腸系膜上血管為導向的中間入路,再到以盲腸部位開始的尾側入路,甚或選擇切開胃結腸韌帶開始的頭側入路,因習慣不同而優缺點各異,比如外側入路是基于既往傳統開腹手術入路,很容易引起術者深入至腎周脂肪層且游離初始時即可能接觸腫瘤處結腸,這不符合腫瘤根治的“No Touch”原則,這種手術入路于當今腹腔鏡手術中基本已被棄用[8]。目前開展最多的是以腸系膜上靜脈為導向的中間入路,開始于回結腸血管的識別,沿腸系膜上靜脈表面向上游離處理沿途血管,這一手術入路在早期即識別右側輸尿管和生殖血管,最大限度地減少了手術過程中的并發癥[9],但此種入路對于系膜肥厚或水腫嚴重患者因腸系膜太厚所致的血管標志識別較為困難,不易進入Toldt,s融合筋膜間隙,再就是在回結腸血管上方術者向胰頭方向游離解剖時的“爬坡”過程是其技術難點,稍有不慎很容易進入十二指腸后方[10]。尾側入路可以更好地進入間隙,但對于回盲部腫瘤來說也容易違反腫瘤根治的“No Touch”原則,且需要面臨的技術難點也是在十二指腸降段右側以及水平部的下方分別解剖游離時“爬坡”的操作過程。
本團隊回顧右半結腸切除術中以胰頭和十二指腸為導向的思路,受腹腔鏡下胰十二指腸切除術過程中切開屈氏韌帶解剖胰頭和十二指腸的啟發,嘗試行腹腔鏡下右半結腸切除術時從切開屈氏韌帶作為開拓右半結腸各間隙的入路,其優點是能輕松進入十二指腸以及胰頭前方疏松間隙,直接游離出導向標志胰頭以及十二指腸并分別向下以及向上拓展,且在游離十二指腸降段以及水平段時變既往傳統方式的“爬坡”操作為“下坡”操作,能快速游離出整個升結腸后間隙,結合腹腔鏡視野下“挖地洞、打隧道,拆房頂”等[11-12]手術技巧進行血管脈絡化操作以及淋巴結清掃。該入路術式優先切開屈氏韌帶游離并進入腹膜后胰頭前間隙,游離過程中部分即已顯露右結腸動脈、靜脈、胃結腸干和腸系膜上靜脈的走行,因此即使遇到血管大出血也可以迅速、容易地處理這種情況。手術團隊完成本例患者手術,自屈氏韌帶入路切開開始至整個右半結腸間隙解剖完成包括淋巴結清掃耗時僅約55 min,而整個手術時間約90 min(包括術中電勾損傷1處十二指腸漿膜層行腹腔鏡下縫合的時間),術中出血量約為 20 mL,該入路具有操作過程簡單,解剖精準,導向清晰等優點,但其缺點是胰頭前間隙血管豐富,操作不慎時可能容易導致血管出血。此入路路徑優先進行便于初次實踐者掌握,但仍需要具有豐富的腹腔鏡下右半結腸切除術手術經驗者實施,且對助手的配合要求相對較高。筆者手術團隊首次嘗試該入路且僅行1例操作,具有一定的局限性,短期手術效果良好,但遠期腫瘤安全性有待進一步的考證,實踐經驗尚需進一步總結,以便更好的推廣該入路術式,相應還可以在該術式基礎上進行其他多方位的實驗研究。腹腔鏡下右半結腸切除術應該是以聯合入路為基礎的操作過程,我們嘗試了經屈氏韌帶路徑優先的入路方式進行,希望為臨床工作者提供一個可行的思路。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:江海濤教授以及劉曉東教授提供寫作思路,邢智遠博士執筆成稿,另外致謝青島大學附屬醫院感染科張鳳娟教授文筆潤色。
倫理聲明:本研究通過了青島大學附屬醫院醫學倫理委員會審批(批文編號: QYFYWZLL28740)。
2022年中國的結直腸癌新發病例為517 106萬[1]。姚宏偉等[2]納入73個中心的結直腸癌病例83 063例分析結果顯示,結腸癌占比略低于直腸癌(42.4%比57.6%)。對于結腸癌患者,有53.5%接受腹腔鏡下完整結腸系膜切除,它具有較低的局部復發率以及較高的生存率[3]。腹腔鏡下右半結腸切除術經歷了多種入路方式[4],從傳統開腹手術時的外側入路到腹腔鏡下以腸系膜上血管為導向的中間入路,再到后來的從盲腸部位開始的尾側入路,甚或選擇切開胃結腸韌帶開始的頭側入路等,各入路方式優缺點各異,如外側入路不符合腫瘤根治的“No Touch”原則,中間入路技術操作復雜,尾側入路同樣面臨“No Touch”原則和技術困難問題。本研究團隊受腹腔鏡下胰十二指腸切除術式切開屈氏韌帶解剖胰頭和十二指腸的啟發,首次嘗試了行腹腔鏡下右半結腸切除術時從切開屈氏韌帶開始作為右半結腸切除的手術入路,現報道1例右半結腸癌患者采用該手術入路的治療過程及結果并總結經驗。
1 臨床資料
1.1 病例介紹
患者,男,67歲,以“右上腹間斷性脹痛不適2個月余”為主訴入院。患者于2個月余前無明顯誘因出現右上腹部疼痛不適,呈間斷性發作,進食后感癥狀明顯,無明顯惡心及嘔吐,無便血以及腹瀉病情。于青島大學附屬醫院外科門診就診,在門診以“升結腸癌”收住入青島大學附屬醫院胃腸外科。
1.2 專科查體
患者一般情況良好,腹平,無胃腸型及蠕動波,腹壁靜脈無迂曲;腹軟,肝脾肋緣下未及,膽囊未及,墨菲征(–),麥氏點無壓痛,右側上腹深壓痛,無反跳痛,未及任何質硬包塊;肝區以及雙側腎區無叩擊痛,移動性濁音(–);腸鳴音正常,4~5次/min;腹部血管雜音(–)。
1.3 實驗室檢查
入院后查血常規、肝功能、腎功能、血脂、電解質、凝血功能4項均在正常范圍內。腫瘤標志物甲胎蛋白、癌胚抗原、血清CA19-9、血清CA-50及糖類抗原72-4水平均正常;C-反應蛋白、白細胞介素6及降鈣素原水平均在正常范圍內。
1.4 入院前后輔助檢查
正常心電圖,心臟彩超射血分數值64%,正常肺功能。胸部CT平掃未見異常,腹部強化CT檢查見升結腸中上段局部腸壁不均勻增厚伴腸腔狹窄,臨床考慮升結腸癌并周圍淋巴結腫大(圖1a)。行結腸鏡檢查病理提示為低分化腺癌。
 圖1
經屈氏韌帶入路切開路徑圖
圖1
經屈氏韌帶入路切開路徑圖
a:CT下定位腫瘤;b:腹腔鏡下探查腫瘤;c:顯露屈氏韌帶;d:切開屈氏韌帶進入十二指腸水平部;e:進入胰腺前Toldt間隙;f:顯露 Henle干及各屬支;g:沿小腸系膜根部拓展間隙;h:擴大拓展胰頭十二指腸前間隙
1.5 術前評估
1.5.1 一般情況
患者身高169 cm,體質量67 kg,BMI 23.5 kg/m2。健康狀況良好,營養狀況良好。
1.5.2 麻醉評估
根據美國麻醉師協會評分系統評為Ⅰ級,無明顯麻醉禁忌證,可以耐受麻醉。
1.5.3 術前討論
患者升結腸惡性腫瘤病理診斷明確,未見有遠處轉移征象,具有明確手術指征且具備根治性切除術條件,可以實施腹腔鏡下右半結腸切除術;術前和患者家屬詳細溝通病情術前談話,簽署手術知情同意書,落實手術知情簽字制度。
1.6 手術步驟
① 體位:麻醉成功后,取患者平臥分腿位。② Trocar布置:術者站位于患者左側,助手站位于患者右側,扶鏡手立于患者兩腿之間。于臍下緣5 cm處穿刺Veress針建立氣腹,維持腹腔壓力12~14 mmHg(1 mmH=0.133 kPa),穿刺置入10 mm Trocar作為觀察孔,左上腹鎖骨中線穿刺10 mm Trocar作為術者主操作孔,左下腹反麥氏點穿刺5 mm Trocar為術者副操作孔,右下腹麥氏點位置5 mm Trocar作為助手主操作孔,右中腹鎖骨中線穿刺5 mm Trocar作助手副操作孔。③ 腹腔探查:常規探查腹腔內無腹水,肝臟表面光滑無結節,腹膜腔無轉移結節,盆腔無種植結節,腫瘤位于升結腸遠端近肝曲位置(圖1b),呈腫塊型生長,大小約5 cm×5 cm,侵及漿膜,術中確定可以行腹腔鏡下右半結腸切除術。④ 屈氏韌帶入路:改患者頭低足高15°,將橫結腸推向頭側,小腸推向右上腹,顯露屈氏韌帶,助手左手鉗向上張緊屈氏韌帶(圖1c),右手鉗沿著小腸系膜根部走形展拉,切開屈氏韌帶進入十二指腸水平部表面(圖1d),沿十二指腸水平部向患者右側游離進入胰腺前筋膜疏松的Toldt間隙內(圖1e),注意胰腺勾突的保護。⑤ Toldt間隙拓展:沿胰腺勾突前筋膜疏松的Toldt間隙向上拓展與橫結腸系膜后葉之間的間隙,清楚顯露 Henle干及各屬支(圖1f),塞紗布條作導引。沿小腸系膜根部向下向外側拓展,顯露腸系膜上血管(圖1g),并順勢進入升結腸后間隙。再次沿胰腺勾突以及十二指腸水平部平面間隙向患者右側拓展(圖1h),于十二指腸降段借勢下坡順勢拓展開腎前間隙并與已經拓展開的升結腸后間隙匯合,至此完成升結腸后間隙以及胰十二指腸前間隙的游離。⑥ 處理血管以及淋巴結清掃:助手張緊小腸系膜,術者沿腸系膜上靜脈以“揭房頂”方式分別處理回結腸血管,右結腸血管,結腸中動脈右支,副右結腸靜脈,血管根部分別Hemlock雙重結扎并完成淋巴結清掃。胃網膜弓下切開胃結腸韌帶,向患者右側解剖游離下結腸肝曲,至此完成右半結腸的間隙游離。⑦ 右上腹經腹直肌小切口加切口保護套,取出右半結腸,裁剪大網膜并分別裸化小腸以及橫結腸系膜,切除右半結腸行回腸與橫結腸側側吻合重建消化道,關閉共同開口,可吸收縫線漿肌層包埋縫合吻合口,徹底沖洗腹腔并止血,于右上腹放置腹腔引流管1枚,關閉腹腔結束手術。
1.7 術后匯總
該手術自屈氏韌帶入路開始至整個右半結腸間隙解剖完成包括淋巴結清掃用時約55 min,整個手術歷時約90 min(包括術中電勾損傷1處十二指腸漿膜層行腹腔鏡下縫合的時間),術中出血量為20 mL,術中補液量1 000 mL。結合科室加速康復外科舉措[5],患者返回病房清醒后進行簡單的床上活動手腳,術后第1天下床洗漱并自行活動,術后第2天患者排氣,患者恢復流質飲食,第4天恢復半流質軟食,排氣排便正常。患者術后狀況恢復順利,白細胞、血紅蛋白、C-反應蛋白均未見異常,術后每日引流液顏色正常且量均少于50 mL,無肺部感染、切口感染、腹腔出血、腹腔膿腫、吻合口出血、腸粘連等并發癥發生,于術后第6天順利出院。術后病理診斷:潰瘍型低分化腺癌,腫瘤大小5.5 cm×5.5 cm,侵及漿膜層;回腸切緣、結腸切緣、系膜切緣及大網膜均陰性;區域淋巴結:腸周(0/24),系膜區(0/7),中央區(0/7)。闌尾陰性。病理分期為pT3N0M0。
2 討論
1991年Jacobs等[6]首次報道了腹腔鏡下結腸癌切除術。對于腹腔鏡右半結腸切除術,入路選擇很重要。隨著膜解剖理念的更新以及解剖思路的改變,腹腔鏡下右半結腸切除術經歷了多種入路方式[4],經歷了三十余年的演變,一直不斷在發展和創新[7],從傳統開腹手術時的外側入路到腹腔鏡下廣泛開展的以腸系膜上血管為導向的中間入路,再到以盲腸部位開始的尾側入路,甚或選擇切開胃結腸韌帶開始的頭側入路,因習慣不同而優缺點各異,比如外側入路是基于既往傳統開腹手術入路,很容易引起術者深入至腎周脂肪層且游離初始時即可能接觸腫瘤處結腸,這不符合腫瘤根治的“No Touch”原則,這種手術入路于當今腹腔鏡手術中基本已被棄用[8]。目前開展最多的是以腸系膜上靜脈為導向的中間入路,開始于回結腸血管的識別,沿腸系膜上靜脈表面向上游離處理沿途血管,這一手術入路在早期即識別右側輸尿管和生殖血管,最大限度地減少了手術過程中的并發癥[9],但此種入路對于系膜肥厚或水腫嚴重患者因腸系膜太厚所致的血管標志識別較為困難,不易進入Toldt,s融合筋膜間隙,再就是在回結腸血管上方術者向胰頭方向游離解剖時的“爬坡”過程是其技術難點,稍有不慎很容易進入十二指腸后方[10]。尾側入路可以更好地進入間隙,但對于回盲部腫瘤來說也容易違反腫瘤根治的“No Touch”原則,且需要面臨的技術難點也是在十二指腸降段右側以及水平部的下方分別解剖游離時“爬坡”的操作過程。
本團隊回顧右半結腸切除術中以胰頭和十二指腸為導向的思路,受腹腔鏡下胰十二指腸切除術過程中切開屈氏韌帶解剖胰頭和十二指腸的啟發,嘗試行腹腔鏡下右半結腸切除術時從切開屈氏韌帶作為開拓右半結腸各間隙的入路,其優點是能輕松進入十二指腸以及胰頭前方疏松間隙,直接游離出導向標志胰頭以及十二指腸并分別向下以及向上拓展,且在游離十二指腸降段以及水平段時變既往傳統方式的“爬坡”操作為“下坡”操作,能快速游離出整個升結腸后間隙,結合腹腔鏡視野下“挖地洞、打隧道,拆房頂”等[11-12]手術技巧進行血管脈絡化操作以及淋巴結清掃。該入路術式優先切開屈氏韌帶游離并進入腹膜后胰頭前間隙,游離過程中部分即已顯露右結腸動脈、靜脈、胃結腸干和腸系膜上靜脈的走行,因此即使遇到血管大出血也可以迅速、容易地處理這種情況。手術團隊完成本例患者手術,自屈氏韌帶入路切開開始至整個右半結腸間隙解剖完成包括淋巴結清掃耗時僅約55 min,而整個手術時間約90 min(包括術中電勾損傷1處十二指腸漿膜層行腹腔鏡下縫合的時間),術中出血量約為 20 mL,該入路具有操作過程簡單,解剖精準,導向清晰等優點,但其缺點是胰頭前間隙血管豐富,操作不慎時可能容易導致血管出血。此入路路徑優先進行便于初次實踐者掌握,但仍需要具有豐富的腹腔鏡下右半結腸切除術手術經驗者實施,且對助手的配合要求相對較高。筆者手術團隊首次嘗試該入路且僅行1例操作,具有一定的局限性,短期手術效果良好,但遠期腫瘤安全性有待進一步的考證,實踐經驗尚需進一步總結,以便更好的推廣該入路術式,相應還可以在該術式基礎上進行其他多方位的實驗研究。腹腔鏡下右半結腸切除術應該是以聯合入路為基礎的操作過程,我們嘗試了經屈氏韌帶路徑優先的入路方式進行,希望為臨床工作者提供一個可行的思路。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:江海濤教授以及劉曉東教授提供寫作思路,邢智遠博士執筆成稿,另外致謝青島大學附屬醫院感染科張鳳娟教授文筆潤色。
倫理聲明:本研究通過了青島大學附屬醫院醫學倫理委員會審批(批文編號: QYFYWZLL28740)。