1 病例資料
患者,男,19歲,因“反復發熱19 d并發現腹部包塊18 d”就診于四川大學華西醫院(簡稱“我院”)。本次就診前19 d時患者無明顯誘因發熱并伴上腹部隱痛,無惡心、嘔吐及腹脹,立即就診于當地醫院并考慮為“肝膿腫、腹腔巨大包塊”。為進一步確診來我院就診,在我院第1次檢查全腹部增強CT(圖1a)示:中上腹腸系膜區見不規則低密度腫塊,其內可見條狀等密度影,邊界清晰,較大層面約18.6 cm×7.2 cm大小,增強后可見其內條狀輕度強化,腸系膜血管包繞其內呈扇形分布,鄰近腸管受壓移位,鄰近腸壁未見增厚,近端腸管未見梗阻征象,考慮為“間葉源性腫瘤,脈管瘤?黏液樣脂肪肉瘤?”;肝右后葉下段見一約5.7 cm×4.1 cm大小的團塊狀低密度影,考慮“肝膿腫?”。后患者自行于另一醫院行彩超引導下肝膿腫穿刺引流,引流液培養示大腸埃希菌并給予抗感染、補液、糾正電解質等對癥治療后患者發熱等癥狀緩解;此次治療后第7 天行超聲引導下經皮腹腔包塊穿刺活檢術,術后腫瘤出血致患者腹脹腹痛加重,伴有惡心嘔吐,嘔吐物為胃內容物,量少,予以禁食、營養支持、抗感染等對癥支持治療后癥狀未見明顯緩解;穿刺活檢術后第8天時轉入我院肝移植中心。查體:貧血貌,消瘦,腹部膨隆,腹軟,中腹部輕度壓痛,無反跳痛,無肌緊張,中腹部可觸及一巨大包塊,呈橢圓形,表面光滑,質地較硬,邊界清楚,活動度差。血紅蛋白74 g/L,白細胞計數7.98×109/L,中性粒細胞百分率86.0%,血小板計數 343×109/L,總膽紅素52.6 μmol/L,直接膽紅素15.0 μmol/L,白蛋白35.3 g/L,尿肌酐68.00 μmol/L,估算腎小球濾過率 131.61 mL/(min·1.73 m2),降鈣素原0.26 μg/L,C-反應蛋白246 mg/L,其余血培養、血兒茶酚胺、空腹血糖、腫瘤標志物均正常。入院后在我院復查全腹部三維血管增強CT(圖1b、1c)示:中上腹腸系膜區見不規則低密度腫塊,其內可見多發稍高密度影并見液液平面,較大層面約22.8 cm×11.4 cm大小,增強后可見其內條狀輕度強化,腸系膜血管包繞其內呈扇形分布,鄰近腸管受壓移位,鄰近腸壁未見增厚,近端腸管未見梗阻征象,考慮為“間葉源性腫瘤合并出血?脈管瘤?腹腔積液、積血”。肝右后葉下段見片狀低密度影,約3.0 cm×2.0 cm大小,邊緣模糊,增強后可見不均勻強化,肝膿腫可能,其內見經皮置管影。此次入我院后繼續給予抗感染、營養支持、糾正電解質、保持引流等對癥支持治療,治療后4 d時患者感染控制可,無膿液引出,并拔出肝膿腫穿刺引流管。經多學科協作團隊討論后,于對癥支持治療后第12天時在全身麻醉下行“腹膜后巨大腫瘤切除+小腸部分切除吻合+胃造瘺+空腸造瘺術”。術中發現:腸系膜根部一約20 cm×12 cm×10 cm大小多囊樣腫物,腫物與周圍組織無明確界限,腫物包繞腸系膜上動靜脈根部、空腸動脈第一支、結腸中動脈起始部、左結腸動脈、十二直腸升部、十二指腸空腸曲及近端空腸約15 cm處腸管受累,無法分離(圖1d)。為了降低腫瘤復發幾率,從組織疏松處多方位易分理處分離;無法分離的部分巨大囊性瘤體,先吸出囊內液體,瘤體縮小后再分離;腫瘤累及的重要血管,先分離一側后再推向對側,打開血管鞘后將之分離;腫瘤囊壁與小腸粘連緊密而無法分離,術中為求完整切除,行聯合部分小腸切除術;臺下剖視標本:腸系膜根部多囊樣腫物,部分囊內可見積血,余囊液呈清亮黃色。術后病理檢查結果示:傾向脈管源性腫瘤伴廣泛繼發改變(圖1e)。免疫組織化學染色示:CD31(+),CD34(+,圖1f),S100(脂肪+),CDK4(–),D2-40(部分+),CD68PG-M1(組織細胞+),HMB-45(–),MART-1(–)。熒光原位雜交未檢出MDM2基因擴增,支持脈管源性腫瘤,形態學可見淋巴管瘤和血管瘤成分,以淋巴管瘤成分為主,伴廣泛繼發改變級泡沫細胞反應。術后給予補液、止痛、抗感染、營養支持等對癥支持治療。患者癥狀好轉,術后恢復良好,術后第10天出院。
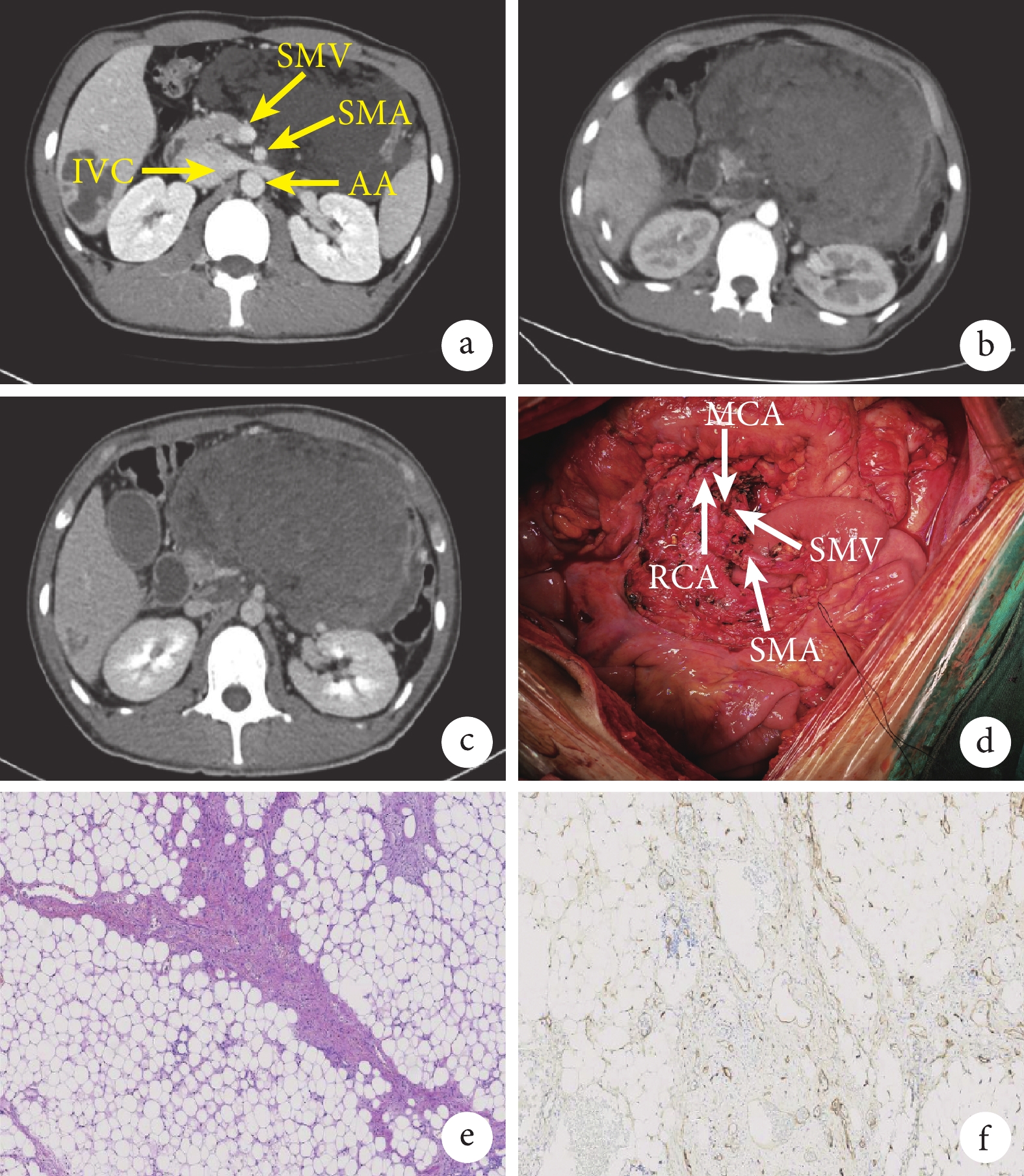 圖1
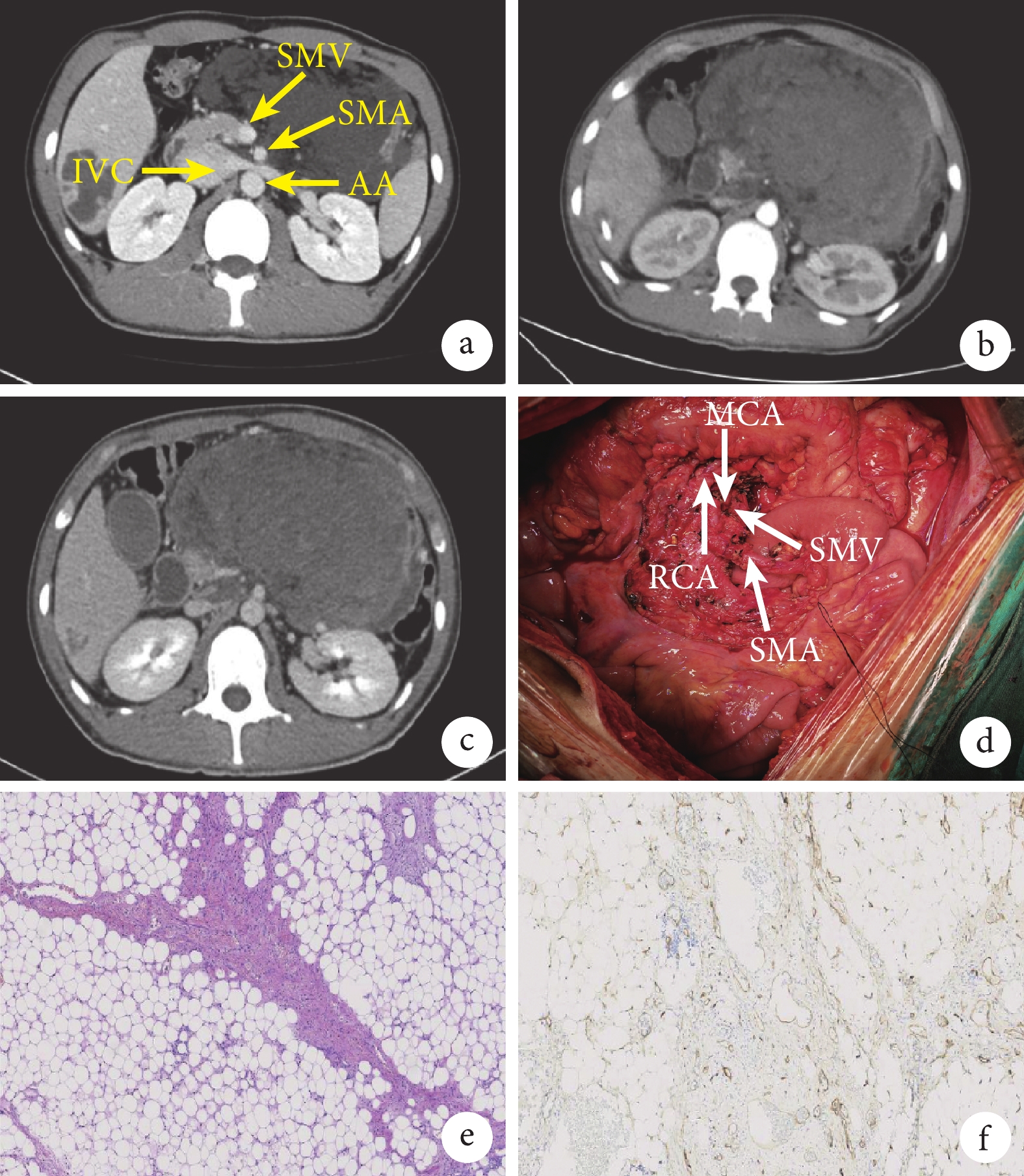
示術前CT檢查結果及術中圖像和術后病例標本和組織病學結果
圖1
示術前CT檢查結果及術中圖像和術后病例標本和組織病學結果
a:第1次于我院就診時CT檢查結果;b、c:第2次于我院住院后CT檢查結果;d:術中圖像;e:術后組織病理學結果(蘇木精-伊紅染色 ×400);f:CD34陽性染色(免疫組織化學染色 ×400)。SMA:腸系膜上動脈;SMV:腸系膜上靜脈;RCA:右結腸動脈;MCA:中結腸動脈;AA:腹主動脈;IVC:下腔靜脈
2 討論
腹膜后淋巴管瘤(簡稱“該病”)是罕見的良性疾病,約占所有淋巴管瘤的1%[1-2],伴肝膿腫者更少見。我院收治1例合并肝膿腫的原發性腹膜后巨大淋巴管瘤。目前認為該病是由于先天性淋巴管瘤發育畸形或因外傷、炎癥、寄生蟲等后天性因素引起淋巴液排出障礙而造成淋巴液潴留導致淋巴管擴張、增生而形成[2-3]。該病侵襲性生長,可侵犯或壓迫周圍組織[4-5]。然而由于該病腹膜后間隙組織疏松而使其伸展空間大,使得其早期癥狀不明顯,待腫瘤壓迫鄰近神經、血管及臟器時才出現癥狀[6-7]。該病術前CT影像學特征為:腫瘤形態呈單房或多房型不規則分葉狀,囊性時其CT值隨囊內容物性質不同而異,若為漿液樣液體時其CT值與水相同,若囊性且合并出血、感染時密度偏高[8]。本例患者經多學科協作討論后手術治療,術中無法分離的巨大囊性瘤體采取先吸出囊內液體,待瘤體縮小后再分離,注意避免內容物流入腹腔;腫瘤累及重要血管,保留腸系膜上動靜脈、結腸動脈、空腸動脈為術中難點,為了完整切除腫瘤的同時力求保留結腸,采取先分離一側后再推向對側,打開血管鞘將之分離;因腫瘤囊壁與小腸粘連緊密而無法分離行部分小腸聯合切除;隨訪至術后21個月時未見復發。該患者術前腹部CTA提示是腹膜后腫瘤伴肝膿腫,腫瘤起源于腸系膜根部,容易壓迫十二指腸及腸系膜靜脈;患者術前膽紅素較高,結合患者出現的癥狀(惡心、嘔吐),肝膿腫的形成考慮為膽管逆行感染或血行感染引起可能。臨床上腹膜后腫瘤引起肝膿腫案例極少。總之,合并肝膿腫的腹膜后巨大淋巴管瘤臨床上極為罕見,術前診斷困難,病情復雜,手術難度極大,建議多學科協作討論以制定最佳的治療方案,讓患者獲益。
重要聲明
利益沖突聲明:本文全體作者聲明無相互競爭的利益。
作者貢獻聲明:伊力亞爾·艾爾肯、楊儉及楊家印共同完成了文獻檢索和匯總;伊力亞爾·艾爾肯完成了文稿的撰寫;楊儉和楊家印完成了文稿的審閱。
倫理聲明:本研究通過了四川大學華西醫院醫學倫理審查委員會審批。
1 病例資料
患者,男,19歲,因“反復發熱19 d并發現腹部包塊18 d”就診于四川大學華西醫院(簡稱“我院”)。本次就診前19 d時患者無明顯誘因發熱并伴上腹部隱痛,無惡心、嘔吐及腹脹,立即就診于當地醫院并考慮為“肝膿腫、腹腔巨大包塊”。為進一步確診來我院就診,在我院第1次檢查全腹部增強CT(圖1a)示:中上腹腸系膜區見不規則低密度腫塊,其內可見條狀等密度影,邊界清晰,較大層面約18.6 cm×7.2 cm大小,增強后可見其內條狀輕度強化,腸系膜血管包繞其內呈扇形分布,鄰近腸管受壓移位,鄰近腸壁未見增厚,近端腸管未見梗阻征象,考慮為“間葉源性腫瘤,脈管瘤?黏液樣脂肪肉瘤?”;肝右后葉下段見一約5.7 cm×4.1 cm大小的團塊狀低密度影,考慮“肝膿腫?”。后患者自行于另一醫院行彩超引導下肝膿腫穿刺引流,引流液培養示大腸埃希菌并給予抗感染、補液、糾正電解質等對癥治療后患者發熱等癥狀緩解;此次治療后第7 天行超聲引導下經皮腹腔包塊穿刺活檢術,術后腫瘤出血致患者腹脹腹痛加重,伴有惡心嘔吐,嘔吐物為胃內容物,量少,予以禁食、營養支持、抗感染等對癥支持治療后癥狀未見明顯緩解;穿刺活檢術后第8天時轉入我院肝移植中心。查體:貧血貌,消瘦,腹部膨隆,腹軟,中腹部輕度壓痛,無反跳痛,無肌緊張,中腹部可觸及一巨大包塊,呈橢圓形,表面光滑,質地較硬,邊界清楚,活動度差。血紅蛋白74 g/L,白細胞計數7.98×109/L,中性粒細胞百分率86.0%,血小板計數 343×109/L,總膽紅素52.6 μmol/L,直接膽紅素15.0 μmol/L,白蛋白35.3 g/L,尿肌酐68.00 μmol/L,估算腎小球濾過率 131.61 mL/(min·1.73 m2),降鈣素原0.26 μg/L,C-反應蛋白246 mg/L,其余血培養、血兒茶酚胺、空腹血糖、腫瘤標志物均正常。入院后在我院復查全腹部三維血管增強CT(圖1b、1c)示:中上腹腸系膜區見不規則低密度腫塊,其內可見多發稍高密度影并見液液平面,較大層面約22.8 cm×11.4 cm大小,增強后可見其內條狀輕度強化,腸系膜血管包繞其內呈扇形分布,鄰近腸管受壓移位,鄰近腸壁未見增厚,近端腸管未見梗阻征象,考慮為“間葉源性腫瘤合并出血?脈管瘤?腹腔積液、積血”。肝右后葉下段見片狀低密度影,約3.0 cm×2.0 cm大小,邊緣模糊,增強后可見不均勻強化,肝膿腫可能,其內見經皮置管影。此次入我院后繼續給予抗感染、營養支持、糾正電解質、保持引流等對癥支持治療,治療后4 d時患者感染控制可,無膿液引出,并拔出肝膿腫穿刺引流管。經多學科協作團隊討論后,于對癥支持治療后第12天時在全身麻醉下行“腹膜后巨大腫瘤切除+小腸部分切除吻合+胃造瘺+空腸造瘺術”。術中發現:腸系膜根部一約20 cm×12 cm×10 cm大小多囊樣腫物,腫物與周圍組織無明確界限,腫物包繞腸系膜上動靜脈根部、空腸動脈第一支、結腸中動脈起始部、左結腸動脈、十二直腸升部、十二指腸空腸曲及近端空腸約15 cm處腸管受累,無法分離(圖1d)。為了降低腫瘤復發幾率,從組織疏松處多方位易分理處分離;無法分離的部分巨大囊性瘤體,先吸出囊內液體,瘤體縮小后再分離;腫瘤累及的重要血管,先分離一側后再推向對側,打開血管鞘后將之分離;腫瘤囊壁與小腸粘連緊密而無法分離,術中為求完整切除,行聯合部分小腸切除術;臺下剖視標本:腸系膜根部多囊樣腫物,部分囊內可見積血,余囊液呈清亮黃色。術后病理檢查結果示:傾向脈管源性腫瘤伴廣泛繼發改變(圖1e)。免疫組織化學染色示:CD31(+),CD34(+,圖1f),S100(脂肪+),CDK4(–),D2-40(部分+),CD68PG-M1(組織細胞+),HMB-45(–),MART-1(–)。熒光原位雜交未檢出MDM2基因擴增,支持脈管源性腫瘤,形態學可見淋巴管瘤和血管瘤成分,以淋巴管瘤成分為主,伴廣泛繼發改變級泡沫細胞反應。術后給予補液、止痛、抗感染、營養支持等對癥支持治療。患者癥狀好轉,術后恢復良好,術后第10天出院。
 圖1
示術前CT檢查結果及術中圖像和術后病例標本和組織病學結果
圖1
示術前CT檢查結果及術中圖像和術后病例標本和組織病學結果
a:第1次于我院就診時CT檢查結果;b、c:第2次于我院住院后CT檢查結果;d:術中圖像;e:術后組織病理學結果(蘇木精-伊紅染色 ×400);f:CD34陽性染色(免疫組織化學染色 ×400)。SMA:腸系膜上動脈;SMV:腸系膜上靜脈;RCA:右結腸動脈;MCA:中結腸動脈;AA:腹主動脈;IVC:下腔靜脈
2 討論
腹膜后淋巴管瘤(簡稱“該病”)是罕見的良性疾病,約占所有淋巴管瘤的1%[1-2],伴肝膿腫者更少見。我院收治1例合并肝膿腫的原發性腹膜后巨大淋巴管瘤。目前認為該病是由于先天性淋巴管瘤發育畸形或因外傷、炎癥、寄生蟲等后天性因素引起淋巴液排出障礙而造成淋巴液潴留導致淋巴管擴張、增生而形成[2-3]。該病侵襲性生長,可侵犯或壓迫周圍組織[4-5]。然而由于該病腹膜后間隙組織疏松而使其伸展空間大,使得其早期癥狀不明顯,待腫瘤壓迫鄰近神經、血管及臟器時才出現癥狀[6-7]。該病術前CT影像學特征為:腫瘤形態呈單房或多房型不規則分葉狀,囊性時其CT值隨囊內容物性質不同而異,若為漿液樣液體時其CT值與水相同,若囊性且合并出血、感染時密度偏高[8]。本例患者經多學科協作討論后手術治療,術中無法分離的巨大囊性瘤體采取先吸出囊內液體,待瘤體縮小后再分離,注意避免內容物流入腹腔;腫瘤累及重要血管,保留腸系膜上動靜脈、結腸動脈、空腸動脈為術中難點,為了完整切除腫瘤的同時力求保留結腸,采取先分離一側后再推向對側,打開血管鞘將之分離;因腫瘤囊壁與小腸粘連緊密而無法分離行部分小腸聯合切除;隨訪至術后21個月時未見復發。該患者術前腹部CTA提示是腹膜后腫瘤伴肝膿腫,腫瘤起源于腸系膜根部,容易壓迫十二指腸及腸系膜靜脈;患者術前膽紅素較高,結合患者出現的癥狀(惡心、嘔吐),肝膿腫的形成考慮為膽管逆行感染或血行感染引起可能。臨床上腹膜后腫瘤引起肝膿腫案例極少。總之,合并肝膿腫的腹膜后巨大淋巴管瘤臨床上極為罕見,術前診斷困難,病情復雜,手術難度極大,建議多學科協作討論以制定最佳的治療方案,讓患者獲益。
重要聲明
利益沖突聲明:本文全體作者聲明無相互競爭的利益。
作者貢獻聲明:伊力亞爾·艾爾肯、楊儉及楊家印共同完成了文獻檢索和匯總;伊力亞爾·艾爾肯完成了文稿的撰寫;楊儉和楊家印完成了文稿的審閱。
倫理聲明:本研究通過了四川大學華西醫院醫學倫理審查委員會審批。