引用本文: 龔文輝, 韋小勇, 高曉天, 許金國, 翁光東, 張成鑫. “一站式”經心尖經導管主動脈瓣置換術聯合二尖瓣緣對緣修復術治療多瓣膜病變的早期療效分析. 中國胸心血管外科臨床雜志, 2024, 31(10): 1467-1474. doi: 10.7507/1007-4848.202312083 復制
版權信息: ?四川大學華西醫院華西期刊社《中國胸心血管外科臨床雜志》版權所有,未經授權不得轉載、改編
多瓣膜心臟病(multivalvular heart disease,MHD)是指兩個或以上瓣膜合并狹窄或反流[1]。在老年心臟瓣膜病患者中,MHD尤為常見,如主動脈瓣狹窄合并二尖瓣反流或主動脈瓣關閉不全合并二尖瓣反流等。危重多瓣膜病變極大地增加了外科瓣膜置換或修復手術的風險[2]。因此,許多需要手術干預的多瓣膜病變患者常因手術風險過高而未能接受外科手術治療。
近年來,心臟瓣膜介入技術快速發展,因其創傷小、恢復快等優勢,成為治療外科手術禁忌或高危患者的合理選擇。經導管主動脈瓣置換術(transcatheter aortic valve replacement,TAVR)已成為治療高危主動脈瓣病變的一種理想方法,特別是對于不能耐受體外循環下常規開胸手術的高危患者,TAVR提供了一種新的治療選擇[3]。而經導管二尖瓣緣對緣修復術(transcatheter mitral valve edge-to-edge repair,TEER)也為外科高危的重度二尖瓣反流患者提供了一種有效的治療方法[4]。近期復旦大學中山醫院報道了“一站式”經心尖TAVR+TEER治療重度主動脈瓣關閉不全+二尖瓣反流的案例,術后30 d隨訪結局良好[5]。通過“一站式”經導管TAVR+TEER介入治療同時處理主動脈瓣及二尖瓣多瓣膜病變是一種新的嘗試,為外科高危的多瓣膜病變患者治療帶來新希望。本研究通過回顧我院心臟大血管外科近期完成的“一站式”經心尖TAVR+TEER病例,初步探討該方法在高危主動脈瓣病變合并重度二尖瓣反流的多瓣膜病變患者中的安全性和有效性。
1 資料與方法
1.1 臨床資料
回顧性分析2022年8月—2023年10月在我院心臟大血管外科完成“一站式”TAVR+TEER患者的臨床資料。納入標準:(1)年齡≥65歲;(2)紐約心臟協會(New York Heart Association,NYHA)心功能分級≥Ⅱ級;(3)根據歐洲心臟病學會和歐洲心胸外科協會指南評估需要手術干預的主動脈瓣重度病變患者;(4)原發性二尖瓣反流患者:① 中重度以上二尖瓣反流,② 有臨床癥狀或無臨床癥狀但左心室射血分數≤60%或左心室收縮末期內徑≥40 mm,③ 經心臟外科團隊充分評估外科手術風險較高或無法行外科手術;(5)繼發性二尖瓣反流患者:① 中重度及以上二尖瓣反流,② 經指南指導的規范抗心力衰竭藥物治療后仍有心力衰竭癥狀,③ 超聲心動圖評估左心室射血分數為20%~50%,左心室收縮末期內徑≤70 mm,④ 肺動脈收縮壓≤70 mm Hg(1 mm Hg=0.133 kPa)[2,4,6];(6)二尖瓣病變為A2/P2區、瓣口面積>4 cm2、夾合區瓣葉無鈣化等解剖結構適合行TEER。排除標準:(1)1個月內發生過急性心肌梗死;(2)1個月內急性期腦血管意外;(3)未經治療的嚴重冠狀動脈狹窄,需要血運重建或需要進行其他心臟手術;(4)存在抗凝禁忌;(5)患者預期壽命<1年;(6)左心室射血分數<20%;(7)合并二尖瓣狹窄;(8)有造影劑過敏反應。
1.2 患者診斷及術前準備
術前經胸超聲心動圖評估主動脈瓣、二尖瓣、三尖瓣等瓣葉功能,初步評估為癥狀性中重度主動脈瓣狹窄或主動脈瓣關閉不全、重度二尖瓣反流;通過主動脈CT及冠狀動脈CT血管造影以及3mensio軟件(3mensio Medical Imaging BV,荷蘭)進行圖像分析,規范評估主動脈根部、主動脈瓣及瓣環、冠狀動脈等解剖結構情況[7];通過經食管超聲心動圖進一步評估患者二尖瓣裝置參數,明確二尖瓣病變類型、瓣口面積、前后葉、反流程度等,進一步明確診斷。所有患者術前均經過心臟外科、超聲及麻醉等多學科團隊進行風險評估并制定“一站式”手術具體方案。
1.3 手術方法
手術均在雜交手術室進行。術前使用經食管超聲心動圖再次評估主動脈瓣和二尖瓣病變的相關數據。經左側股動靜脈穿刺置入6F/5F 鞘管,分別放置主動脈造影豬尾導管、起搏導線,并測試起搏導線功能是否正常。透視下行心尖定位后,確定最佳左外側切口位置,手術切口長約4~6 cm。十字切開心包并懸吊于切口,以充分暴露心尖位置,使用3-0 Prolene線帶毛氈片于心尖部縫合雙重六邊形的荷包,在距左前降支外側1~2 cm處選擇荷包縫合位置。全身肝素化(1 mg/kg,活化凝血時間>220 s),主動脈根部造影,在荷包內穿刺置入16~20F血管鞘,后置入150 cm超滑泥鰍導絲,導絲通過主動脈瓣和導管配合過弓到達降主動脈,交換260 cm支撐加硬導絲。對于主動脈瓣狹窄或鈣化患者可行球囊預擴張(球囊至目標位置后,180次/min快速起搏,擴張球囊,回抽后停起搏),退出球囊和鞘管。置入J-Valve瓣膜(蘇州杰成醫療科技有限公司)輸送裝置跨過主動脈瓣瓣口,升主動脈造影定位并進行角度調整,確認定位件置于竇底,調整支架瓣膜位置至主動脈瓣環內,定位后釋放J-valve人工瓣膜。對主動脈瓣狹窄或鈣化患者,可行球囊后擴張。術中釋放后即刻經食管超聲心動圖和造影評估,確認瓣膜定位良好,無瓣周漏,退出導絲及輸送裝置,主動脈瓣置換結束;見圖1。
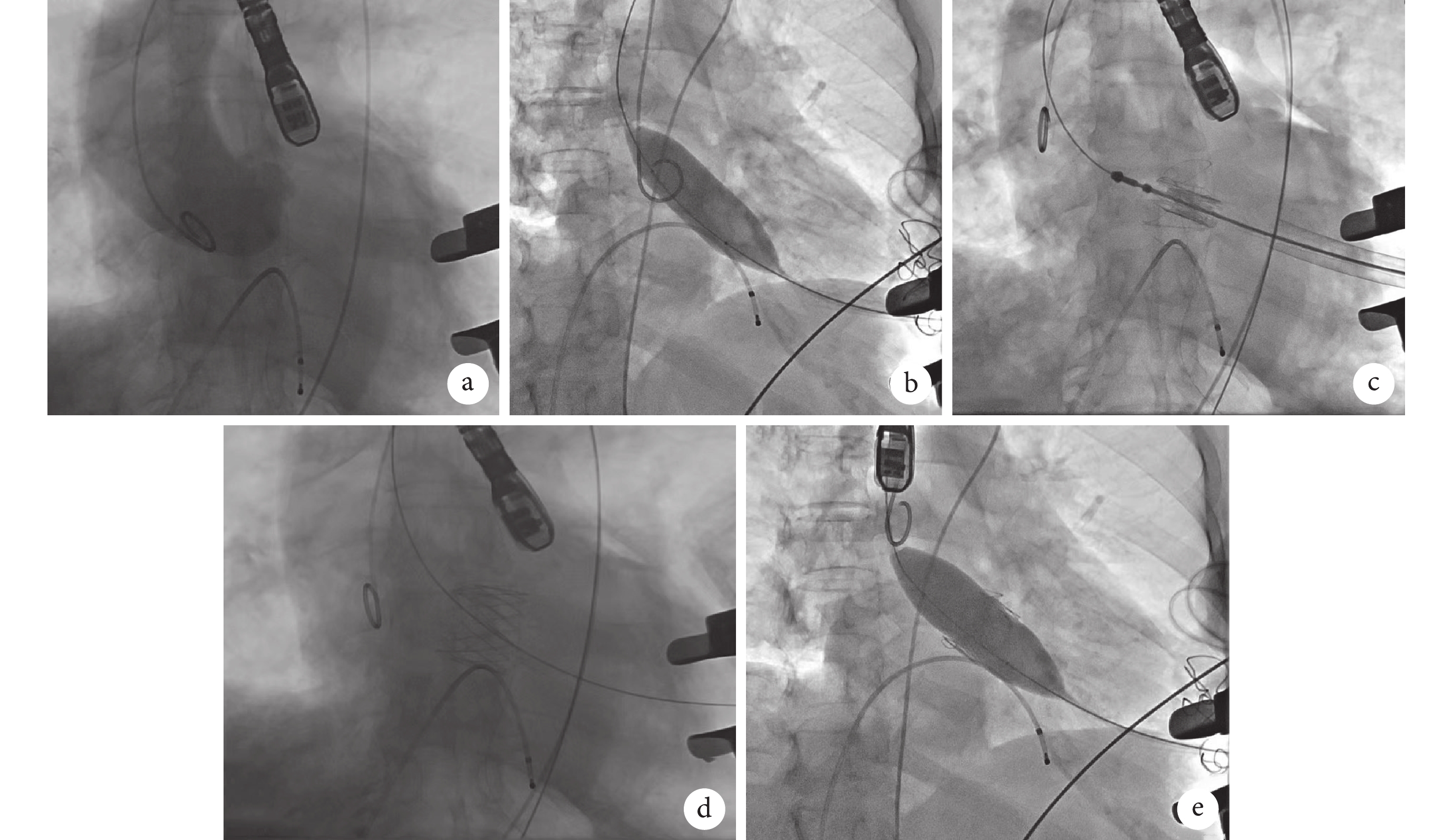 圖1
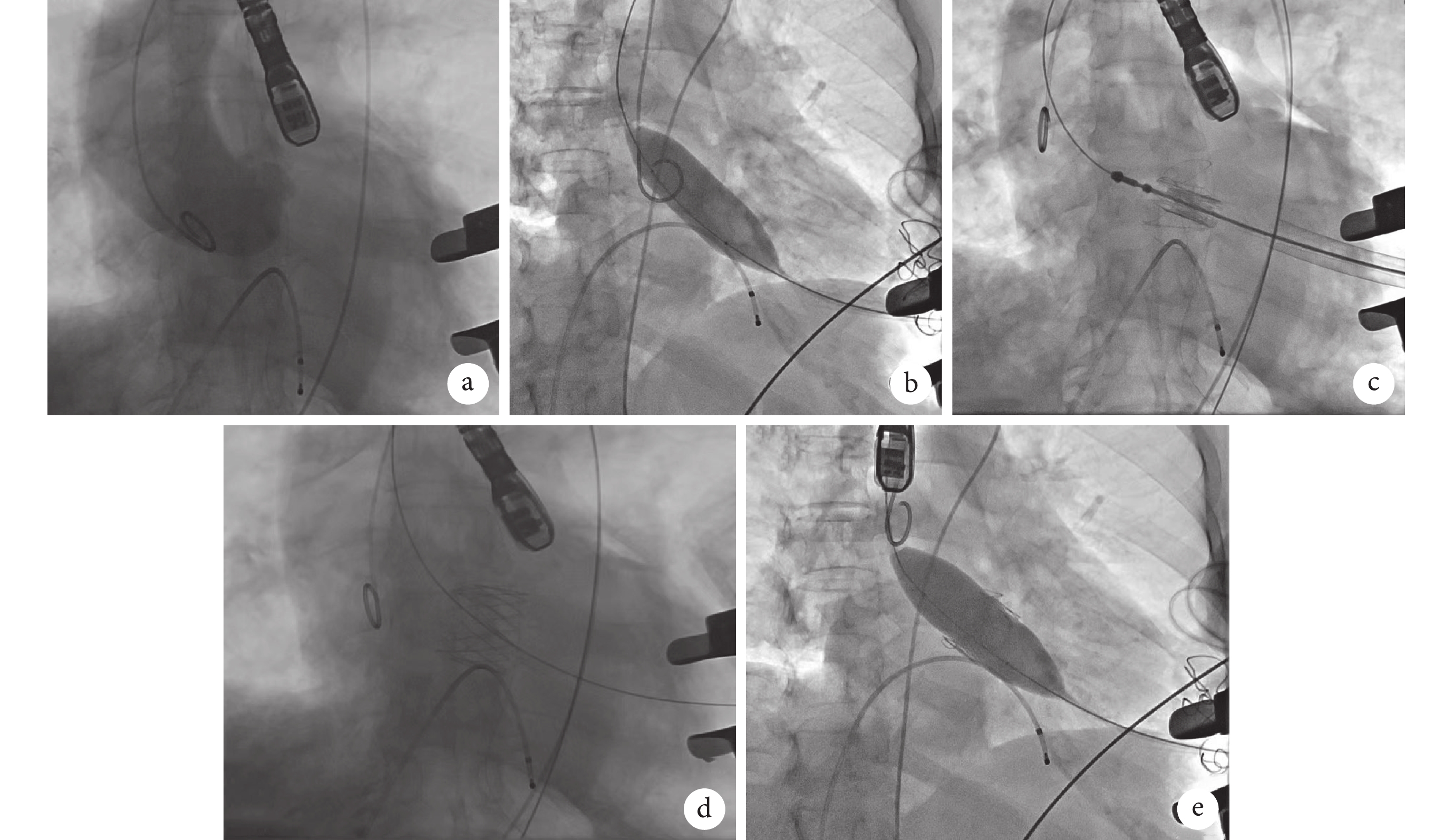
經心尖經導管主動脈瓣置換術(TAVR)手術流程
圖1
經心尖經導管主動脈瓣置換術(TAVR)手術流程
a:術前主動脈根部造影示主動脈瓣反流;b:主動脈瓣嚴重狹窄或鈣化可行球囊預擴張;c:支架瓣膜定位件進入主動脈竇內,瓣膜下降至主動脈瓣環平面;d:瓣膜釋放完畢,主動脈根部造影示支架瓣膜位置及功能完好,撤出輸送裝置;e:主動脈瓣嚴重狹窄或鈣化可行球囊后擴張
經穿刺點置入短導絲,經導絲置入鞘管,置入跨瓣器,超聲引導下過二尖瓣瓣環至左心房,進鞘管至左心房,輕輕擺動跨瓣器,確認其未纏繞二尖瓣腱索后沿引導鞘管退出跨瓣器。裝載MCV-Ⅲ型二尖瓣夾合器(ValveClamp,上海捍宇醫療科技股份有限公司),將夾合器沿引導鞘管送至左心房,反復經胸超聲心動圖定位,使夾子與瓣葉平面垂直并位于A2/P2區,使前后葉均落在二尖瓣夾上,確保夾住瓣緣后收縮夾子,超聲評估見反流明顯減少,瓣口呈現兩瓣口,無明顯狹窄,釋放二尖瓣夾合器,再次超聲評估,若存在中度以上二尖瓣反流,可重復上述步驟,再次置入二尖瓣夾合器。超聲評估效果滿意,退出輸送裝置。心尖荷包打結,止血置引流管,逐層關胸;見圖2。
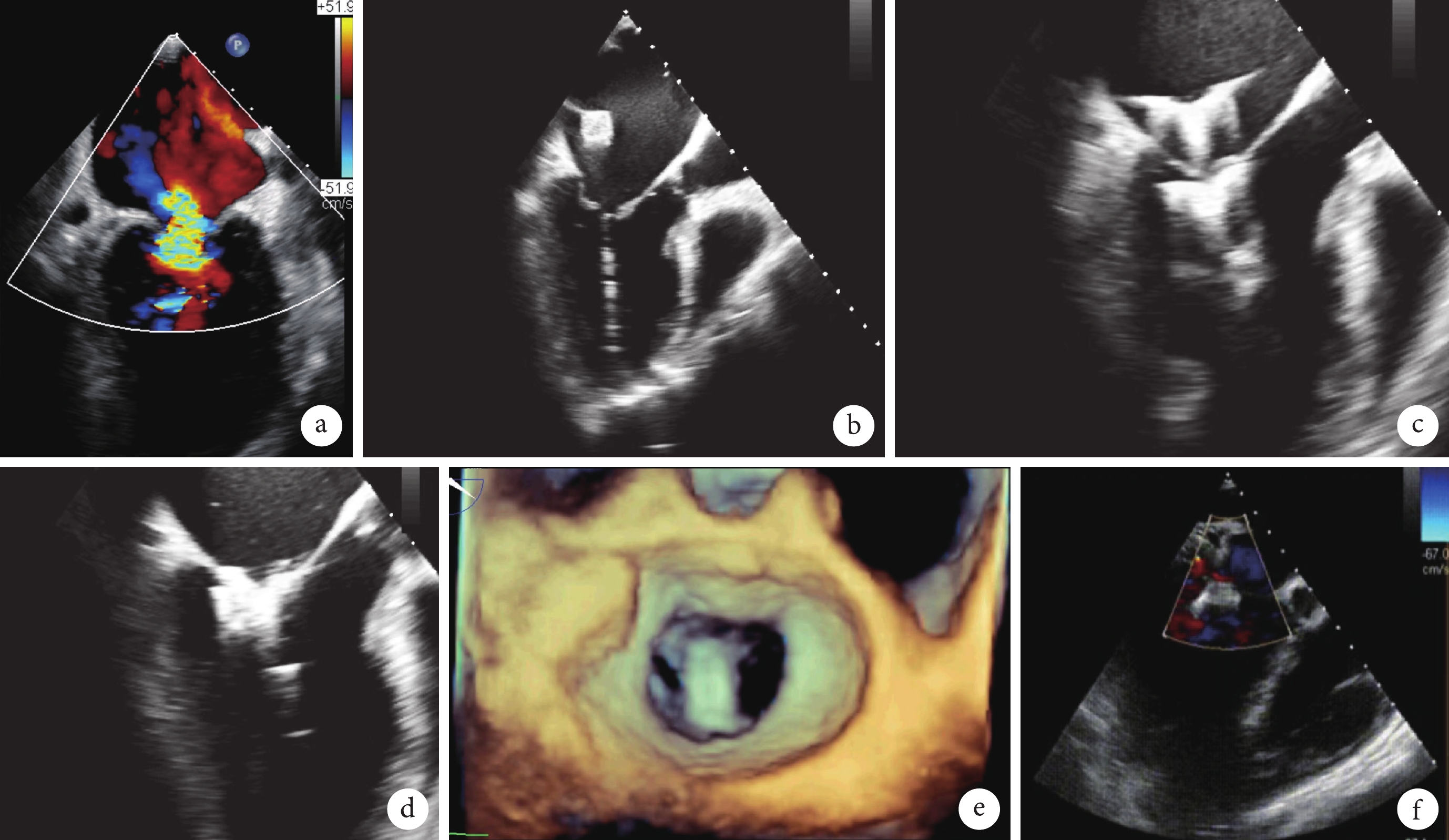 圖2
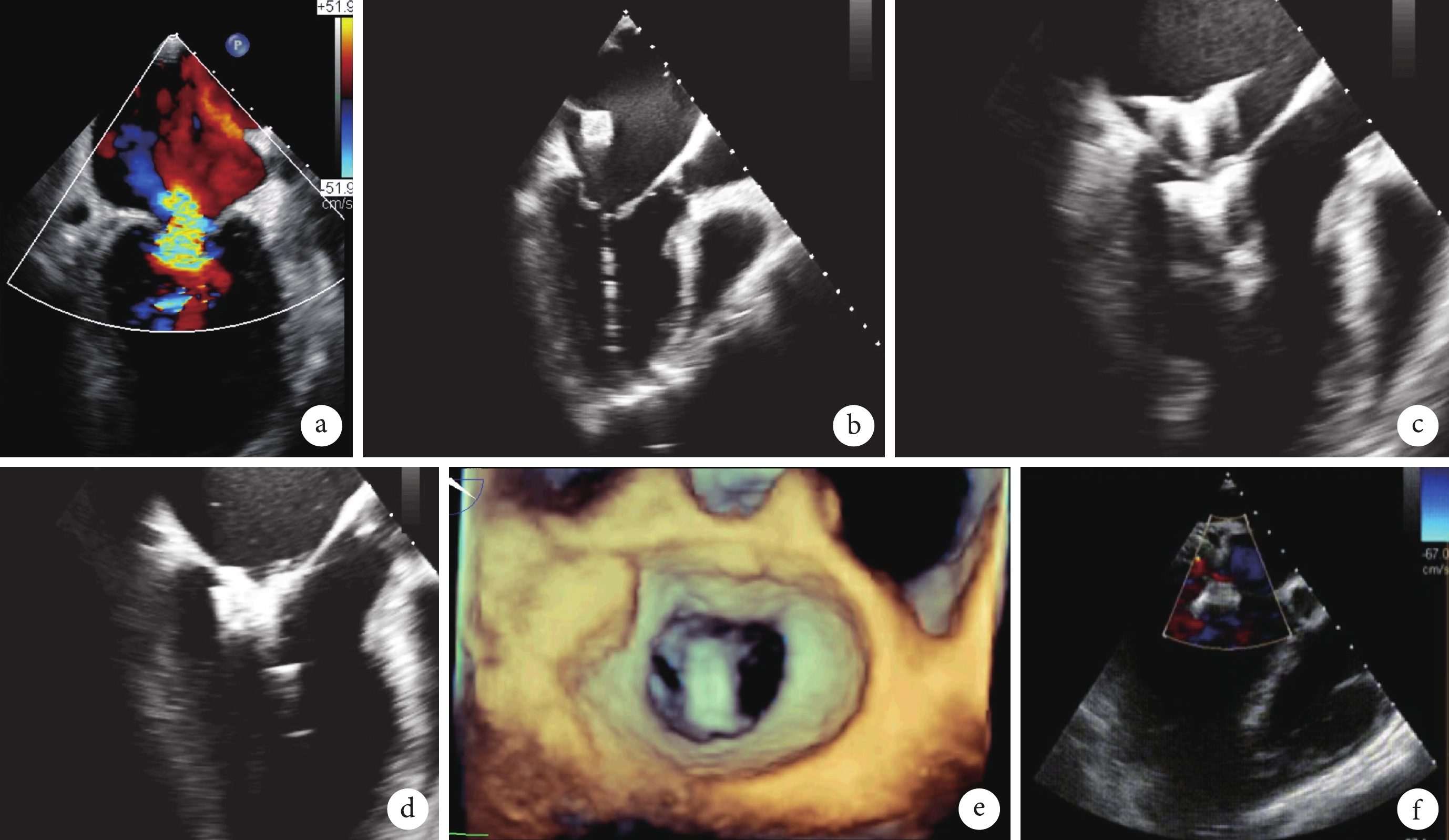
病例3 經心尖經導管二尖瓣緣對緣修復術(TEER)手術流程
圖2
病例3 經心尖經導管二尖瓣緣對緣修復術(TEER)手術流程
a:術前超聲心動圖提示二尖瓣重度反流;b:置入跨瓣器;c:前后夾與二尖瓣開放線垂直,并位于 A2/P2 區;d:收緊夾合器;e:釋放夾合器;f:術后復查超聲心動圖提示二尖瓣反流降為輕度
1.4 資料收集
收集并記錄患者的基線資料:年齡、性別、相關病史、NYHA心功能分級、術前影像學評估結果等。手術資料:瓣膜型號、手術時間、呼吸機輔助時間、ICU住院時間、術后住院時間等。收集術后1個月、3個月內的隨訪結果。
1.5 隨訪及研究終點
所有患者出院后定期通過心臟大血管外科門診或電話隨訪,記錄患者術后臨床癥狀、超聲心動圖結果和不良終點事件發生時間和情況。本研究的主要終點為隨訪期(術后1個月和3個月)內結果,包括心功能分級、主動脈瓣瓣周漏、二尖瓣反流嚴重程度、左心室大小改變和左心室射血分數改變等。次要終點為手術相關并發癥,包括瓣膜移位、夾合器脫落、新發心房顫動或房室傳導阻滯、需要腎臟替代治療的急性腎損傷、再次手術等。
1.6 統計學分析
所有數據采用SPSS 23.0軟件進行分析。服從正態分布的計量資料以均數±標準差( ±s)描述,不服從正態分布的計量資料以中位數(上下四分位數)[M(P25,P75)]描述。計數資料采用例數描述。
±s)描述,不服從正態分布的計量資料以中位數(上下四分位數)[M(P25,P75)]描述。計數資料采用例數描述。
1.7 倫理審查
本研究經安徽醫科大學第一附屬醫院倫理委員會審批通過,倫理審批號:PJ2024-02-42。所有研究對象均簽署知情同意書。
2 結果
2.1 患者基線資料
共納入5例患者,其中男3例、女2例,平均年齡(66.6±1.8)歲。 主動脈瓣關閉不全合并二尖瓣反流4例、主動脈瓣狹窄伴關閉不全合并二尖瓣反流1例。重度原發性二尖瓣反流2例,重度繼發性二尖瓣反流3例。患者年齡、高血壓、糖尿病、心房顫動、腦血管病變、術前心功能分級等資料見表1。
2.2 圍術期結果
5例患者均順利完成“一站式”經心尖TAVR+TEER,所有患者圍術期內未出現死亡、出血、再次手術等不良事件,其中3例患者因術前合并慢性腎功能不全在術后需要接受連續性腎臟替代治療,2例患者因術后呼吸困難再次接受呼吸機輔助治療,1例患者新發房室傳導阻滯。手術時間(179.00±50.67)min,術后呼吸機輔助時間(16.70±3.79)h,術后中位ICU住院時間3.0(2.0,15.0)d,術后中位住院時間7.0(5.5,29.0)d,中位總住院時間24.0(17.0,42.5)d;見表2。
2.3 隨訪結果
術后即刻超聲結果顯示人工主動脈瓣膜植入效果良好,輕度瓣周漏1例。5例患者二尖瓣反流程度由術前的重度降為輕度。術后7 d,5例患者復查超聲心動圖提示人工瓣膜無移位,二尖瓣夾無脫落,瓣葉無損傷。術后1個月隨訪結果顯示4例患者心功能得到不同程度改善,1例患者因多器官功能衰竭死亡。1例患者出院后2個月余突發腦血管意外死亡,其余3例術后3個月超聲心動圖結果顯示左心房內徑、左心室內徑、左心室射血分數以及肺動脈壓均有不同程度改善,未出現輕度以上瓣周漏、主動脈瓣和二尖瓣反流,患者心功能和日常生活能力明顯改善;見表3。
3 討論
隨著人口老齡化的加劇,MHD的發病率持續上升。根據歐洲心臟病學會調查的結果顯示,瓣膜性心臟病患者中≥20%的患者存在MHD,在美國胸外科醫師協會(Society of Thoracic Surgeons,STS)數據庫中納入的60多萬例瓣膜手術患者中,接受多瓣膜手術治療患者占瓣膜手術患者的11%,其中最常見的是主動脈瓣聯合二尖瓣手術[8-9]。一項中國瓣膜性心臟病(China-VHD)注冊登記研究[10]顯示,在納入的13 917例瓣膜性心臟病患者中,MHD患者約為29.0%。雖然MHD在心臟瓣膜病患者中很常見,但其治療和干預一直是一大難題[2]。
外科雙瓣膜手術是治療多瓣膜病變的主要手段,但在高危的老年患者中,同時行雙瓣膜手術會顯著增加并發癥發生率和死亡率[11]。經導管介入瓣膜手術的出現為MHD患者提供了新的治療選擇,TAVR已成為老年或高危主動脈瓣狹窄患者的首選治療方法,并且隨著手術技術的發展和適應證的擴大,TAVR在主動脈瓣關閉不全的治療中同樣發揮著越來越重要的作用[3,12]。TEER被批準用于高危重度原發性二尖瓣反流患者以及經過優化抗心力衰竭治療后仍有癥狀的繼發性二尖瓣反流患者[4]。研究[13]表明,在接受TAVR治療的患者中,約25%的患者合并中度以上二尖瓣反流,合并中重度二尖瓣反流明顯增加了TAVR患者的早期和遠期死亡率。盡管約50%的患者在TAVR后二尖瓣反流分級可以得到改善,特別是合并繼發性或功能性二尖瓣反流的患者,但術后殘留持續性中重度二尖瓣反流的患者預后較差[13-14]。因此對于重度主動脈瓣狹窄和繼發性二尖瓣反流患者,若術后伴有明顯癥狀的持續性二尖瓣反流,如果解剖結構合適,可以考慮分期行TEER。對于重度主動脈瓣狹窄合并重度原發性二尖瓣反流患者,二尖瓣反流分級在TAVR術后改善不明顯,對于此類患者,如果解剖結構合適且TAVR術后二尖瓣反流持續存在,則可以考慮進行分期TEER[15-17]。但迄今為止,經導管多瓣膜手術治療的臨床經驗和結果數據有限,只有少量研究[5,15-17]報道TAVR同期或分期行二尖瓣介入修復或置換的可行性。
Kische等[15]報道12例合并重度二尖瓣反流的患者因心力衰竭癥狀加重,在TAVR后使用MitraClip裝置行TEER,術后患者心功能分級明顯改善,30 d內無患者死亡或重大不良事件發生。一項西班牙的研究[16]表明,5例在TAVR術后存在顯著二尖瓣反流的患者使用MitraClip裝置行TEER,術后二尖瓣反流明顯減少,患者心功能分級和臨床癥狀明顯改善。一項由23家TAVR中心組成的多中心登記研究[17]報道106例在TAVR后接受經導管二尖瓣介入治療患者(100例分期,6例同期,其中TEER 95例)的結局,結果顯示93.2%的患者在TEER術后殘留的中重度二尖瓣反流降為中度或更低(56.8% 輕度或以下,P<0.001),并在6個月和1年內保持穩定(P=0.344 和 P=0.897)。這項研究表明在TAVR后殘留持續癥狀性中重度二尖瓣反流且在解剖學上適合經導管二尖瓣介入治療的患者,接受TAVR和經導管二尖瓣介入分期治療可以顯著改善二尖瓣反流分級和NYHA心功能分級,并且是安全可行的。Zajarias等[18]回顧了STS/美國心臟病學會經導管瓣膜治療登記處257例自體瓣膜或生物瓣膜衰敗同期或分期進行TAVR和經導管二尖瓣置換治療的結果(同期135例,分期122例),結果顯示,針對選定的高危主動脈瓣和二尖瓣病變患者,經導管多瓣膜治療可同期,也可分期,同期和分期治療組30 d和1年卒中率和死亡率是可接受的。上述研究結果為經導管治療多瓣膜病變的安全性和可行性提供了一定基礎,但仍需要進一步的隨機對照研究來評估經導管介入治療在MHD中的療效和安全性。
與現有文獻中大多為主動脈瓣狹窄+二尖瓣反流患者不同,本研究主動脈瓣關閉不全+二尖瓣反流的患者比例較高(主動脈瓣狹窄伴關閉不全+二尖瓣反流 1例,主動脈瓣關閉不全+二尖瓣反流 4例)。主動脈瓣關閉不全+二尖瓣反流在MHD中常見,但指導主動脈瓣關閉不全和二尖瓣反流聯合治療的數據有限[2,8]。主動脈瓣關閉不全合并二尖瓣反流的患者通常伴隨著嚴重的左心室擴張、超容量負荷,患者對手術耐受性較差,術后左心室功能不全的發生率高,術后生存率降低[2,8,19]。因此,此類患者手術方案的選擇不僅取決于單個瓣膜的反流嚴重程度,還取決于患者的年齡、合并癥、虛弱程度以及雙瓣膜手術的風險等多種因素[2,8]。同時,還應充分考慮患者及其家屬手術治療的意愿,選擇最終的治療方案。我院心臟中心團隊經過充分評估和密切配合,使用經心尖途徑的J-Valve人工瓣膜(蘇州杰成醫療科技有限公司)和ValveClamp二尖瓣夾合器(上海捍宇醫療科技股份有限公司)對5例患者順利實施“一站式”經心尖TAVR+TEER[12,20]。術后即刻超聲心動圖結果提示主動脈瓣人工瓣膜位置和功能良好,重度二尖瓣反流即刻降為輕度,未出現二尖瓣瓣葉損傷、二尖瓣夾合器脫落等不良結果。術后1個月,4例隨訪患者的術后心功能得到不同程度的改善。1例患者因多器官功能衰竭死亡,這與患者術前自身情況較差以及嚴重的合并癥,如氣管切開狀態、肺部感染、慢性腎功能不全等情況密切相關。1例患者在出院后2個月余因突發腦血管意外死亡,其余3例術后3個月心功能明顯改善,日常生活能力明顯恢復,術后隨訪超聲心動圖顯示未出現輕度以上的瓣周漏和二尖瓣反流。5例患者中有2例在隨訪期間死亡,這與選擇接受“一站式”經心尖TAVR+TEER的患者類型密切相關。我們通常選擇無法接受常規手術治療的多瓣膜病變患者,患者手術風險較大、病情危重,但又迫切需要治療,因此有2例患者出現預后不良,但并非代表手術本身存在很大的風險。但我們的研究也存在一定局限性,樣本量較小,隨訪時間較短,因此在后續的研究中我們將擴大樣本量,并進行中遠期隨訪,進一步驗證該手術的長期安全性和有效性。因此,綜合而言,“一站式”經心尖TAVR+TEER治療高危主動脈瓣膜病變合并重度二尖瓣反流的多瓣膜病變患者具有較好的療效,可以為患者帶來較好的獲益,該治療方案對臨床治療高危主動脈瓣病變合并重度二尖瓣反流的多瓣膜病變具有一定的借鑒意義。
利益沖突:無。
作者貢獻:龔文輝負責論文設計和撰寫,數據采集與分析;高曉天、許金國、韋小勇負責研究設計與數據結果校對;翁光東負責數據統計分析,病例隨訪;張成鑫負責論文審閱與修改。
多瓣膜心臟病(multivalvular heart disease,MHD)是指兩個或以上瓣膜合并狹窄或反流[1]。在老年心臟瓣膜病患者中,MHD尤為常見,如主動脈瓣狹窄合并二尖瓣反流或主動脈瓣關閉不全合并二尖瓣反流等。危重多瓣膜病變極大地增加了外科瓣膜置換或修復手術的風險[2]。因此,許多需要手術干預的多瓣膜病變患者常因手術風險過高而未能接受外科手術治療。
近年來,心臟瓣膜介入技術快速發展,因其創傷小、恢復快等優勢,成為治療外科手術禁忌或高危患者的合理選擇。經導管主動脈瓣置換術(transcatheter aortic valve replacement,TAVR)已成為治療高危主動脈瓣病變的一種理想方法,特別是對于不能耐受體外循環下常規開胸手術的高危患者,TAVR提供了一種新的治療選擇[3]。而經導管二尖瓣緣對緣修復術(transcatheter mitral valve edge-to-edge repair,TEER)也為外科高危的重度二尖瓣反流患者提供了一種有效的治療方法[4]。近期復旦大學中山醫院報道了“一站式”經心尖TAVR+TEER治療重度主動脈瓣關閉不全+二尖瓣反流的案例,術后30 d隨訪結局良好[5]。通過“一站式”經導管TAVR+TEER介入治療同時處理主動脈瓣及二尖瓣多瓣膜病變是一種新的嘗試,為外科高危的多瓣膜病變患者治療帶來新希望。本研究通過回顧我院心臟大血管外科近期完成的“一站式”經心尖TAVR+TEER病例,初步探討該方法在高危主動脈瓣病變合并重度二尖瓣反流的多瓣膜病變患者中的安全性和有效性。
1 資料與方法
1.1 臨床資料
回顧性分析2022年8月—2023年10月在我院心臟大血管外科完成“一站式”TAVR+TEER患者的臨床資料。納入標準:(1)年齡≥65歲;(2)紐約心臟協會(New York Heart Association,NYHA)心功能分級≥Ⅱ級;(3)根據歐洲心臟病學會和歐洲心胸外科協會指南評估需要手術干預的主動脈瓣重度病變患者;(4)原發性二尖瓣反流患者:① 中重度以上二尖瓣反流,② 有臨床癥狀或無臨床癥狀但左心室射血分數≤60%或左心室收縮末期內徑≥40 mm,③ 經心臟外科團隊充分評估外科手術風險較高或無法行外科手術;(5)繼發性二尖瓣反流患者:① 中重度及以上二尖瓣反流,② 經指南指導的規范抗心力衰竭藥物治療后仍有心力衰竭癥狀,③ 超聲心動圖評估左心室射血分數為20%~50%,左心室收縮末期內徑≤70 mm,④ 肺動脈收縮壓≤70 mm Hg(1 mm Hg=0.133 kPa)[2,4,6];(6)二尖瓣病變為A2/P2區、瓣口面積>4 cm2、夾合區瓣葉無鈣化等解剖結構適合行TEER。排除標準:(1)1個月內發生過急性心肌梗死;(2)1個月內急性期腦血管意外;(3)未經治療的嚴重冠狀動脈狹窄,需要血運重建或需要進行其他心臟手術;(4)存在抗凝禁忌;(5)患者預期壽命<1年;(6)左心室射血分數<20%;(7)合并二尖瓣狹窄;(8)有造影劑過敏反應。
1.2 患者診斷及術前準備
術前經胸超聲心動圖評估主動脈瓣、二尖瓣、三尖瓣等瓣葉功能,初步評估為癥狀性中重度主動脈瓣狹窄或主動脈瓣關閉不全、重度二尖瓣反流;通過主動脈CT及冠狀動脈CT血管造影以及3mensio軟件(3mensio Medical Imaging BV,荷蘭)進行圖像分析,規范評估主動脈根部、主動脈瓣及瓣環、冠狀動脈等解剖結構情況[7];通過經食管超聲心動圖進一步評估患者二尖瓣裝置參數,明確二尖瓣病變類型、瓣口面積、前后葉、反流程度等,進一步明確診斷。所有患者術前均經過心臟外科、超聲及麻醉等多學科團隊進行風險評估并制定“一站式”手術具體方案。
1.3 手術方法
手術均在雜交手術室進行。術前使用經食管超聲心動圖再次評估主動脈瓣和二尖瓣病變的相關數據。經左側股動靜脈穿刺置入6F/5F 鞘管,分別放置主動脈造影豬尾導管、起搏導線,并測試起搏導線功能是否正常。透視下行心尖定位后,確定最佳左外側切口位置,手術切口長約4~6 cm。十字切開心包并懸吊于切口,以充分暴露心尖位置,使用3-0 Prolene線帶毛氈片于心尖部縫合雙重六邊形的荷包,在距左前降支外側1~2 cm處選擇荷包縫合位置。全身肝素化(1 mg/kg,活化凝血時間>220 s),主動脈根部造影,在荷包內穿刺置入16~20F血管鞘,后置入150 cm超滑泥鰍導絲,導絲通過主動脈瓣和導管配合過弓到達降主動脈,交換260 cm支撐加硬導絲。對于主動脈瓣狹窄或鈣化患者可行球囊預擴張(球囊至目標位置后,180次/min快速起搏,擴張球囊,回抽后停起搏),退出球囊和鞘管。置入J-Valve瓣膜(蘇州杰成醫療科技有限公司)輸送裝置跨過主動脈瓣瓣口,升主動脈造影定位并進行角度調整,確認定位件置于竇底,調整支架瓣膜位置至主動脈瓣環內,定位后釋放J-valve人工瓣膜。對主動脈瓣狹窄或鈣化患者,可行球囊后擴張。術中釋放后即刻經食管超聲心動圖和造影評估,確認瓣膜定位良好,無瓣周漏,退出導絲及輸送裝置,主動脈瓣置換結束;見圖1。
 圖1
經心尖經導管主動脈瓣置換術(TAVR)手術流程
圖1
經心尖經導管主動脈瓣置換術(TAVR)手術流程
a:術前主動脈根部造影示主動脈瓣反流;b:主動脈瓣嚴重狹窄或鈣化可行球囊預擴張;c:支架瓣膜定位件進入主動脈竇內,瓣膜下降至主動脈瓣環平面;d:瓣膜釋放完畢,主動脈根部造影示支架瓣膜位置及功能完好,撤出輸送裝置;e:主動脈瓣嚴重狹窄或鈣化可行球囊后擴張
經穿刺點置入短導絲,經導絲置入鞘管,置入跨瓣器,超聲引導下過二尖瓣瓣環至左心房,進鞘管至左心房,輕輕擺動跨瓣器,確認其未纏繞二尖瓣腱索后沿引導鞘管退出跨瓣器。裝載MCV-Ⅲ型二尖瓣夾合器(ValveClamp,上海捍宇醫療科技股份有限公司),將夾合器沿引導鞘管送至左心房,反復經胸超聲心動圖定位,使夾子與瓣葉平面垂直并位于A2/P2區,使前后葉均落在二尖瓣夾上,確保夾住瓣緣后收縮夾子,超聲評估見反流明顯減少,瓣口呈現兩瓣口,無明顯狹窄,釋放二尖瓣夾合器,再次超聲評估,若存在中度以上二尖瓣反流,可重復上述步驟,再次置入二尖瓣夾合器。超聲評估效果滿意,退出輸送裝置。心尖荷包打結,止血置引流管,逐層關胸;見圖2。
 圖2
病例3 經心尖經導管二尖瓣緣對緣修復術(TEER)手術流程
圖2
病例3 經心尖經導管二尖瓣緣對緣修復術(TEER)手術流程
a:術前超聲心動圖提示二尖瓣重度反流;b:置入跨瓣器;c:前后夾與二尖瓣開放線垂直,并位于 A2/P2 區;d:收緊夾合器;e:釋放夾合器;f:術后復查超聲心動圖提示二尖瓣反流降為輕度
1.4 資料收集
收集并記錄患者的基線資料:年齡、性別、相關病史、NYHA心功能分級、術前影像學評估結果等。手術資料:瓣膜型號、手術時間、呼吸機輔助時間、ICU住院時間、術后住院時間等。收集術后1個月、3個月內的隨訪結果。
1.5 隨訪及研究終點
所有患者出院后定期通過心臟大血管外科門診或電話隨訪,記錄患者術后臨床癥狀、超聲心動圖結果和不良終點事件發生時間和情況。本研究的主要終點為隨訪期(術后1個月和3個月)內結果,包括心功能分級、主動脈瓣瓣周漏、二尖瓣反流嚴重程度、左心室大小改變和左心室射血分數改變等。次要終點為手術相關并發癥,包括瓣膜移位、夾合器脫落、新發心房顫動或房室傳導阻滯、需要腎臟替代治療的急性腎損傷、再次手術等。
1.6 統計學分析
所有數據采用SPSS 23.0軟件進行分析。服從正態分布的計量資料以均數±標準差( ±s)描述,不服從正態分布的計量資料以中位數(上下四分位數)[M(P25,P75)]描述。計數資料采用例數描述。
±s)描述,不服從正態分布的計量資料以中位數(上下四分位數)[M(P25,P75)]描述。計數資料采用例數描述。
1.7 倫理審查
本研究經安徽醫科大學第一附屬醫院倫理委員會審批通過,倫理審批號:PJ2024-02-42。所有研究對象均簽署知情同意書。
2 結果
2.1 患者基線資料
共納入5例患者,其中男3例、女2例,平均年齡(66.6±1.8)歲。 主動脈瓣關閉不全合并二尖瓣反流4例、主動脈瓣狹窄伴關閉不全合并二尖瓣反流1例。重度原發性二尖瓣反流2例,重度繼發性二尖瓣反流3例。患者年齡、高血壓、糖尿病、心房顫動、腦血管病變、術前心功能分級等資料見表1。
2.2 圍術期結果
5例患者均順利完成“一站式”經心尖TAVR+TEER,所有患者圍術期內未出現死亡、出血、再次手術等不良事件,其中3例患者因術前合并慢性腎功能不全在術后需要接受連續性腎臟替代治療,2例患者因術后呼吸困難再次接受呼吸機輔助治療,1例患者新發房室傳導阻滯。手術時間(179.00±50.67)min,術后呼吸機輔助時間(16.70±3.79)h,術后中位ICU住院時間3.0(2.0,15.0)d,術后中位住院時間7.0(5.5,29.0)d,中位總住院時間24.0(17.0,42.5)d;見表2。
2.3 隨訪結果
術后即刻超聲結果顯示人工主動脈瓣膜植入效果良好,輕度瓣周漏1例。5例患者二尖瓣反流程度由術前的重度降為輕度。術后7 d,5例患者復查超聲心動圖提示人工瓣膜無移位,二尖瓣夾無脫落,瓣葉無損傷。術后1個月隨訪結果顯示4例患者心功能得到不同程度改善,1例患者因多器官功能衰竭死亡。1例患者出院后2個月余突發腦血管意外死亡,其余3例術后3個月超聲心動圖結果顯示左心房內徑、左心室內徑、左心室射血分數以及肺動脈壓均有不同程度改善,未出現輕度以上瓣周漏、主動脈瓣和二尖瓣反流,患者心功能和日常生活能力明顯改善;見表3。
3 討論
隨著人口老齡化的加劇,MHD的發病率持續上升。根據歐洲心臟病學會調查的結果顯示,瓣膜性心臟病患者中≥20%的患者存在MHD,在美國胸外科醫師協會(Society of Thoracic Surgeons,STS)數據庫中納入的60多萬例瓣膜手術患者中,接受多瓣膜手術治療患者占瓣膜手術患者的11%,其中最常見的是主動脈瓣聯合二尖瓣手術[8-9]。一項中國瓣膜性心臟病(China-VHD)注冊登記研究[10]顯示,在納入的13 917例瓣膜性心臟病患者中,MHD患者約為29.0%。雖然MHD在心臟瓣膜病患者中很常見,但其治療和干預一直是一大難題[2]。
外科雙瓣膜手術是治療多瓣膜病變的主要手段,但在高危的老年患者中,同時行雙瓣膜手術會顯著增加并發癥發生率和死亡率[11]。經導管介入瓣膜手術的出現為MHD患者提供了新的治療選擇,TAVR已成為老年或高危主動脈瓣狹窄患者的首選治療方法,并且隨著手術技術的發展和適應證的擴大,TAVR在主動脈瓣關閉不全的治療中同樣發揮著越來越重要的作用[3,12]。TEER被批準用于高危重度原發性二尖瓣反流患者以及經過優化抗心力衰竭治療后仍有癥狀的繼發性二尖瓣反流患者[4]。研究[13]表明,在接受TAVR治療的患者中,約25%的患者合并中度以上二尖瓣反流,合并中重度二尖瓣反流明顯增加了TAVR患者的早期和遠期死亡率。盡管約50%的患者在TAVR后二尖瓣反流分級可以得到改善,特別是合并繼發性或功能性二尖瓣反流的患者,但術后殘留持續性中重度二尖瓣反流的患者預后較差[13-14]。因此對于重度主動脈瓣狹窄和繼發性二尖瓣反流患者,若術后伴有明顯癥狀的持續性二尖瓣反流,如果解剖結構合適,可以考慮分期行TEER。對于重度主動脈瓣狹窄合并重度原發性二尖瓣反流患者,二尖瓣反流分級在TAVR術后改善不明顯,對于此類患者,如果解剖結構合適且TAVR術后二尖瓣反流持續存在,則可以考慮進行分期TEER[15-17]。但迄今為止,經導管多瓣膜手術治療的臨床經驗和結果數據有限,只有少量研究[5,15-17]報道TAVR同期或分期行二尖瓣介入修復或置換的可行性。
Kische等[15]報道12例合并重度二尖瓣反流的患者因心力衰竭癥狀加重,在TAVR后使用MitraClip裝置行TEER,術后患者心功能分級明顯改善,30 d內無患者死亡或重大不良事件發生。一項西班牙的研究[16]表明,5例在TAVR術后存在顯著二尖瓣反流的患者使用MitraClip裝置行TEER,術后二尖瓣反流明顯減少,患者心功能分級和臨床癥狀明顯改善。一項由23家TAVR中心組成的多中心登記研究[17]報道106例在TAVR后接受經導管二尖瓣介入治療患者(100例分期,6例同期,其中TEER 95例)的結局,結果顯示93.2%的患者在TEER術后殘留的中重度二尖瓣反流降為中度或更低(56.8% 輕度或以下,P<0.001),并在6個月和1年內保持穩定(P=0.344 和 P=0.897)。這項研究表明在TAVR后殘留持續癥狀性中重度二尖瓣反流且在解剖學上適合經導管二尖瓣介入治療的患者,接受TAVR和經導管二尖瓣介入分期治療可以顯著改善二尖瓣反流分級和NYHA心功能分級,并且是安全可行的。Zajarias等[18]回顧了STS/美國心臟病學會經導管瓣膜治療登記處257例自體瓣膜或生物瓣膜衰敗同期或分期進行TAVR和經導管二尖瓣置換治療的結果(同期135例,分期122例),結果顯示,針對選定的高危主動脈瓣和二尖瓣病變患者,經導管多瓣膜治療可同期,也可分期,同期和分期治療組30 d和1年卒中率和死亡率是可接受的。上述研究結果為經導管治療多瓣膜病變的安全性和可行性提供了一定基礎,但仍需要進一步的隨機對照研究來評估經導管介入治療在MHD中的療效和安全性。
與現有文獻中大多為主動脈瓣狹窄+二尖瓣反流患者不同,本研究主動脈瓣關閉不全+二尖瓣反流的患者比例較高(主動脈瓣狹窄伴關閉不全+二尖瓣反流 1例,主動脈瓣關閉不全+二尖瓣反流 4例)。主動脈瓣關閉不全+二尖瓣反流在MHD中常見,但指導主動脈瓣關閉不全和二尖瓣反流聯合治療的數據有限[2,8]。主動脈瓣關閉不全合并二尖瓣反流的患者通常伴隨著嚴重的左心室擴張、超容量負荷,患者對手術耐受性較差,術后左心室功能不全的發生率高,術后生存率降低[2,8,19]。因此,此類患者手術方案的選擇不僅取決于單個瓣膜的反流嚴重程度,還取決于患者的年齡、合并癥、虛弱程度以及雙瓣膜手術的風險等多種因素[2,8]。同時,還應充分考慮患者及其家屬手術治療的意愿,選擇最終的治療方案。我院心臟中心團隊經過充分評估和密切配合,使用經心尖途徑的J-Valve人工瓣膜(蘇州杰成醫療科技有限公司)和ValveClamp二尖瓣夾合器(上海捍宇醫療科技股份有限公司)對5例患者順利實施“一站式”經心尖TAVR+TEER[12,20]。術后即刻超聲心動圖結果提示主動脈瓣人工瓣膜位置和功能良好,重度二尖瓣反流即刻降為輕度,未出現二尖瓣瓣葉損傷、二尖瓣夾合器脫落等不良結果。術后1個月,4例隨訪患者的術后心功能得到不同程度的改善。1例患者因多器官功能衰竭死亡,這與患者術前自身情況較差以及嚴重的合并癥,如氣管切開狀態、肺部感染、慢性腎功能不全等情況密切相關。1例患者在出院后2個月余因突發腦血管意外死亡,其余3例術后3個月心功能明顯改善,日常生活能力明顯恢復,術后隨訪超聲心動圖顯示未出現輕度以上的瓣周漏和二尖瓣反流。5例患者中有2例在隨訪期間死亡,這與選擇接受“一站式”經心尖TAVR+TEER的患者類型密切相關。我們通常選擇無法接受常規手術治療的多瓣膜病變患者,患者手術風險較大、病情危重,但又迫切需要治療,因此有2例患者出現預后不良,但并非代表手術本身存在很大的風險。但我們的研究也存在一定局限性,樣本量較小,隨訪時間較短,因此在后續的研究中我們將擴大樣本量,并進行中遠期隨訪,進一步驗證該手術的長期安全性和有效性。因此,綜合而言,“一站式”經心尖TAVR+TEER治療高危主動脈瓣膜病變合并重度二尖瓣反流的多瓣膜病變患者具有較好的療效,可以為患者帶來較好的獲益,該治療方案對臨床治療高危主動脈瓣病變合并重度二尖瓣反流的多瓣膜病變具有一定的借鑒意義。
利益沖突:無。
作者貢獻:龔文輝負責論文設計和撰寫,數據采集與分析;高曉天、許金國、韋小勇負責研究設計與數據結果校對;翁光東負責數據統計分析,病例隨訪;張成鑫負責論文審閱與修改。