引用本文: 易成, 劉嘉燁, 李志輝. 銅綠假單胞菌注射液輔助治療對甲狀腺髓樣癌術后血清降鈣素異常患者預后的影響. 中國普外基礎與臨床雜志, 2024, 31(11): 1313-1318. doi: 10.7507/1007-9424.202411050 復制
甲狀腺髓樣癌(medullary thyroid cancer,MTC)是起源于甲狀腺濾泡旁細胞的惡性腫瘤,占所有類型新發甲狀腺癌的2%~3%[1-2]。根據臨床特性,MTC分為遺傳性(25%)和散發性(75%)兩種類型。盡管這兩種疾病的病因相同,均來源于甲狀腺濾泡旁神經內分泌細胞,但散發性MTC比遺傳性MTC更具侵襲性,并更易轉移到頸部淋巴結[3]。手術切除甲狀腺和局部淋巴結仍然是治療MTC的主要方法。近年來,酪氨酸激酶抑制劑(tyrosine kinase inhibitors,TKIs)在MTC的靶向治療方面取得了顯著進展,改善了晚期MTC患者的無進展生存期[4]。
銅綠假單胞菌注射液由無活性的銅綠假單胞菌甘露糖敏感性血凝素(Pseudomonas aeruginosa mannose-sensitive-hemagglutinin,PA-MSHA)經磷酸鹽緩沖液稀釋而成。PA-MSHA首次分離于1985年。早期銅綠假單胞菌注射液由PA-MSHA制成,現階段通過基因工程、利用菌毛產生的減毒活疫苗已經開始使用。菌毛作為一種具有強黏附能力的糖蛋白樣配體,其末端可與甘露糖特異性結合。通過阻止受體與腫瘤生長和轉移相關的配體結合,菌毛可影響腫瘤的生長和轉移。在多種腫瘤的治療中,銅綠假單胞菌已被驗證具有免疫激活和誘導細胞凋亡的作用[5-8]。目前,銅綠假單胞菌注射液已被中國食品藥品監督管理局批準用于惡性腫瘤的輔助治療。在研究銅綠假單胞菌注射液對術后降鈣素水平異常升高MTC患者預后的影響時,筆者團隊開展了一項回顧性真實世界研究,為盡可能減少混雜因素的影響,采用了傾向得分匹配(propensity score matching,PSM)的方法,旨在探討使用銅綠假單胞菌注射液對MTC術后降鈣素水平異常患者無復發生存(recurrence free survival,RFS)及總生存(overall survival,OS)的影響。
1 資料與方法
1.1 研究對象及分組
本研究回顧性收集2015年1月至2024年4月期間于四川大學華西醫院病理學診斷為MTC患者的臨床資料。納入標準包括:① 病理學診斷為MTC;② 在四川大學華西醫院接受部分或全部甲狀腺切除手術;③ 術后每3個月1次的動態監測過程中出現連續2次血清降鈣素水平高于2倍正常值上限(男性:>19.04 pg/mL,女性:>12.80 pg/mL);④ 除手術治療或銅綠假單胞菌注射液輔助治療外,未接受其他針對 MTC 的治療,如放療、化療或靶向治療;⑤ 有完整可以提取數據的病例信息。排除標準包括:① 曾診斷有其他類型的腫瘤(多發性內分泌瘤除外);② 術后使用銅綠假單胞菌短于12個月;③ 隨訪數據缺失。
銅綠假單胞菌注射液的主要成分是滅活的銅綠假單胞菌-甘露糖敏感血凝菌毛株,該藥物已被批準用于惡性腫瘤的輔助治療。標準給藥方案為:術后1個月開始上臂皮下注射,隔日注射1次,首次注射0.5 mL,之后每次1 mL,連續注射30次,完成30次注射后每個月注射2次,每次1 mL。納入研究的患者根據是否在診斷MTC后使用銅綠假單胞菌注射液分為銅綠組(使用銅綠假單胞菌注射液)及對照組(未使用銅綠假單胞菌注射液)。
1.2 數據收集及處理
本研究的數據提取自四川大學華西醫院病歷系統,提取變量包括:年齡、性別、TNM分期、臨床分級、術后血清降鈣素水平、復發時間及死亡時間。MTC的TNM分期及臨床分級使用美國癌癥委員會第8版甲狀腺髓樣癌分級系統[9-10]。此外,患者使用銅綠假單胞菌的持續時間及劑量信息也提取自醫院病歷系統。數據提取后,對數據缺失情況進行檢查,剔除病例信息不全的患者。
1.3 隨訪
本研究通過評估RFS和OS來確定銅綠假單胞菌注射液的療效。對照組患者的 RFS 定義為從 MTC 根治性手術至首次復發(包括局部復發和區域復發)、遠處轉移、死亡或隨訪截止的時間;銅綠組患者的 RFS 則定義為接受銅綠假單胞菌注射液治療后,從上一次根治性手術到下一次出現復發、遠處轉移、死亡或隨訪截止的時間。OS定義為從首次MTC手術到患者因任何原因死亡或隨訪截止的時間。
隨訪從患者MTC手術日開始,持續至2024年10月1日。隨訪方法包括門診隨訪以及電話隨訪。患者每年隨訪1次,具體隨訪日期根據每例患者的手術日期確定。隨訪信息缺失定義為無法通過電話或筆者所在醫院影像學或病例資料確認患者是否有復發、轉移或發生死亡事件。
1.4 倫理審批
本單中心回顧性隊列研究在開始研究前經四川大學華西醫院生物醫學倫理審查委員會審查通過 [2024年審(687)號)]。由于本研究為回顧性研究,因此免除了書面知情同意的要求。
1.5 統計學方法
本研究數據分析采用Stata軟件(version 18.0)完成(包括基線分析、PSM分析、對數秩檢驗及Cox比例風險回歸模型擬合),RFS和OS曲線采用GraphPad Prism(Version 10.2.0)繪制。原始數據的提取與分析由2位作者獨立完成,并經過仔細復核以確保其準確性。PSM是一種在未進行隨機化情況下評估干預效果的匹配方法,能夠在觀察性隊列研究中減少混雜偏倚的影響。本研究PSM的協變量包括:年齡、性別、術后血清降鈣素水平、臨床分級和復發情況。對銅綠組患者按照近鄰匹配1∶2選擇對照組患者進行匹配。對于患者的基線計量資料,本研究使用Kolmogorov–Smirnov檢驗其正態性,根據數據是否服從正態分布,進行獨立樣本比較的t檢驗和Wilcoxon秩和檢驗。二分類資料由成組χ2檢驗驗證相關性。在匹配后,采用Kaplan-Meier方法繪制RFS和OS曲線,生存分析方法采用對數秩檢驗和Cox比例風險回歸模型,結果采用相對危險度(relative risk,RR)及95%置信區間(confidence interval,CI)表示。檢驗水準α=0.05。
2 結果
2.1 PSM前后銅綠組和觀察組患者的基線特征比較
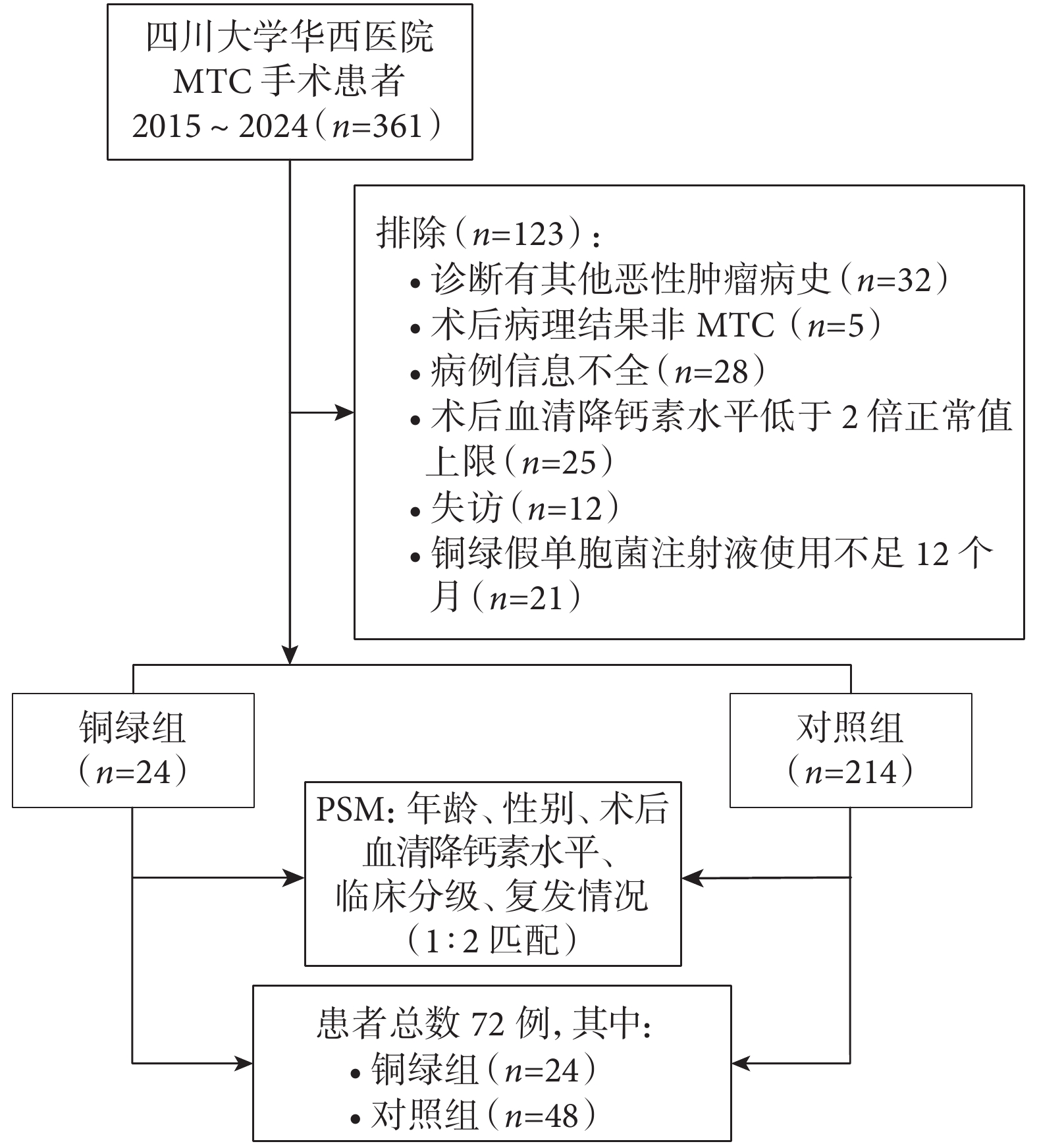
根據納入和排除標準,共納入361例在四川大學華西醫院接受手術的MTC患者,排除123例患者(圖1)。其中接受銅綠假單胞菌治療24例(銅綠組),未接受銅綠假單胞菌治療214例(對照組)。PSM前,2組患者的臨床分級以及復發率比較差異存在統計學意義(P<0.05)。PSM后,共72例患者納入研究,其中銅綠組24例,對照組48例;匹配后2組患者的年齡、術后血清降鈣素水平、性別、臨床分級和復發情況比較差異均無統計學意義(P>0.05),見表1。
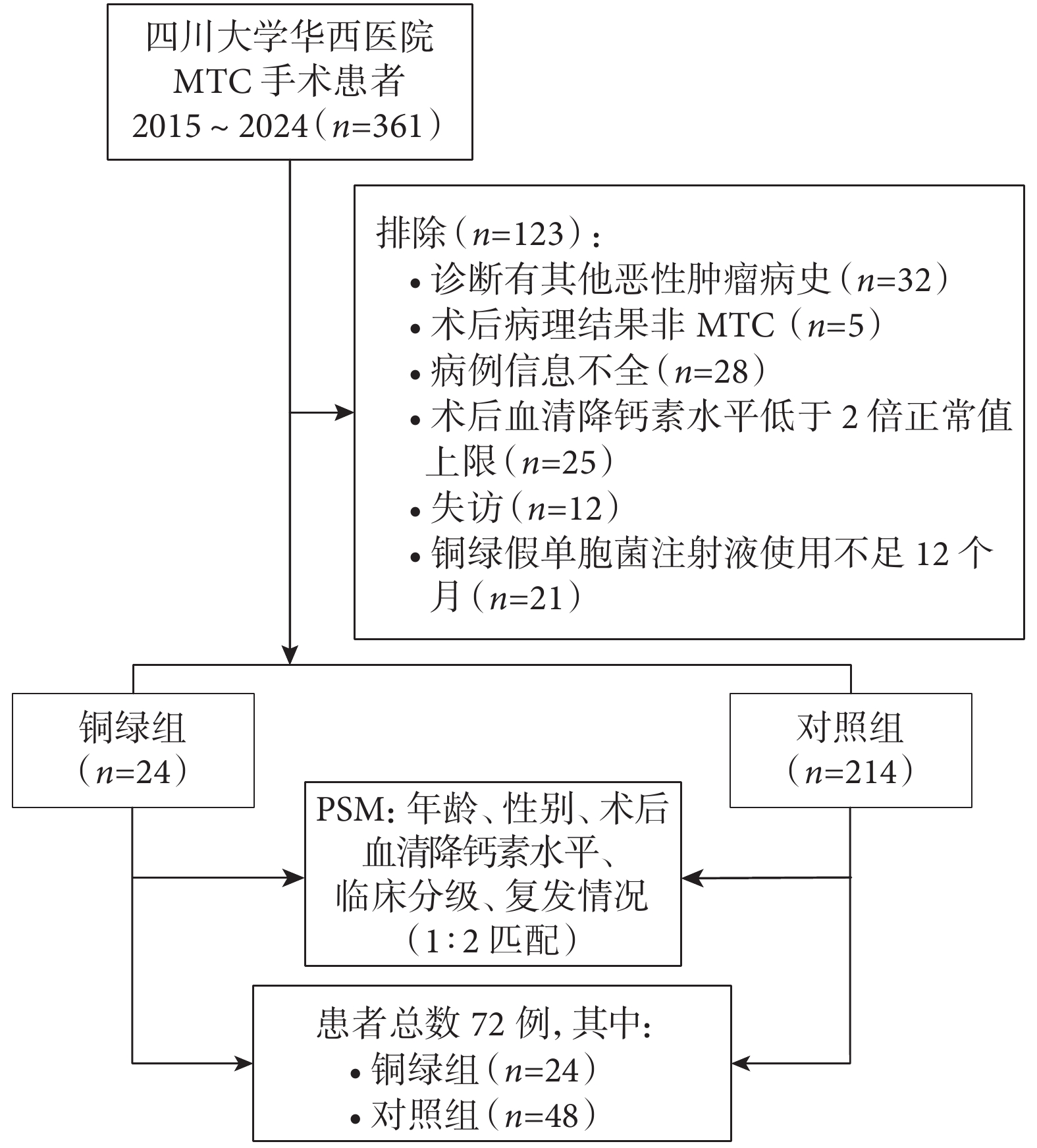 圖1
示患者篩選流程圖
圖1
示患者篩選流程圖
2.2 PSM后銅綠組和觀察組患者的RFS和OS比較
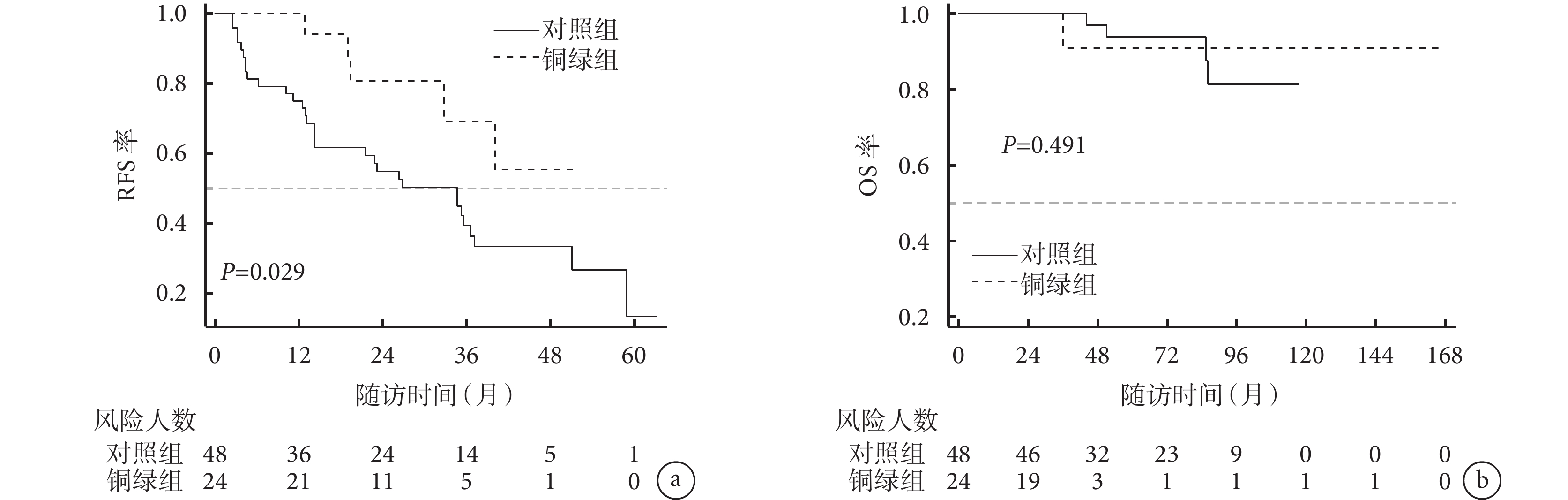
匹配后的72例患者中位隨訪時間為66個月(11~168個月)。隨訪期間,36例患者出現復發,其中銅綠組5例,對照組31例;5例患者死亡,其中銅綠組1例,對照組4例。銅綠組的1年RFS率為100%,對照組為75.0%。銅綠組的2年RFS率為87.5%,對照組為56.3%。2組患者的RFS比較差異有統計學意義(χ2=4.791,P=0.029),銅綠組的RFS較優,見圖2a。銅綠組的5年OS率為90.9%,對照組為93.5%,2組的OS比較差異無統計學意義(χ2=0.469,P=0.491),見圖2b。
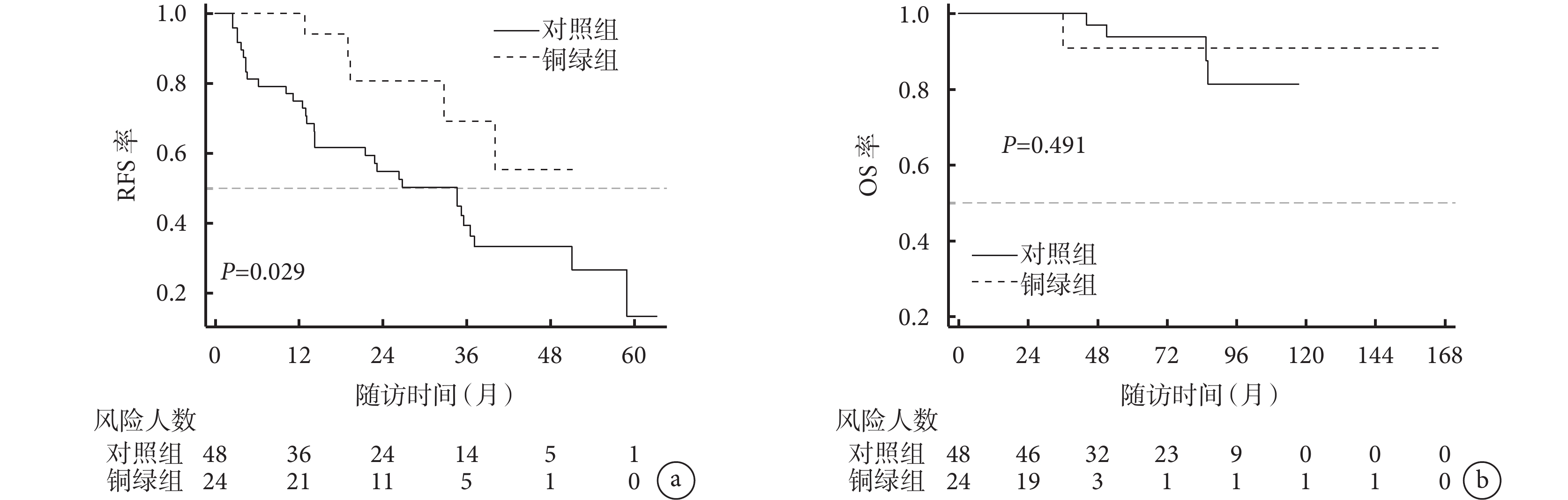 圖2
PSM后2組患者的RFS(a)和OS(b)曲線
圖2
PSM后2組患者的RFS(a)和OS(b)曲線
采用 Cox比例風險回歸模型探索銅綠假單胞菌注射液對預后的影響,結果表明,術后規范使用銅綠假單胞菌注射液的MTC患者,其中位RFS延長 [25個月 vs 21個月,RR=0.350,95%CI(0.135,0.900),P=0.029],但對OS的影響無統計學意義 [66個月 vs 69個月,RR=2.22,95%CI(0.229,21.444),P=0.503]。
3 討論
本研究采用PSM方法探討了銅綠假單胞菌注射液對術后血清降鈣素水平異常MTC患者的療效。在PSM前,對照組中Ⅰ~Ⅲ期、未復發MTC患者占比較高,PSM后2組患者的基線信息,包括年齡、性別、術后血清降鈣素水平、臨床分級和復發情況比較均無統計學意義。PSM后的分析結果表明,銅綠組與對照組患者的RFS比較差異存在統計學意義,但2組患者的OS比較差異無統計學意義。PSM的應用減少了上述混雜因素對最終結果可能產生的影響。
在PSM過程中,納入過多的詳細指標可能導致無效匹配并減少樣本量,選擇匹配自變量的關鍵在于盡量減少混雜偏倚的同時,避免納入過多自變量導致無效匹配。因此,選擇適當的匹配自變量至關重要且具有挑戰性。本研究團隊對指標的選擇進行了深入討論,并參考了已發表的相關文獻[11-12],最終選擇了年齡、性別、術后血清降鈣素水平、臨床分級和復發作為匹配變量。
盡管市面上已有多種酪氨酸激酶抑制劑用于存在RET原癌基因突變的MTC患者,但長期使用這些藥物常導致患者產生耐藥性。因此,亟需開發針對晚期MTC患者的新治療模式。腫瘤應被視為一種包括與癌細胞相關的多種細胞和非細胞成分的復雜組織,這些成分共同構成了腫瘤微環境(tumor microenvironment,TME)。TME包括細胞外基質、間質細胞、免疫炎癥細胞、血液、淋巴管等。甲狀腺癌相關的間質組織成分因不同病理類型而異,MTC細胞則表現出一種致密的間質反應,這與腫瘤的侵襲性和淋巴結轉移相關[13-14]。腫瘤內的免疫和間質細胞可以依賴于特定的環境方式促進或限制惡性狀態[15-16],對MTC免疫微環境的進一步研究可以揭示利用銅綠假單胞菌泛免疫治療晚期MTC的內在機制,明確利用患者免疫系統進行抗癌治療的具體生理過程。
在一項采用銅綠假單胞菌皮下注射與化療聯用治療晚期胃癌患者的臨床研究[17]中,銅綠假單胞菌可增強晚期胃癌術后機體T細胞及自然殺傷細胞的免疫功能,使晚期胃癌術后機體細胞的免疫受損狀態較早恢復,減輕化療期間化療藥物對細胞的免疫抑制作用和化療不良反應,增強對化療的耐受性及療效[18]。提示銅綠假單胞菌聯合傳統一線藥物治療惡性腫瘤能夠從減輕藥物副作用、調節機體免疫狀態等方面使患者達到臨床獲益的目的。多年的臨床應用表明銅綠假單胞菌注射液能有效提高肺癌、淋巴瘤等腫瘤的完全緩解率和有效率[19],降低感染的發生率和感染程度,局部注射能有效降低胸腹部惡性腫瘤的復發率和轉移率[20]。同時,在臨床銅綠假單胞菌注射液能有效調節機體免疫,抵抗感染發生、降低感染程度,并且具有良好的安全性和耐受性[21-22]。
銅綠假單胞菌注射液在TME中誘導炎性反應并激活T細胞活性,同時誘導細胞凋亡,這已在體內外研究中得到驗證[23-25]。目前,銅綠假單胞菌注射液已經被國家藥品監督管理局批準用作惡性腫瘤的輔助治療藥物[26]。本研究將銅綠假單胞菌注射液應用于術后血清降鈣素水平異常的患者人群中,以期通過調節患者TME的免疫狀態,延長患者術后RFS,減少MTC患者的復發。先前的研究[25]表明,銅綠假單胞菌注射液能夠提升非小細胞癌患者對抗程序性死亡受體1(programmed cell death protein 1,PD-1 )治療的敏感性。因此,結合細菌藥物和免疫檢查點抑制的前沿治療方法,為局部晚期不可切除或已有遠處轉移的晚期MTC患者提供了一種新的治療思路,有助于該類癌癥患者的免疫治療,延長其OS。
根據2024版美國國立綜合癌癥網絡(National Comprehensive Cancer Network,NCCN)指南的推薦,MTC的首選治療方法為手術切除。對于術后復發的患者,建議切除復發病灶;對于不可手術切除的病灶,推薦采用全身系統治療,包括凡德他尼、卡博替尼、塞普替尼、普拉替尼等靶向藥物,同時帕博利珠單抗等PD-1抑制劑可能對部分患者有效。在一項331例局部晚期或遠處轉移MTC患者接受凡德他尼治療的研究[26]中,凡德他尼顯著延長了患者的無進展生存期(19.3個月 vs 30.5個月),并在改善患者生存質量方面表現出積極作用。
考慮到MTC在首次手術后的高復發率,患者的隨訪和監測尤為重要。降鈣素持續升高或反復升高通常表明腫瘤病灶殘留或復發。然而,降鈣素水平雖升高但相對穩定的患者,其臨床預后通常較好,因此,對這些患者的隨訪和治療不應過于激進[27-29]。事實上,在術后血清降鈣素水平升高的患者中,有部分患者通過常規的影像學評估手段無法發現復發病灶。因此,本研究引入銅綠假單胞菌這一輔助腫瘤免疫治療藥物,以驗證其延長患者RFS以及OS的有效性。本研究結果表明,銅綠假單胞菌延長MTC術后血清降鈣素異常升高患者的RFS,而對OS影響不明顯,可能與隨訪時間不足有關。MTC的5年生存率為80%~90%,10年生存率約為75%,而本研究的中位隨訪時間僅為66個月。即使在PSM后更多晚期MTC人群被納入研究,但隨訪時間的不足仍可能導致后續的死亡時間未能被充分觀察;因此,尚需進行更長隨訪時間的研究,以進一步觀察銅綠假單胞菌注射液對OS的影響。
總之,本研究結果表明,銅綠假單胞菌注射液改善了術后血清降鈣素升高MTC患者的RFS,這為未來的前瞻性研究提供了現實數據支持,且進一步研究如何優化銅綠假單胞菌注射液在MTC患者中的應用十分必要。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:易成、劉嘉燁共同完成了數據檢索及處理;易成完成了文稿撰寫;李志輝完成了試驗架構設計及文稿審閱。
倫理聲明:本研究已通過四川大學華西醫院醫學倫理審查委員會的審核批準 [批文編號:2024年審(687)號)]。
甲狀腺髓樣癌(medullary thyroid cancer,MTC)是起源于甲狀腺濾泡旁細胞的惡性腫瘤,占所有類型新發甲狀腺癌的2%~3%[1-2]。根據臨床特性,MTC分為遺傳性(25%)和散發性(75%)兩種類型。盡管這兩種疾病的病因相同,均來源于甲狀腺濾泡旁神經內分泌細胞,但散發性MTC比遺傳性MTC更具侵襲性,并更易轉移到頸部淋巴結[3]。手術切除甲狀腺和局部淋巴結仍然是治療MTC的主要方法。近年來,酪氨酸激酶抑制劑(tyrosine kinase inhibitors,TKIs)在MTC的靶向治療方面取得了顯著進展,改善了晚期MTC患者的無進展生存期[4]。
銅綠假單胞菌注射液由無活性的銅綠假單胞菌甘露糖敏感性血凝素(Pseudomonas aeruginosa mannose-sensitive-hemagglutinin,PA-MSHA)經磷酸鹽緩沖液稀釋而成。PA-MSHA首次分離于1985年。早期銅綠假單胞菌注射液由PA-MSHA制成,現階段通過基因工程、利用菌毛產生的減毒活疫苗已經開始使用。菌毛作為一種具有強黏附能力的糖蛋白樣配體,其末端可與甘露糖特異性結合。通過阻止受體與腫瘤生長和轉移相關的配體結合,菌毛可影響腫瘤的生長和轉移。在多種腫瘤的治療中,銅綠假單胞菌已被驗證具有免疫激活和誘導細胞凋亡的作用[5-8]。目前,銅綠假單胞菌注射液已被中國食品藥品監督管理局批準用于惡性腫瘤的輔助治療。在研究銅綠假單胞菌注射液對術后降鈣素水平異常升高MTC患者預后的影響時,筆者團隊開展了一項回顧性真實世界研究,為盡可能減少混雜因素的影響,采用了傾向得分匹配(propensity score matching,PSM)的方法,旨在探討使用銅綠假單胞菌注射液對MTC術后降鈣素水平異常患者無復發生存(recurrence free survival,RFS)及總生存(overall survival,OS)的影響。
1 資料與方法
1.1 研究對象及分組
本研究回顧性收集2015年1月至2024年4月期間于四川大學華西醫院病理學診斷為MTC患者的臨床資料。納入標準包括:① 病理學診斷為MTC;② 在四川大學華西醫院接受部分或全部甲狀腺切除手術;③ 術后每3個月1次的動態監測過程中出現連續2次血清降鈣素水平高于2倍正常值上限(男性:>19.04 pg/mL,女性:>12.80 pg/mL);④ 除手術治療或銅綠假單胞菌注射液輔助治療外,未接受其他針對 MTC 的治療,如放療、化療或靶向治療;⑤ 有完整可以提取數據的病例信息。排除標準包括:① 曾診斷有其他類型的腫瘤(多發性內分泌瘤除外);② 術后使用銅綠假單胞菌短于12個月;③ 隨訪數據缺失。
銅綠假單胞菌注射液的主要成分是滅活的銅綠假單胞菌-甘露糖敏感血凝菌毛株,該藥物已被批準用于惡性腫瘤的輔助治療。標準給藥方案為:術后1個月開始上臂皮下注射,隔日注射1次,首次注射0.5 mL,之后每次1 mL,連續注射30次,完成30次注射后每個月注射2次,每次1 mL。納入研究的患者根據是否在診斷MTC后使用銅綠假單胞菌注射液分為銅綠組(使用銅綠假單胞菌注射液)及對照組(未使用銅綠假單胞菌注射液)。
1.2 數據收集及處理
本研究的數據提取自四川大學華西醫院病歷系統,提取變量包括:年齡、性別、TNM分期、臨床分級、術后血清降鈣素水平、復發時間及死亡時間。MTC的TNM分期及臨床分級使用美國癌癥委員會第8版甲狀腺髓樣癌分級系統[9-10]。此外,患者使用銅綠假單胞菌的持續時間及劑量信息也提取自醫院病歷系統。數據提取后,對數據缺失情況進行檢查,剔除病例信息不全的患者。
1.3 隨訪
本研究通過評估RFS和OS來確定銅綠假單胞菌注射液的療效。對照組患者的 RFS 定義為從 MTC 根治性手術至首次復發(包括局部復發和區域復發)、遠處轉移、死亡或隨訪截止的時間;銅綠組患者的 RFS 則定義為接受銅綠假單胞菌注射液治療后,從上一次根治性手術到下一次出現復發、遠處轉移、死亡或隨訪截止的時間。OS定義為從首次MTC手術到患者因任何原因死亡或隨訪截止的時間。
隨訪從患者MTC手術日開始,持續至2024年10月1日。隨訪方法包括門診隨訪以及電話隨訪。患者每年隨訪1次,具體隨訪日期根據每例患者的手術日期確定。隨訪信息缺失定義為無法通過電話或筆者所在醫院影像學或病例資料確認患者是否有復發、轉移或發生死亡事件。
1.4 倫理審批
本單中心回顧性隊列研究在開始研究前經四川大學華西醫院生物醫學倫理審查委員會審查通過 [2024年審(687)號)]。由于本研究為回顧性研究,因此免除了書面知情同意的要求。
1.5 統計學方法
本研究數據分析采用Stata軟件(version 18.0)完成(包括基線分析、PSM分析、對數秩檢驗及Cox比例風險回歸模型擬合),RFS和OS曲線采用GraphPad Prism(Version 10.2.0)繪制。原始數據的提取與分析由2位作者獨立完成,并經過仔細復核以確保其準確性。PSM是一種在未進行隨機化情況下評估干預效果的匹配方法,能夠在觀察性隊列研究中減少混雜偏倚的影響。本研究PSM的協變量包括:年齡、性別、術后血清降鈣素水平、臨床分級和復發情況。對銅綠組患者按照近鄰匹配1∶2選擇對照組患者進行匹配。對于患者的基線計量資料,本研究使用Kolmogorov–Smirnov檢驗其正態性,根據數據是否服從正態分布,進行獨立樣本比較的t檢驗和Wilcoxon秩和檢驗。二分類資料由成組χ2檢驗驗證相關性。在匹配后,采用Kaplan-Meier方法繪制RFS和OS曲線,生存分析方法采用對數秩檢驗和Cox比例風險回歸模型,結果采用相對危險度(relative risk,RR)及95%置信區間(confidence interval,CI)表示。檢驗水準α=0.05。
2 結果
2.1 PSM前后銅綠組和觀察組患者的基線特征比較
根據納入和排除標準,共納入361例在四川大學華西醫院接受手術的MTC患者,排除123例患者(圖1)。其中接受銅綠假單胞菌治療24例(銅綠組),未接受銅綠假單胞菌治療214例(對照組)。PSM前,2組患者的臨床分級以及復發率比較差異存在統計學意義(P<0.05)。PSM后,共72例患者納入研究,其中銅綠組24例,對照組48例;匹配后2組患者的年齡、術后血清降鈣素水平、性別、臨床分級和復發情況比較差異均無統計學意義(P>0.05),見表1。
 圖1
示患者篩選流程圖
圖1
示患者篩選流程圖
2.2 PSM后銅綠組和觀察組患者的RFS和OS比較
匹配后的72例患者中位隨訪時間為66個月(11~168個月)。隨訪期間,36例患者出現復發,其中銅綠組5例,對照組31例;5例患者死亡,其中銅綠組1例,對照組4例。銅綠組的1年RFS率為100%,對照組為75.0%。銅綠組的2年RFS率為87.5%,對照組為56.3%。2組患者的RFS比較差異有統計學意義(χ2=4.791,P=0.029),銅綠組的RFS較優,見圖2a。銅綠組的5年OS率為90.9%,對照組為93.5%,2組的OS比較差異無統計學意義(χ2=0.469,P=0.491),見圖2b。
 圖2
PSM后2組患者的RFS(a)和OS(b)曲線
圖2
PSM后2組患者的RFS(a)和OS(b)曲線
采用 Cox比例風險回歸模型探索銅綠假單胞菌注射液對預后的影響,結果表明,術后規范使用銅綠假單胞菌注射液的MTC患者,其中位RFS延長 [25個月 vs 21個月,RR=0.350,95%CI(0.135,0.900),P=0.029],但對OS的影響無統計學意義 [66個月 vs 69個月,RR=2.22,95%CI(0.229,21.444),P=0.503]。
3 討論
本研究采用PSM方法探討了銅綠假單胞菌注射液對術后血清降鈣素水平異常MTC患者的療效。在PSM前,對照組中Ⅰ~Ⅲ期、未復發MTC患者占比較高,PSM后2組患者的基線信息,包括年齡、性別、術后血清降鈣素水平、臨床分級和復發情況比較均無統計學意義。PSM后的分析結果表明,銅綠組與對照組患者的RFS比較差異存在統計學意義,但2組患者的OS比較差異無統計學意義。PSM的應用減少了上述混雜因素對最終結果可能產生的影響。
在PSM過程中,納入過多的詳細指標可能導致無效匹配并減少樣本量,選擇匹配自變量的關鍵在于盡量減少混雜偏倚的同時,避免納入過多自變量導致無效匹配。因此,選擇適當的匹配自變量至關重要且具有挑戰性。本研究團隊對指標的選擇進行了深入討論,并參考了已發表的相關文獻[11-12],最終選擇了年齡、性別、術后血清降鈣素水平、臨床分級和復發作為匹配變量。
盡管市面上已有多種酪氨酸激酶抑制劑用于存在RET原癌基因突變的MTC患者,但長期使用這些藥物常導致患者產生耐藥性。因此,亟需開發針對晚期MTC患者的新治療模式。腫瘤應被視為一種包括與癌細胞相關的多種細胞和非細胞成分的復雜組織,這些成分共同構成了腫瘤微環境(tumor microenvironment,TME)。TME包括細胞外基質、間質細胞、免疫炎癥細胞、血液、淋巴管等。甲狀腺癌相關的間質組織成分因不同病理類型而異,MTC細胞則表現出一種致密的間質反應,這與腫瘤的侵襲性和淋巴結轉移相關[13-14]。腫瘤內的免疫和間質細胞可以依賴于特定的環境方式促進或限制惡性狀態[15-16],對MTC免疫微環境的進一步研究可以揭示利用銅綠假單胞菌泛免疫治療晚期MTC的內在機制,明確利用患者免疫系統進行抗癌治療的具體生理過程。
在一項采用銅綠假單胞菌皮下注射與化療聯用治療晚期胃癌患者的臨床研究[17]中,銅綠假單胞菌可增強晚期胃癌術后機體T細胞及自然殺傷細胞的免疫功能,使晚期胃癌術后機體細胞的免疫受損狀態較早恢復,減輕化療期間化療藥物對細胞的免疫抑制作用和化療不良反應,增強對化療的耐受性及療效[18]。提示銅綠假單胞菌聯合傳統一線藥物治療惡性腫瘤能夠從減輕藥物副作用、調節機體免疫狀態等方面使患者達到臨床獲益的目的。多年的臨床應用表明銅綠假單胞菌注射液能有效提高肺癌、淋巴瘤等腫瘤的完全緩解率和有效率[19],降低感染的發生率和感染程度,局部注射能有效降低胸腹部惡性腫瘤的復發率和轉移率[20]。同時,在臨床銅綠假單胞菌注射液能有效調節機體免疫,抵抗感染發生、降低感染程度,并且具有良好的安全性和耐受性[21-22]。
銅綠假單胞菌注射液在TME中誘導炎性反應并激活T細胞活性,同時誘導細胞凋亡,這已在體內外研究中得到驗證[23-25]。目前,銅綠假單胞菌注射液已經被國家藥品監督管理局批準用作惡性腫瘤的輔助治療藥物[26]。本研究將銅綠假單胞菌注射液應用于術后血清降鈣素水平異常的患者人群中,以期通過調節患者TME的免疫狀態,延長患者術后RFS,減少MTC患者的復發。先前的研究[25]表明,銅綠假單胞菌注射液能夠提升非小細胞癌患者對抗程序性死亡受體1(programmed cell death protein 1,PD-1 )治療的敏感性。因此,結合細菌藥物和免疫檢查點抑制的前沿治療方法,為局部晚期不可切除或已有遠處轉移的晚期MTC患者提供了一種新的治療思路,有助于該類癌癥患者的免疫治療,延長其OS。
根據2024版美國國立綜合癌癥網絡(National Comprehensive Cancer Network,NCCN)指南的推薦,MTC的首選治療方法為手術切除。對于術后復發的患者,建議切除復發病灶;對于不可手術切除的病灶,推薦采用全身系統治療,包括凡德他尼、卡博替尼、塞普替尼、普拉替尼等靶向藥物,同時帕博利珠單抗等PD-1抑制劑可能對部分患者有效。在一項331例局部晚期或遠處轉移MTC患者接受凡德他尼治療的研究[26]中,凡德他尼顯著延長了患者的無進展生存期(19.3個月 vs 30.5個月),并在改善患者生存質量方面表現出積極作用。
考慮到MTC在首次手術后的高復發率,患者的隨訪和監測尤為重要。降鈣素持續升高或反復升高通常表明腫瘤病灶殘留或復發。然而,降鈣素水平雖升高但相對穩定的患者,其臨床預后通常較好,因此,對這些患者的隨訪和治療不應過于激進[27-29]。事實上,在術后血清降鈣素水平升高的患者中,有部分患者通過常規的影像學評估手段無法發現復發病灶。因此,本研究引入銅綠假單胞菌這一輔助腫瘤免疫治療藥物,以驗證其延長患者RFS以及OS的有效性。本研究結果表明,銅綠假單胞菌延長MTC術后血清降鈣素異常升高患者的RFS,而對OS影響不明顯,可能與隨訪時間不足有關。MTC的5年生存率為80%~90%,10年生存率約為75%,而本研究的中位隨訪時間僅為66個月。即使在PSM后更多晚期MTC人群被納入研究,但隨訪時間的不足仍可能導致后續的死亡時間未能被充分觀察;因此,尚需進行更長隨訪時間的研究,以進一步觀察銅綠假單胞菌注射液對OS的影響。
總之,本研究結果表明,銅綠假單胞菌注射液改善了術后血清降鈣素升高MTC患者的RFS,這為未來的前瞻性研究提供了現實數據支持,且進一步研究如何優化銅綠假單胞菌注射液在MTC患者中的應用十分必要。
重要聲明
利益沖突聲明:本文全體作者閱讀并理解了《中國普外基礎與臨床雜志》的政策聲明,我們沒有相互競爭的利益。
作者貢獻聲明:易成、劉嘉燁共同完成了數據檢索及處理;易成完成了文稿撰寫;李志輝完成了試驗架構設計及文稿審閱。
倫理聲明:本研究已通過四川大學華西醫院醫學倫理審查委員會的審核批準 [批文編號:2024年審(687)號)]。